Είτε στην Ελλάδα, είτε στην πολιτισμένη Ευρώπη, που όλοι οι ξενολάτρες Ελληναράδες έχουν σαν πρότυπο και πολύ ψηλά στην εκτίμηση τους το αστυνομικό σώμα φαίνεται να έχει την ίδια συμπεριφορά και αντίληψη..Πολίτες όλου του κόσμου μπορείτε να νιώθετε ασφαλείς αφού το άρτια εκπαιδευμένο και εξοπλισμένο ανθρώπινο δυναμικό της αστυνομίας σας προστατεύει όλο το 24ωρο από “απειλές” όπως η παρακάτω..Εσείς ακόμα δεν είδατε το καλό πρόσωπο της αστυνομίας??
Πέμπτη 31 Μαρτίου 2011
Τρίτη 29 Μαρτίου 2011
Παρέλαση 25ης Μαρτίου 2011 στη Σύρο
Πέρυσι την 25η Μαρτίου στην στρατιωτική παρέλαση της Αθήνας ντράπηκα που έγινα θεατής του παρακάτω περιστατικού . Εν έτη 2ο1ο τότε, τα “καμάρια” του στρατού, μας ρεζίλεψαν και μας παρουσίασαν σαν ανεγκέφαλους και αμόρφωτους νταήδες.. Και μετά όσοι αρέσκονται σε τέτοιου τύπου συνθήματα έχουν το θράσος να λένε βαρύγδουπες εκφράσεις του τύπου “Πας μη Έλλην, βάρβαρος”. Μόνο που οι βάρβαροι εκείνη την ημέρα δεν ήταν ούτε οι Αλβανοί, ούτε οι Τούρκοι, ούτε οι κάτοικοι της Παπούα Νέας Γουινέας ή όποιοι άλλοι μπορείτε να φανταστείτε..Βάρβαροι ήταν αυτοί που με περίσσεια θράσους φώναζαν αυτά τα συνθήματα και όσοι τους επικροτούσαν.Σε έναν από τους πιο ιστορικούς δρόμους της Αθήνας, σε ένα δρόμο πολιτισμού, ακριβώς δίπλα από το Πανεπιστήμιο μας, την Ακαδημία και τη Βιβλιοθήκη..Κτίρια και έννοιες που ποτέ δεν πρόκειται να συλλάβουν με το φτωχό τους μυαλουδάκι ποια είναι η αξία τους και η σημασία τους..
Αυτά γίνανε πέρυσι κ μακάρι να μην ξανασυμβούν αν και αυτό είναι λίγο απίθανο με το μορφωτικό επίπεδο τέτοιων ανθρώπων..Φέτος όμως στη Σύρο, την οποία και έκανε το λάθος να επισκεφθεί ο George Papandreou Junior και με αφορμή το “πολύ προοδευτικό” νομοσχέδιο περί των συγχωνεύσεων των σχολείων της “πολύ προοδευτικής” ηγεσίας της χώρας μας, ακολούθησε το παρακάτω περιστατικό..Οι μαθητές της Σύρου που έκαναν παρέλαση αντί να στρέψουν το κεφάλι τους προς τη πλευρά των επισήμων για το συνήθη χαιρετισμό, στράφηκαν επιδεικτικά προς την αντίθετη κατεύθυνση, στο άγαλμα του Μιαούλη και στο πλήθος που παρευρίσκονταν εκεί..Είναι η πρώτη φορά που συμβαίνει κάτι τέτοιο σε παρέλαση, ένα “επεισόδιο” από τους ίδιους τους μαθητές και όχι από τραμπούκους χρυσαυγίτες η άλλων πολιτικών χώρων..
Πόσο μεγάλη διαφορά αντιδράσεων για τα δυο γεγονότα πέρυσι κ φέτος..Πόσο μεγάλη διαφορά στην αντίληψη αυτών των ανθρώπων..Τέτοια γεγονότα έρχονται να σε γεμίσουν αισιοδοξία ότι ο κόσμος δεν “κοιμάται”..Είναι έτοιμος ανά πάσα στιγμή να αντιδράσει.. Άλλαξε ο κόσμος? -Όχι.. Άλλαξε το πολιτικό σύστημα? –Όχι ακόμα..Έγινε όμως ένα ακόμη βήμα προς την αλλαγή αυτού του τόπου, ως προς το να μην θεωρούνται όλα δεδομένα πλέον και ότι τα πράγματα ίσως να μην μπορούν να τα ελέγξουν απόλυτα οι ισχυροί που διοικούν.. Ίσως ο κόσμος να αρχίζει να συνειδητοποιεί ότι η απειλή και ο εχθρός αυτής της χώρας δεν είναι εξ’ ολοκλήρου εκτός συνόρων και κυρίως όχι σε αυτούς που μέχρι τώρα μας παρουσίαζαν ως εχθρούς..Ίσως να γίνεται κατανοητό ότι τα μεγάλα προβλήματα αυτής της χώρας δεν θα αφανιστούν αν λυθεί το μεταναστευτικό των Πακιστανών και λοιπών έγχρωμων και μη (και εμείς οι Έλληνες για άλλη μια φορά στην ιστορία μας έχουμε αρχίσει να μεταναστεύουμε πάλι προς την Ευρώπη και την Αμερική χωρίς να φταίνε οι μετανάστες για αυτό..)..Ούτε οι Τούρκοι είναι αυτοί που απειλούν τα σύνορα μας (πλέον οι κατακτήσεις δεν γίνονται με πόλεμο ούτε γίνονται για τις γραμμές των συνόρων αλλά με την οικονομική κυριαρχία κατακτούνται πλέον τα κράτη)..Όταν έχουμε ξεπουλήσει όλες μας τις υπηρεσίες και σιγά σιγά παρέχουμε τη γη μας και τους δίνουμε και το δικαίωμα να μας εξουσιάζουν υπακούοντας στις εντολές τους τότε θα πρέπει να αναζητήσουμε την απειλή κάπου πιο βόρεια και δυτικά ίσως, και όχι ανατολικά όπως προσπαθούν να μας πείσουν μέχρι τώρα.. Άλλωστε αν οι Ευρωπαίοι, οι Αμερικάνοι και το ΝΑΤΟ είναι όντως σύμμαχοι και συμπαραστάτες μας και θέλουν το “καλό” μας, γιατί δεν μας διασφαλίζουν ότι μέχρι να ξεχρεωθούν τα χρέη της Ελλάδας τα σύνορα μας θα μείνουν ακέραια και δεν θα χρειάζεται να ξοδεύουμε υπέρογκα ποσά για στρατιωτικούς εξοπλισμούς..Γιατί τα σύνορα της Ελλάδας είναι και τα σύνορα της Ευρώπης από την ανατολή..Για μια ακόμη φορά δεν θα βοηθήσουν όπως και δεν το έκαναν ποτέ (θυμηθείτε τη σφαγή στη Σμύρνη όπου τα πλοία των μεγάλων δυνάμεων ήταν απέναντι από το λιμάνι και απλά παρακολουθούσαν τις αγριότητες).Οι μόνες φορές που βοήθησαν ήταν μόνο όταν το επέβαλλε το συμφέρον τους και μόνο τότε..Και τώρα το συμφέρον τους είναι να είμαστε υποταγμένοι με την σύγχρονη μορφή υποταγής..Το Χρέος..
Αυτά γίνανε πέρυσι κ μακάρι να μην ξανασυμβούν αν και αυτό είναι λίγο απίθανο με το μορφωτικό επίπεδο τέτοιων ανθρώπων..Φέτος όμως στη Σύρο, την οποία και έκανε το λάθος να επισκεφθεί ο George Papandreou Junior και με αφορμή το “πολύ προοδευτικό” νομοσχέδιο περί των συγχωνεύσεων των σχολείων της “πολύ προοδευτικής” ηγεσίας της χώρας μας, ακολούθησε το παρακάτω περιστατικό..Οι μαθητές της Σύρου που έκαναν παρέλαση αντί να στρέψουν το κεφάλι τους προς τη πλευρά των επισήμων για το συνήθη χαιρετισμό, στράφηκαν επιδεικτικά προς την αντίθετη κατεύθυνση, στο άγαλμα του Μιαούλη και στο πλήθος που παρευρίσκονταν εκεί..Είναι η πρώτη φορά που συμβαίνει κάτι τέτοιο σε παρέλαση, ένα “επεισόδιο” από τους ίδιους τους μαθητές και όχι από τραμπούκους χρυσαυγίτες η άλλων πολιτικών χώρων..
Πόσο μεγάλη διαφορά αντιδράσεων για τα δυο γεγονότα πέρυσι κ φέτος..Πόσο μεγάλη διαφορά στην αντίληψη αυτών των ανθρώπων..Τέτοια γεγονότα έρχονται να σε γεμίσουν αισιοδοξία ότι ο κόσμος δεν “κοιμάται”..Είναι έτοιμος ανά πάσα στιγμή να αντιδράσει.. Άλλαξε ο κόσμος? -Όχι.. Άλλαξε το πολιτικό σύστημα? –Όχι ακόμα..Έγινε όμως ένα ακόμη βήμα προς την αλλαγή αυτού του τόπου, ως προς το να μην θεωρούνται όλα δεδομένα πλέον και ότι τα πράγματα ίσως να μην μπορούν να τα ελέγξουν απόλυτα οι ισχυροί που διοικούν.. Ίσως ο κόσμος να αρχίζει να συνειδητοποιεί ότι η απειλή και ο εχθρός αυτής της χώρας δεν είναι εξ’ ολοκλήρου εκτός συνόρων και κυρίως όχι σε αυτούς που μέχρι τώρα μας παρουσίαζαν ως εχθρούς..Ίσως να γίνεται κατανοητό ότι τα μεγάλα προβλήματα αυτής της χώρας δεν θα αφανιστούν αν λυθεί το μεταναστευτικό των Πακιστανών και λοιπών έγχρωμων και μη (και εμείς οι Έλληνες για άλλη μια φορά στην ιστορία μας έχουμε αρχίσει να μεταναστεύουμε πάλι προς την Ευρώπη και την Αμερική χωρίς να φταίνε οι μετανάστες για αυτό..)..Ούτε οι Τούρκοι είναι αυτοί που απειλούν τα σύνορα μας (πλέον οι κατακτήσεις δεν γίνονται με πόλεμο ούτε γίνονται για τις γραμμές των συνόρων αλλά με την οικονομική κυριαρχία κατακτούνται πλέον τα κράτη)..Όταν έχουμε ξεπουλήσει όλες μας τις υπηρεσίες και σιγά σιγά παρέχουμε τη γη μας και τους δίνουμε και το δικαίωμα να μας εξουσιάζουν υπακούοντας στις εντολές τους τότε θα πρέπει να αναζητήσουμε την απειλή κάπου πιο βόρεια και δυτικά ίσως, και όχι ανατολικά όπως προσπαθούν να μας πείσουν μέχρι τώρα.. Άλλωστε αν οι Ευρωπαίοι, οι Αμερικάνοι και το ΝΑΤΟ είναι όντως σύμμαχοι και συμπαραστάτες μας και θέλουν το “καλό” μας, γιατί δεν μας διασφαλίζουν ότι μέχρι να ξεχρεωθούν τα χρέη της Ελλάδας τα σύνορα μας θα μείνουν ακέραια και δεν θα χρειάζεται να ξοδεύουμε υπέρογκα ποσά για στρατιωτικούς εξοπλισμούς..Γιατί τα σύνορα της Ελλάδας είναι και τα σύνορα της Ευρώπης από την ανατολή..Για μια ακόμη φορά δεν θα βοηθήσουν όπως και δεν το έκαναν ποτέ (θυμηθείτε τη σφαγή στη Σμύρνη όπου τα πλοία των μεγάλων δυνάμεων ήταν απέναντι από το λιμάνι και απλά παρακολουθούσαν τις αγριότητες).Οι μόνες φορές που βοήθησαν ήταν μόνο όταν το επέβαλλε το συμφέρον τους και μόνο τότε..Και τώρα το συμφέρον τους είναι να είμαστε υποταγμένοι με την σύγχρονη μορφή υποταγής..Το Χρέος..
Ετικέτες
Μαθητικός Παλμός,
Πολιτική-Οικονομία
Σάββατο 26 Μαρτίου 2011
Η Αλχημεία στην Τέχνη ανά τους Αιώνες
Η Αλχημεία, όπως ήταν φυσικό λόγω της δυσκολίας της να γίνει κατανοητή από το ευρύ κοινό, ανά τους αιώνες, δημιούργησε δεισιδαιμονίες μεν, αλλά και θαυμασμό στα μάτια του κόσμου, κάτι βέβαια που δεν μπορούσε να μην αποτυπωθεί στην τέχνη εκείνων των εποχών..
Παρακάτω είναι μερικά παραδείγματα πινάκων ζωγραφικής και όχι μόνο, με θέμα την Αλχημεία..

Παρακάτω είναι μερικά παραδείγματα πινάκων ζωγραφικής και όχι μόνο, με θέμα την Αλχημεία..

Ταοϊστής Μοναχός Αλχημιστής
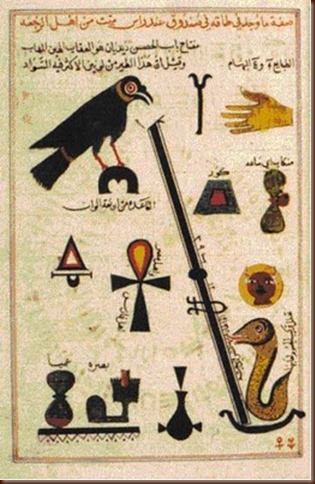
Έγγραφο Αραβικής Αλχημείας
Αλχημιστής επί τω έργω
Άλλος ένας Αλχημιστής επί τω έργω
H. Khunrath, Amphitheatrum sapientiae aeternae, 1602. Κοσμολογική απεικόνιση του αλχημιστικού έργου με τη μορφή του βολβού του οφθαλμού.
D. Stolcius von Stolcenberg, Viridarium chymicum, Φρανκφούρτη 1624. Στα 4 στοιχεία (από αριστερά γη, νερό, αέρας, φωτιά) αντιστοιχούν οι 4 φάσεις του αλχημιστικού έργου και οι 4 βαθμοί του πυρός.
Arabic manuscript in the Museum of Fine Arts in Boston.
An emblem from Honoratus Marinier’s ca. 1790 Alchemical Manuscript of the Seven Keys (McLean’s edition).
Giacinto Grimaldi. Dell’Alchimia. Palermo, 1645.
Το βυζαντινό Υγρό Πυρ
M. Maler, (Atalanta fugiens), Oppenheim 1618. Η γέννηση της φιλοσοφικής λίθου στον αέρα
Ζωγραφική απεικόνιση αλχημιστή στο εργαστήριο του...
Ζωγραφική απεικόνιση αλχημιστή στο εργαστήριο του..
Ζωγραφική απεικόνιση αλχημιστή στο εργαστήριο του.
Ζωγραφική απεικόνιση εργαστηριού αλχημείας
Η πυρίτιδα ανακαλύφθηκε από τους Κινέζους κατά τον 8ο μ.Χ. αιώνα. Ενώ αρχικά χρησιμοποιήθηκε για ψυχαγωγία (πυροτεχνήματα), σύντομα διαπιστώθηκε η χρησιμότητά της στις πολεμικές επιχειρήσεις.
Αλχημιστής σε αναζήτηση της Φιλοσοφικής Λίθου. Ζωγραφικός πίνακας (1771) του Joseph Wright, όπου απεικονίζεται ο αλχημιστής Hennig Brand (1630-1710)να ανακαλύπτει τον φωσφόρο. Αυτό συνέβη "κατά λάθος", όταν ο Brand αναζητούσε τη Φιλοσοφική Λίθο στο στερεό υπόλειμμα μεγάλης ποσότητας ούρων.
Ετικέτες
Επιστήμη της Χημείας,
Πολιτιστικά
Κυριακή 20 Μαρτίου 2011
Σύντομη Ιστορία της Χημείας
1. Η Χημεία από τις Προϊστορικές Εποχές
Η ιστορία της Χημείας ξεκινάει από την εποχή που οι προϊστορικοί άνθρωποι άρχισαν να ενδιαφέρονται για τα υλικά που χρησιμοποιούσαν για να κατασκευάσουν τις καλύβες τους, τα κεραμικά και γυάλινα σκεύη, τα μεταλλικά αντικείμενα και άλλα είδη καθημερινής χρήσης. Συγχρόνως, οι άνθρωποι άρχισαν να πειραματίζονται για το πως θα βελτίωναν τις ιδιότητες και την ποιότητα των υλικών και των αντικειμένων αυτών, αναμιγνύοντας διάφορα συστατικά και εφαρμόζοντας διάφορους τρόπους επεξεργασίας. Κάπου εκεί θα πρέπει να αναζητηθούν οι απαρχές της Χημείας, σε καμιά περίπτωση βέβαια ως επιστήμης, αλλά σαν μια μεθοδολογία που βασιζόταν σε εμπειρικές παρατηρήσεις του τύπου "δοκιμής και λάθους". Ωστόσο, και το τυχαίο αποδίδει, όταν διατίθεται άφθονος χρόνος.

Η Εύφορη Ημισέληνος, είναι η περιοχή που περιλαμβάνει τη Μεσοποταμία, δηλ. τις κοιλάδες των ποταμών Τίγρη και Ευφράτη. Στις περιοχές αυτές, για πρώτη φορά, αναπτύχθηκαν τουλάχιστον πριν 10.000 χρόνια διάφοροι πολιτισμοί αγροτικού χαρακτήρα.
Η ιστορία της Χημείας και τα εξελικτικά στάδιά της πέρασαν μέσα από τις εποχές των πανάρχαιων πολιτισμών των Σουμέριων και των Αιγυπτίων, τις φιλοσοφικές αναζητήσεις των υλιστικών φιλοσόφων της Αρχαίας Ελλάδας, των Ινδών και Κινέζων πειραματιστών και στη συνέχεια των Ρωμαίων και των Μουσουλμάνων, που ανακάλυψαν πλήθος νέων χημικών ουσιών και νέες πρακτικές μεθόδους παρασκευής τους.
Οι πρώτες χημικές γνώσεις διαδόθηκαν ταχύτατα στη Μεσαιωνική Ευρώπη, χάρις στους Αλχημιστές. Με μια πορεία μέσα από παρανοήσεις και λάθη, μέσα από ένα συνονθύλευμα μυστικισμού, προκαταλήψεων και παράξενων θρησκευτικών δοξασιών, κατάφερε να αναδειχθεί η Χημεία ως ένας αυτεξούσιος επιστημονικός κλάδος κάπου κατά τον 17ου αιώνα, χάρις στη δουλειά λίγων πραγματικά φωτισμένων ανθρώπων.
Η λέξη Αλχημεία προέρχεται από το αραβικό οριστικό άρθρο Αλ- και τη λέξη Χημεία (al-kimya). Η προέλευση της λέξης Χημεία παραμένει ακόμη και σήμερα αντικείμενο πολλών θεωριών και αναζητήσεων. Η επικρατέστερη εκδοχή είναι ότι σχετίζεται με τις λέξεις χημία και χυμεία.
Η "χημία" εικάζεται ότι προέρχεται από την αρχαία αιγυπτιακή λέξη κεμ (= μαύρος), διότι ως τέχνη και επιστήμη συνδέθηκε με την Αίγυπτο, που σύμφωνα με τον Πλούταρχο ονομαζόταν και ως Μαύρη Γη ή Μαύρη Χώρα. Ακόμη μπορεί να σχετίζεται με τη μετατροπή των "μαύρων" ορυκτών και μεταλλευμάτων σε χρήσιμες ουσίες και μέταλλα.
Η λέξη χυμεία (khymeia) προέρχεται από το ρήμα χέω και τη διαδικασία της χύτευσης και αναφέρονταν στην ανάμιξη χρυσού και αργύρου με σύντηξη, που εκτελούσαν οι χυμευτές. Υπάρχει Βυζαντινό έγγραφο όπου αναφέρεται ότι παλαιότερα ο Ρωμαίος Αυτοκράτορας Διοκλητιανός (245-312 μ.Χ.) είχε διατάξει την καταστροφή όλων των Αιγυπτιακών βιβλίων που σχετίζονταν με τη χυμεία, δηλ. τη σύντηξη χρυσού και αργύρου.
Μια ακόμη εκδοχή για την προέλευση της λέξης "χημεία" προσφέρεται από έναν 'Ελληνα ή Αιγύπτιο αλχημιστή των πρωτοχριστιανικών αιώνων, τον Ζώσιμο τον Πανοπολίτη (4ος-5ος αιώνας). Στο βιβλίο του με τίτλο Ιμούθ (μια από τις αποδόσεις του ονόματος του Φαραώ Imhotep, 2655-2600 π.Χ., σε ελληνικά κείμενα), γράφει για τη γένεση της Αλχημείας, σύμφωνα με την οποία ο "πρώτος των τεχνών" ήταν ο Χημεύ (με αιγυπτιακή γραφή: "Chêmi"), από τον οποίο προέρχεται "το όνομα της χημείας".

Ο χρυσός και ο χαλκός είναι από τα λίγα μέταλλα που βρίσκονται στη φύση ελεύθερα. Το γεγονός αυτό σε συνδυασμό με το χαμηλό σημείο τήξεως, δικαιολογεί το γεγονός ότι ήταν τα πρώτα μέταλλα που γνώρισε και επεξεργάστηκε ο άνθρωπος.


Διακοσμητικά μεταλλικά αντικείμενα (από χαλκό και κράματά του) από τον πολιτισμό των Σουμερίων (Πόλη Ούρ, Μεσοποταμία).
Ανεξάρτητα πάντως της προέλευσης της λέξης Χημεία, το βέβαιο είναι οι δύο αρχαίοι πολιτισμοί της Αιγύπτου και της Ελλάδας συνέβαλαν αποφασιστικά στην προώθηση και στην εξέλιξης της Χημείας.
Πηγές από το Διαδίκτυο: (1) "Etymology of Chemistry" (Journal of Chemical Education). (2) "Chemistry (etymology)" (Wikipedia). (3) "Η Αλχημία στα Βυζαντινά Χρόνια" (Νικόλαος Βασ. Λίτσας, Αρχαιολογία και Τέχνες, τχ. 107)
2. Η Απαρχή της Χημείας στη Μεσοποταμία
Η ιστορία της Χημείας ξεκινά από την εποχή της δημιουργίας των πρώτων αγροτικών πολιτισμών στην περιοχή των ποταμών Τίγρη και Ευφράτη, στην περιοχή η οποία στα ιστορικά δοκίμια αναφέρεται ως Εύφορη Ημισέληνος (Fertile Crescent).
 Στην περιοχή αυτή αναπτύχθηκαν οι πρώτοι αγροτικοί πολιτισμοί (8.000-10.000 π.Χ.). Τα νερά των ποταμών που πλημμύριζαν την κοιλάδα και η πλούσια σε θρεπτικά συστατικά λάσπη, βοηθούσαν τις συστηματικές αγροτικές καλλιέργειες και επομένως συνέβαλαν στη μόνιμη εγκατάσταση λαών που μέχρι τότε ζούσαν νομαδικά, αναζητώντας τροφή από κυνήγι και άγρια φρούτα και λαχανικά.
Στην περιοχή αυτή αναπτύχθηκαν οι πρώτοι αγροτικοί πολιτισμοί (8.000-10.000 π.Χ.). Τα νερά των ποταμών που πλημμύριζαν την κοιλάδα και η πλούσια σε θρεπτικά συστατικά λάσπη, βοηθούσαν τις συστηματικές αγροτικές καλλιέργειες και επομένως συνέβαλαν στη μόνιμη εγκατάσταση λαών που μέχρι τότε ζούσαν νομαδικά, αναζητώντας τροφή από κυνήγι και άγρια φρούτα και λαχανικά.
Η Μεσοποταμία έγινε το λίκνο πλούσιων πολιτισμών και δημιουργίας μεγάλων πόλεων, όπως η Βαβέλ (Βαβυλώνα) και η Ουρ. Εκεί αναπτύχθηκε ο πανάρχαιος πολιτισμός των Σουμερίων (4η χιλιετηρίδα π.Χ.). Οι Σουμέριοι ανέπτυξαν τη γραφή σε εγχάρακτες πλάκες, την κεραμική με τη χρήση του κεραμευτικού τροχού και τη μεταλλουργία για την κατασκευή οικιακών εργαλείων και δοχείων, αλλά και όπλων.
Ευρήματα που ανάγονται στο 6.000 π.Χ., αποδεικνύουν πως από τότε ήταν ήδη γνωστές τεχνικές επεξεργασίας μεταλλευμάτων για την παρασκευή μεταλλικού χαλκού. Ακολούθησαν οι περισσότερες συστηματικές μεταλλουργικές πρακτικές και πιο εξελιγμένες τεχνικές της μεταλλουργίας (καθαρισμός μεταλλευμάτων με υψηλές θερμοκρασίες, χύτευση, εμπλουτισμός).
Στη συνέχεια διαπίστωσαν ότι ο χαλκός που παρασκευαζόταν με αναγωγή ορυκτών χαλκού αναμιγμένων με ορυκτά κασσιτέρου, ήταν σκληρότερος και ανθεκτικότερος. 'Ετσι, ανακαλύφθηκε ο ορείχαλκος, κράμα χαλκού-κασσιτέρου (με 10 έως 20% κασσίτερο). 'Ετσι, ήδη από το 3.800-4.000 π.Χ. οι Σουμέριοι γνώριζαν τα κράματα.
Με βάση αρχαιολογικά ευρήματα, εκτιμάται ότι κατά χρονολογική σειρά ανακαλύφθηκαν και άρχισε να γίνεται η χρήση των ακόλουθων μετάλλων (σε παρένθεση: η εκτιμούμενη χρονολογία κατασκευής/χρήσης του αρχαιότερου μεταλλικού αντικειμένου): Χρυσός (6.000 π.Χ.), χαλκός (4.200 π.Χ.), άργυρος (4.000 π.Χ.), μόλυβδος (3.500 π.Χ.), κασσίτερος (1.750 π.Χ.), σίδηρος (1.500 π.Χ.), υδράργυρος (750 π.Χ.).
Τότε περίπου άρχισε να γίνεται αισθητή και η ανάγκη για καύσιμα, τόσο για τις καθημερινές ανάγκες των πληθυσμών, όσο και για τη μεταλλουργία. Οι ανάγκες αυτές σε μεγάλο μέρος τους καλύπτονταν από την άσφαλτο και άλλα πισσώδη υλικά, που αφθονούσαν στην περιοχή της Μεσοποταμίας και ανάβλυζαν από ρωγμές των εδαφών.

Η τυχαία ανακάλυψη του γυαλιού και ορισμένα γυάλινα φιαλίδια της ρωμαϊκής εποχής, όταν είχε πλέον εξελιχθεί κατά πολύ η τέχνη της υαλουργίας.
Παράλληλα, οι κάτοικοι των περιοχών αυτών άρχισαν να ασχολούνται με τη βαφική. Χρησιμοποιούσαν χρώματα, που παρασκεύαζαν από εκχυλίσματα καρπών και φλοιών δέντρων ή από έγχρωμα ορυκτά υλικά, για να βάφουν υφάσματα, αλλά και το ίδιο το δέρμα τους για καλλωπιστικούς λόγους. Σύντομα διαπίστωσαν τις απορρυπαντικές ιδιότητες της στάχτης ξύλων. Βρήκαν τρόπους να παραλαμβάνουν τα αιθέρια έλαια από αρωματικά φυτά και τους καρπούς τους και να παρασκευάζουν αρώματα και καλλυντικά.
Η βυρσοδεψία ήταν μια ακόμη δραστηριότητα. Μέσω της χρήσης χημικών υλικών, βελτίωναν σημαντικά την ποιότητα και την αντοχή των δερμάτινων προϊόντων.
'Οταν διαπίστωσαν πως στις φωτιές που άναβαν καίγοντας ξύλα στην άμμο, έβρισκαν ανάμεσα στις στάχτες κάτι περίεργες σχεδόν διαφανείς συμπαγείς μάζες (αποτέλεσμα της σύντηξης της άμμου με τα ανθρακικά άλατα του καλίου από τη στάχτη των ξύλων), άρχισαν να σκέφτονται πως θα μπορούσαν να αξιοποιήσουν αυτό το περίεργο νέο υλικό που δεν ήταν άλλο από το γυαλί.

Αρχαία αιγυπτιακή τοιχογραφία με απεικόνιση εργασιών σε διάφορα εργαστήρια.
Οι παραπάνω τέχνες και τεχνικές βελτιώθηκαν με πειραματισμό και βαθμιαία καθιερώθηκαν μεθοδολογίες και πρακτικές που μεταβιβάζονταν από γενεά σε γενεά. Οι αρχαίοι τεχνίτες δεν είχαν βέβαια ιδέα για τη χημεία των υλικών, αλλά είχαν αποκτήσει με την πάροδο των χρόνων ένα πλούτο από πρακτικές γνώσεις.
Πηγές από το Διαδίκτυο: (1) "The Fertile Crescent" (University of Victoria, Canada). (2) "Sumerians" (AncientScripts.com). (3) "History of Metallurgy". (4) "A Short History of Metals" (Alan W. Cramb, Carnegie Mellon University). (5) "A Brief History of Glass" (GlassOnLine.com).
3. Η Χημεία κατά την Περίοδο της Αρχαίας Αιγύπτου
Η Αρχαία Αίγυπτος χαρακτηρίσθηκε από τον πλούσιο αρχαίο πολιτισμό της που εξελίχθηκε από τις προϊστορικές εποχές (περίπου 3.300 π.Χ.) μέχρι το 31 π.Χ., όταν η Αίγυπτος κατέστη επαρχία της Ρωμαϊκής Αυτοκρατορίας.
Η Αίγυπτος με τα πολυάριθμα σταθερά βασίλεια και με τα πολιτισμικά επιτεύγματα (3.200 π.Χ.: γραφή με ιερογλυφικά, 3.100 π.Χ.: χρήση δεκαδικού συστήματος αρίθμησης, 3.100 π.Χ.: κελάρια κρασιού, 2.700 π.Χ.: χειρουργική τεχνική, 2.500 π.Χ.: κατασκευή της μεγάλης πυραμίδας της Giza), αποτελεί ένα πλούσιο σε εξελίξεις στάδιο στην ιστορία της Χημείας. Πολλές τεχνικές που είχαν ήδη αναπτυχθεί και καθιερωθεί στη Μεσοποταμία μεταφέρθηκαν και εξελίχθηκαν ακόμη περισσότερο στην Αρχαία Αίγυπτο.
Μερικές τεχνικές της αρχαίας Αιγυπτιακής χημείας προξενούν και σήμερα το ενδιαφέρον για τις πλούσιες γνώσεις που διέθεταν για πολλά χημικά υλικά και τις ιδιότητές τους. Κατέγραφαν με λεπτομέρειες διάφορες τεχνικές και τα αποτελέσματα διάφορων δοκιμών. Οι γνώσεις πολλών από αυτών των τεχνικών, είχαν την έννοια της τέχνης παρά της επιστήμης και αποτελούσαν αποκλειστικό προνόμιο της τάξης των ιερέων.

Αιματίτης, Fe2O3

Ορυχείο κίτρινης ώχρας, ένυδρο Fe2O3

Αζουρίτης, Cu3(OH)2(CO3)2

Μαλαχίτης, Cu2CO3(OH)2

Κιννάβαρι, HgS

Ερυθρά σανδαράχη (realgar), As2S2

Κίτρινη σανδαράχη (orpiment), As2S3

Αντιμονίτης, Sb2S3

Γαληνίτης, PbS
Μερικά από τα ορυκτά που χρησιμοποιούσαν οι αρχαίοι πολιτισμοί ως χρώματα.
Η σύγχρονη Ιατρική οφείλει πολλά στους αρχαίους Αιγυπτίους. Στην αρχή, επειδή ο άνθρωπος δεν μπορούσε να εξηγήσει όλα όσα του συνέβαιναν, άρχισε να τα αποδίδει σε υπερφυσικές δυνάμεις. Οι αρρώστιες θεωρήθηκαν έργα κακών πνευμάτων ή τιμωρία από μια θεότητα. Ο Imhotep (2655-2600 BC), 'Ιμυθες για τους αρχαίους 'Ελληνες, υπήρξε ο πιο διάσημος Αιγύπτιος ιατρός-παθολόγος, που ήταν συγχρόνως αστρονόμος και αρχιτέκτονας. Ο Imhotep χρησιμοποιούσε διάφορες χημικές ουσίες για θεραπείες ασθενειών. Αργότερα, ο Imhotep λατρεύτηκε ως θεός της Θεραπείας και της Ιατρικής.
Οι Αιγύπτιοι ανέπτυξαν τις τεχνικές της μεταλλουργίας και έγιναν εξειδικευμένοι τεχνικοί για την κατεργασία του χρυσού από μεταλλεύματα και να το αναμιγνύουν με άλλα μέταλλα για να είναι σταθερότερο. Γνώριζαν την παρασκευή ορείχαλκου (μπρούτζου) από χαλκό και κασσίτερο. Ευρήματα σιδηρών αντικειμένων σε πυραμίδες δίνουν την εντύπωση ότι γνώριζαν και τρόπους παρασκευής χάλυβα (ατσάλι) ήδη από το 2.900 π.Χ.
Η υαλουργία υπήρξε ένας ακόμη τομέας στον οποίο οι αρχαίοι Αιγύπτιοι έκαναν σημαντικές προόδους. Τα ευρήματα μεγάλων φούρνων υαλουργίας (ανασκαφές στην περιοχή Tel-El-Amarna, χρονολογούμενοι γύρω στο 1400 π.Χ.) και τα διάφορα είδη υάλινων σκευών και κοσμημάτων από έγχρωμο γυαλί δείχνουν μια υψηλή τεχνική κατάρτιση και γνώση αυτών των υλικών. 'Ετσι φαίνεται ότι γνώριζαν την κατασκευή μολυβδούχου υάλου (κρυστάλλου), όπως επίσης γνώριζαν πως μπορούσαν να χρησιμοποιήσουν κοβαλτιούχα ορυκτά για την παρασκευή βαθυκύανης υάλου. Ακόμη, γνώριζαν να κατασκευάζουν υαλώματα (σμάλτα) από οξείδια διαφόρων μετάλλων και να καλύπτουν με αυτά τις επιφάνειες πήλινων δοχείων και άλλων πήλινων αντικειμένων.
Οι αρχαίοι Αιγύπτιοι σημείωσαν εξαιρετικές προόδους στην υφαντουργία, γνώριζαν την κατασκευή υφασμάτων από βαμβάκι και μαλλί και τρόπους χρώσης τους με φυσικές ουσίες. Τυπικά ανόργανα υλικά που χρησιμοποιούσαν σε βαφές ήταν ο αιματίτης (Fe2O3) για κόκκινο χρώμα, βαθυκύανο τριμμένο γυαλί (ύαλος κοβαλτίου) για μπλε, βασικά ανθρακικά άλατα χαλκού για γαλάζιο χρώμα (αζουρίτης) και πράσινο χρώμα (μαλαχίτης), κίτρινη ώχρα (ένυδρο Fe2O3) για κίτρινο. Με τα ίδια χρώματα και τα υλικά που χρησιμοποιούσαν έβαφαν ανάκτορα, ναούς, σπίτια και τάφους.
Οι Αιγύπτιοι ανέπτυξαν τεχνικές και μεθόδους για την παρασκευή χρωστικών ουσιών από ανόργανα υλικά και από φυτικές ουσίες. Χρησιμοποίησαν τη φωτιά για την ανάμιξη και τη συνθετική παρασκευή χρωμάτων (με υγρές χημικές μεθόδους και χημικά στάδια). 'Ηδη από το 3.000 π.Χ., χρησιμοποιούσαν ορυκτά, όπως ο γαληνίτης (PbS) και ο αντιμονίτης (Sb2S3) σε ψιμύθια (καλλυντικά προσώπου). Για παράδειγμα, μίγμα λειοτριβημένου αντιμονίτη και λίπους, χρησιμοποιούσαν ως καλλυντική βαφή, για να βάφουν μαύρο το περίγραμμα των ματιών. Πιθανώς επίσης γνώριζαν και τον υδράργυρο, αφού χρησιμοποιούσαν το ορυκτό κιννάβαρι (HgS) για τη ερυθρά χρώση υφασμάτων. Οι γνώσεις αυτές μεταφέρθηκαν και εφαρμόσθηκαν και στην Αρχαία Ελλάδα, αλλά ήταν ήδη τόσο προχωρημένες τεχνικές που δεν χρειάσθηκε να βελτιωθούν.
Τέλος, οι αρχαίοι Αιγύπτιοι ανέπτυξαν τις τεχνικές για την παρασκευή αρωμάτων και ελαιωδών αλοιφών για το δέρμα. Οι τεχνικές που χρησιμοποιούσαν ήταν εξαιρετικά αναπτυγμένες και οι ανακαλύψεις και οι συνθέσεις τους αξιοποιήθηκαν και από άλλους πολιτισμούς που ακολούθησαν τον Αιγυπτιακό.

(1)

(2)

(3)

(4)

(5)
Αρχαία Αίγυπτος: (1) Γυάλινο δοχείο. (2) Μεταλλικό δακτυλίδι. (3) Υαλουργικές εργασίες. (4) Συλλογή φιαλιδίων με καλλυντικά. (5) Μεταφορά φυτών μυρτιάς για την παρασκευή αρωμάτων
4. Οι Αρχαίοι 'Ελληνες Φιλόσοφοι και η Συμβολή τους στη Χημεία
Η αρχαία Ελλάδα και ο πολιτισμός της είναι ασφαλώς η συνέχεια του πολιτισμού της αρχαίας Αιγύπτου με μια όμως πολύ μεγαλύτερη δυναμική. Οι αρχαίοι 'Ελληνες αξιοποίησαν πολλά από τα επιτεύγματα των Αιγυπτίων στις τεχνικές της μεταλλουργίας, της υαλουργίας, της βαφής υφασμάτων και των αρωματικών υλών. Οι τεχνικές αυτές ήταν ήδη πολύ εξελιγμένες και δεν χρειάστηκαν ουσιαστικά να προσθέσουν νέες βελτιώσεις ή κάποιες αλλαγές στις μεθοδολογίες.
Τους αρχαίους Έλληνες απασχολούσε όχι τόσο το "πώς", αλλά το "γιατί", δηλ. η αναζήτηση της αλήθειας και των αιτίων. Σύμφωνα με τους αρχαιολόγους, η συνεισφορά των Αρχαίων Ελλήνων και διανοητών στις φυσικές επιστήμες ήταν κυρίως οι θεωρητικές έννοιες. Στην αρχαία Ελλάδα πραγματοποιήθηκε για πρώτη φορά η απόδοση των φυσικών φαινομένων σε φυσικά αίτια και η αντικατάσταση των υπερφυσικών δυνάμεων από τους φυσικούς νόμους.






Εμπεδοκλής (495 - 435 π.Χ.)
Λεύκιππος (5ος αιώνα π.Χ., δάσκαλος του Δημόκριτου)
Δημόκριτος
(460-370 π.Χ.)
Πλάτων
(428-348 π.Χ.)
Αριστοτέλης
(384-322 π.Χ.)
Επίκουρος
(341 - 270 π.Χ.)
Οι ιδέες των αρχαίων Ελλήνων φιλοσόφων ήταν η απαρχή πολλών σημερινών εννοιών των φυσικών επιστημών. Η αρχαία ελληνική φυσική φιλοσοφία είχε μεγάλη επίδραση και στη σύγχρονη χημεία, είτε άμεσα, είτε έμμεσα, έστω και μέσω των παραδοξοτήτων της αλχημείας. Μερικές από αυτές τις ιδέες που βρήκαν εφαρμογή στη χημεία ακόμη και σήμερα είναι:

Το κλασικό διάγραμμα ενός τετραγώνου εγγεγραμμένου σε ένα άλλο. Στις γωνίες του ενός βρίσκονται τα βασικά στοιχεία και στις γωνίες του άλλου βρίσκονται οι ιδιότητές τους.
(α) Η έννοια του στοιχείου. Η θεωρία των τεσσάρων βασικών στοιχείων ή ριζωμάτων (γη, ύδωρ, πυρ και αήρ) διατυπώθηκε από τον Εμπεδοκλή (495-435 π.Χ., από Ακράγαντα, Σικελία). Τα τέσσερα στοιχεία ήταν μέρος της φιλοσοφικής του συμβολής και ιδιαίτερα το ποίημα (2.000 στίχοι) "Περί Φύσεως". Τα πάντα είναι συνδυασμοί αυτών των τεσσάρων στοιχείων. Στα στοιχεία αυτά αποδίδονται κυκλικά οι ιδιότητες "υγρό", "θερμό", "ξηρό" και "ψυχρό" ως πρωτεύουσες ή δευτερεύουσες. Ο "αήρ" είναι πρωτίστως "υγρός" και δευτερευόντως "θερμός", το "πυρ" είναι πρωτίστως "θερμό" και δευτερευόντως "ξηρό", η "γη" είναι πρωτίστως "ξηρή" και δευτερευόντως "ψυχρή" και το "ύδωρ" είναι πρωτίστως "ψυχρό" και δευτερευόντως "υγρό".
(β) Η έννοια του ατόμου. Η ατομική θεωρία για τη συγκρότηση ύλης διατυπώθηκε αρχικά από τον Λεύκιππο (5ος αιώνας π.Χ., Μίλητος). Για τον Λεύκιππο είναι λίγα πράγματα γνωστά. 'Εζησε κατά την περίοδο (περίπου) 480-420 π.Χ. Παρακολούθησε την Ιονική σχολή φιλοσοφίας, σπούδασε και στην Ελέα (σήμερα Velia, στη νότια Ιταλία) και φαίνεται ότι επηρεάστηκε κυρίως από τον προσωκρατικό φιλόσοφο Ζήνωνα τον Ελεάτη (490;-430; π.Χ.). Ίδρυσε σχολή στα 'Αβδηρα της Θράκης. Η ατομική θεωρία του Λεύκιππου διατυπώθηκε πιο συστηματικά από τον μαθητή του Δημόκριτο (460-370 π.Χ., 'Αβδηρα, Θράκη). Η ατομική θεωρία όριζε ότι τα άτομα είναι τα έσχατα μόρια της ύλης. Τα άτομα (: α-στερητικό + τομή) είναι άτμητα, άφθαρτα, αναλλοίωτα και κινούνται αδιάκοπα στον χώρο. Υπάρχουν άπειρα είδη ατόμων σε συνεχή κίνηση και οποιαδήποτε μεταβολή της ύλης δεν είναι παρά ένα είδος ανασυνδυασμού των ατόμων.
(γ) Η διατήρηση της μάζας. Η θεωρία της αφθαρσίας της ύλης που διατύπωσαν παράλληλα ο Δημόκριτος και ο Διογένης ο Απολλωνιάτης (5ος αιώνας π.Χ.).

Πλάτωνας και Αριστοτέλης. Λεπτομέρεια από τον περίφημο πίνακα του Raphael "Η Σχολή των Αθηνών" (1510).
Οι ιδέες αυτές διαδόθηκαν κυρίως με τη διδασκαλία του Επίκουρου και αργότερα από το εκτενές φιλοσοφικό ποίημα του Λουκρητίου (Τίτος Λουκρήτιος Κάρος, 98-53 π.Χ., Ρωμαίος φιλόσοφος) που είχε τίτλο De Rerum Natura (Περί της Φύσεως των Πραγμάτων), όπου και εξηγούσε τις αρχές της ατομικής θεωρίας του Δημόκριτου.
Ο Επίκουρος (Σάμος 341- Αθήνα 270 π.Χ.) ήταν 'Ελληνας φιλόσοφος, ο οποίος ίδρυσε τη φιλοσοφική σχολή που έμεινε γνωστή ως "Επικούρειος Κήπος". Στόχος του Επίκουρου ήταν η αναζήτηση των αιτιών της ανθρώπινης δυστυχίας και των εσφαλμένων δοξασιών που την προκαλούν, όπως η δεισιδαιμονία.
Βασικές αρχές της διδασκαλίας του Επίκουρου είναι οι εξής: Με τον θάνατο έρχεται το τέλος όχι μόνο του σώματος αλλά και της ψυχής - οι θεοί ούτε επιβραβεύουν, ούτε τιμωρούν τους ανθρώπους. Το σύμπαν είναι άπειρο και αιώνιο - τα γενόμενα στον κόσμο συμβαίνουν τελικά, με βάση τις κινήσεις και τις αλληλεπιδράσεις των ατόμων που βρίσκονται σε έναν κενό χώρο.
Οι υλιστικές απόψεις του Επίκουρου πολεμήθηκαν άγρια από μεταγενέστερους φιλοσόφους και θεολόγους. Ο ίδιος κατασυκοφαντήθηκε και χαρακτηρίστηκε ως άτομο με ροπή προς τις ηδονές και τις απολαύσεις. Θα πρέπει να σημειωθεί ότι οι υλιστικές ιδέες και η αντίληψη περί ατόμων και αφθαρσίας της ύλης αναπτύχθηκαν περίπου την ίδια περίοδο από Ινδούς φιλοσόφους (Βεδική φιλοσοφία), αλλά με αρκετά πιο ήπιους τόνους και με ποιητική διάθεση.
Οι ατομικές θεωρίες του Δημόκριτου για την ύλη έμειναν στο περιθώριο για πολλούς αιώνες. Οι υλιστικές θεωρίες περί ατόμων, αφθαρσίας της ύλης και των στοιχείων δεν είχαν προοπτική διάδοσης, αφού έπεσαν στη δυσμένεια των φιλοσόφων Πλάτωνα (428-348 π.Χ.) και Αριστοτέλη (384-322 π.Χ.).
Ο Αριστοτέλης, ο πολυγραφότερος διαλεκτικός φιλόσοφος της αρχαιότητας, επηρέασε με τις θεωρίες του τη δυτική φιλοσοφική και επιστημονική σκέψη μέχρι και τον 17ο αιώνα. Ο Αριστοτέλης μελέτησε και έγραψε για πολλούς κλάδους (φιλοσοφία, ψυχολογία, λογική, πολιτική, φυσική, βιολογία, κ.α.). 'Εγραψε πολλά βιβλία για τη Φυσική (φυσική ακρόαση, περί ουρανού, περί γενέσεως και φθοράς, μετεωρολογικά και περί κόσμου) και τη Βιολογία (περί ζώων ιστορίας, περί ζώων μορίων, περί ζώων πορείας, περί ζώων κινήσεως, περί ζώων γενέσεως και περί φυτών).
Η φιλοσοφία του Αριστοτέλη κλείνει προς τον ιδεαλισμό και θέτει τον υλισμό σε μια μάλλον παθητική μοίρα. Σύμφωνα με τις θεωρίες του κάθε πράγμα αποτελείται από ύλη και πνεύμα, που είναι μεταξύ τους αδιάσπαστα ενωμένα. Η ύλη είναι παθητική και μόνη της παρέχει τη δυνατότητα, ενώ το πνεύμα ενεργητικό, και αποτελεί τη δύναμη που μεταβάλλει τη δυνατότητα σε πραγματικότητα.
Ο κόσμος, κατά τον Αριστοτέλη, είναι ενιαίος και αιώνιος και το σύμπαν ή ο κόσμος είναι σφαιρικός με κέντρο τη Γη. Η θεωρία αυτή ταίριαζε με τις θρησκευτικές αντιλήψεις και η γεωκεντρική εικόνα επικράτησε μέχρι την εποχή του Γαλιλαίου. Μέσω της τυπικής λογικής βλέπει την αντικειμενική πραγματικότητα "στατικά" και όχι μέσα στην αέναη μεταβολή και κίνησή της. Ο Αριστοτέλης διετύπωσε τη θεωρία της ύπαρξης του πέμπτου στοιχείου της φύσης (πέραν των τεσσάρων: γη, ύδωρ, πυρ και αήρ, που πίστευαν οι 'Ιωνες φιλόσοφοι). Ο Αριστοτέλης πρόσθεσε τον αιθέρα (: καθαρός, φρέσκος αέρας, καθαρός ουρανός) στο κέντρο του κλασικού τετραγώνου των στοιχείων. Ο αιθέρας παρουσιάζει κάποιες ιδιαιτερότητες ως στοιχείο, είναι: αγέννητος, αγήραντος, άφθαρτος, αΐδιος (αιώνιος), αναυξής και αναλλοίωτος. Ο αιθέρας θα ταυτισθεί αργότερα με τη Φιλοσοφική Λίθο των αλχημιστών. Επιπλέον εντοπίζεται στον "άνω τόπο" όπου κατοικεί η Θεότητα.

Να σημειωθεί στο σημείο αυτό, ότι η πρώτη αναφορά στην έννοια στοιχείον έγινε από τον Πλάτωνα, περίπου το 360 π.Χ. στον διάλογό του "Τίμαιος", όπου περιλαμβάνεται μια συζήτηση πάνω στη σύνθεση των ανόργανων και των οργανικών σωμάτων, μια πρωταρχική προσέγγιση πάνω στη χημεία. Ο Πλάτωνας θεωρούσε ότι το μικρότερο σωματίδιο κάθε στοιχείου αντιστοιχούσε σε ένα από τα πέντε κανονικά πολύεδρα, δηλ. κυρτά πολύεδρα με έδρες κανονικά πολύγωνα και ίδιες, τα οποία είναι γνωστά και ως "Πλατωνικά στερεά": το τετράεδρο (η φωτιά), ο κύβος (η γη), το οκτάεδρο (ο αέρας), το δωδεκάεδρο (ο αιθέρας) και το εικοσάεδρο (το νερό).
Ο Αριστοτέλης δέχεται ότι η παθητική ύλη συνδυάζεται με την ενεργητική αρχή, την εντελέχεια (ετυμολογία: εν + τέλος + έχω, η ενυπάρχουσα σε κάθε ον τάση για τελειότητα) ή ψυχή, που τη διαμορφώνει και της δίνει κίνηση. Με την αναντίρρητη εξουσία του στις φυσικές επιστήμες, οι γνώμες του επηρέασαν τη μελλοντική ιστορία των φυσικών επιστημών. Οι θεωρίες του αποτέλεσαν το υπόβαθρο της αντίληψης του κόσμου από τους θρησκευτικούς καθοδηγητές της Χριστιανικής εκκλησίας και ιδιαίτερα του Αγίου Αυγουστίνου. Η φιλοσοφική σκέψη μπορούσε να διατηρηθεί κάτω από τον μανδύα των δογματικών θρησκευτικών αντιλήψεων και η φύση γίνονταν κατανοητή όχι με την παρατήρηση και το πείραμα, αλλά από τα αναγραφόμενα στα θρησκευτικά βιβλία.

Ο προσωκρατικός φιλόσοφος Ζήνων ο Ελεάτης δείχνει στους μαθητές του τις πόρτες της αλήθειας (veritas) και του ψεύδους (falsitas). Τοιχογραφία στη Βιβλιοθήκη El Escorial της Μαδρίτης.
Πηγές από το Διαδίκτυο: (1) "The History of Ancient Chemistry" (Lois Fruen, www.realscience.breckschool.org). (2) "Atoms and Atheism - the changing ways that Christians have viewed the nature of matter".
5. Η Χημεία κατά την Περίοδο των Ρωμαίων


(α) Τίτος Λουκρήτιος Κάρος (98-55 π.Χ.). (β) Εξώφυλλο του 1ου τόμου του έργου του De Rerum Natura (έκδοση 1656).
Η συνεισφορά των Ρωμαίων στη Χημεία ήταν μάλλον περιορισμένη, αφού κυρίως ενδιαφέρονταν κυρίως για τις πρακτικές εφαρμογές των τεχνικών που ήδη γνωστές. Οι Ρωμαίοι φιλόσοφοι που συνέβαλαν κυρίως σε θέματα φυσικής και χημείας ήταν ο Λουκρήτιος και ο Πλίνιος.
Ο Τίτος Λουκρήτιος Κάρος (Titus Lucretius Carus, 98 π.Χ.- 55 π.Χ.) ήταν Ρωμαίος ποιητής και φιλόσοφος. Διατύπωσε τα διδάγματα της επικούρειας φιλοσοφίας σε ένα μνημειώδες ποίημα 7.415 στίχων στη λατινική γλώσσα, το De Rerum Natura ("Περί της Φύσεως των πραγμάτων"), το μόνο γνωστό του έργο. Ο Λουκρήτιος διαδραμάτισε σημαντικό ρόλο στη μετάδοση των ελληνικών φιλοσοφικών ιδεών και ιδιαίτερα των ατομικών θεωριών του Επίκουρου και κατ' επέκταση των υλιστικών θεωριών του Δημοκρίτου.
Ο Λουκρήτιος είχε εξαιρετικά ορθολογικές φιλοσοφικές αντιλήψεις για μια εποχή που κυριαρχούσαν μεταφυσικές ιδέες και δεισιδαιμονίες. Ο στόχος του έργου ήταν να απαλλάξει το νου των ανθρώπων από την προκατάληψη και το φόβο του θανάτου.
Ανέπτυξε διεξοδικά τις θέσεις του Επίκουρου, τον οποίον και αποθεώνει. Ο Λουκρήτιος εκφράζει τις επικούρειες απόψεις του για τη μεταφυσική, την υλιστική ατομική θεωρία και, γενικότερα, την υπεροχή των φυσικών φαινομένων ως κεντρικής ερμηνείας της λειτουργίας του κόσμου.
Ο Λουκρήτιος αντιπαθούσε και έβλεπε ως αβάσιμο κάθε είδος δεισιδαιμονίας, καθώς δεν πίστευε ότι το Σύμπαν κυβερνάται από θεϊκές παρεμβάσεις ή υπερφυσικές δυνάμεις.
Ο Πλίνιος ο Πρεσβύτερος (Pliny the Elder, 23-79 μ.Χ.), στο έργο του Φυσική Ιστορία (Naturalis Historiae, 77-79 μ.Χ.), διακρίνει τα φυσικά από τα χημικά φαινόμενα και επίσης εξετάζει θέματα ζωολογίας, βοτανικής, μεταλλουργίας και ορυκτών. Η "Φυσική Ιστορία" (31 βιβλία), είναι ένα πλήρες εγκυκλοπαιδικό σύγγραμμα φιλοσοφίας (ιδιαιτέρως φυσικής φιλοσοφίας), στο οποίο συνοψίζεται όλη η γνώση της εποχής του, ανθολογημένη από διάσπαρτα προγενέστερα ελληνικά και λατινικά συγγράμματα, στους τομείς της μεταφυσικής, της αστρονομίας, των μαθηματικών, της γεωγραφίας, της εθνογραφίας, της ανθρωπολογίας, της ζωολογίας, της βοτανολογίας, της φαρμακολογίας, της ηφαιστειολογίας, της ορυκτολογίας κ.α.



(α) Πλίνιος ο Πρεσβύτερος (23-79 μ.Χ.) (β) Εξώφυλλο του 1ου τόμου της Φυσικής Ιστορίας του Πλίνιου (έκδοση 1669). (γ) Το κιννάβαρι (HgS) οι Ρωμαίοι το εξόρυσσαν από τα ορυχεία του Almaden στην Ισπανία. Για την εξόρυξη του πολύτιμου αυτού ορυκτού αυτού χρησιμοποιούσαν μόνο κατάδικους, αφού η εργασία στα ορυχεία αυτά ισοδυναμούσε με καταδίκη σε θάνατο, λόγω της μεγάλης περιεκτικότητας της ατμόσφαιρας του ορυχείου σε ατμούς υδραργύρου. Ο Πλίνιος ήταν από τους πρώτους που αναγνώρισαν την τοξικότητα αυτού του πολύτιμου ορυκτού (το χρησιμοποιούσαν ως κόκκινη βαφή), αλλά και γενικότερα της επικινδυνότητας κάθε εργασίας με τον υδράργυρο.
Στην περιγραφή των φυτών, ο Πλίνιος μπόρεσε να συλλέξει αρκετές πληροφορίες για θεραπείες με βότανα. Στο τέλος του έργου, ως ο μοναδικός Ρωμαίος μετά τον Λουκρήτιο, που είχε για θέμα του ολόκληρο το βασίλειο της Φύσης, προσεύχεται για τις ευλογίες της παγκόσμιας μητέρας στο ολοκληρωμένο έργο του. Κατά τους αιώνες που ακολούθησαν η "Φυσική Ιστορία" χρησιμοποιήθηκε από αναρίθμητους σοφούς ως έγκυρη πηγή τόσο σε θέματα φυσικής φιλοσοφίας, όσο και ιατρικής.
Ο Πλίνιος έκανε αρκετές αναφορές σε μέταλλα και στην κατεργασία τους. Σε αυτά περιλαμβάνονται ο χρυσός, ο άργυρος, ο σίδηρος, ο μόλυβδος, ο κασσίτερος, ο υδράργυρος και το αντιμόνιο. Αναγνώρισε τις τοξικές ιδιότητες του υδραργύρου, όπως και τις διαφορές στις ιδιότητες μεταξύ του κοινών μορφών σιδήρου και του χάλυβα.
Σημαντική υπήρξε και η συνεισφορά του Πλίνιου στον τομέα των ορυκτών και των ιδιοτήτων διαφόρων μεταλλευμάτων. Μεταξύ πολλών άλλων συνεισφορών του σε θέματα χημείας και μεταλλουργίας, εισήγαγε μέθοδο διάκρισης της καθαρότητας πολύτιμων μετάλλων, όπως και ένα σύστημα χαρακτηρισμού της σκληρότητας των ορυκτών, ένα "πρώιμο" σύστημα της σημερινής κλίμακας σκληρότητας Mohs.
Ο θάνατος του Πλίνιου κατά πάσα πιθανότητα οφείλεται στην επιθυμία του να παρατηρήσει για όσο το δυνατόν μεγαλύτερο χρονικό διάστημα την έκρηξη του ηφαιστείου Βεζούβιου, που κατέστρεψε το 79 μ.Χ. την Πομπηία και το επίνειό της το Ερκουλάνουμ.
6. Η Χημεία στην Αρχαία Ινδία και τα Ιερά Κείμενα Vedas
Στην αρχαία Ινδία αναπτύχθηκε μεγάλος αριθμός χημικών διεργασιών και τεχνικών. Οι Ινδοί πειραματίσθηκαν με πλήθος διάφορων υλικών, ιδιαίτερα με φάρμακα από φυτικά εκχυλίσματα και έκαναν χρήσιμες παρατηρήσεις για τη φύση και τις ιδιότητες χημικών ουσιών για ιατρικούς σκοπούς. Οι γνώσεις αυτές αξιοποιήθηκαν αργότερα κατά την ονομαζόμενη Χρυσή Ισλαμική Περίοδο (Islamic Golden Age), δηλ. κατά την περίοδο 750-1250 μ.Χ., από τους Μουσουλμάνους, οι οποίοι βελτίωσαν πολλές ινδικής προέλευσης τεχνικές μεταλλουργίας, παρασκευής αρωμάτων και χρήσης βοτάνων και καρυκευμάτων.
Οι Ινδοί κατείχαν γνώσεις πυρομεταλλουργίας και της κατεργασίας μεταλλικών αντικειμένων από ορείχαλκο, ίσως και από το 2.300 π.Χ και αργότερα, από το 1500 π.Χ., αντικειμένων από σίδηρο. Από την πρώτη χιλιετία π.Χ., οι Ινδοί είχαν γίνει ειδικοί στην κατεργασία και παρασκευή υψηλής ποιότητας χάλυβα, ο οποίος ήταν πολυτιμότερος και από τον ίδιο τον χρυσό σε ορισμένες περιοχές της Ευρώπης και της Μέσης Ανατολής. Μόλις τον 17ο αιώνα μ.Χ., οι Ευρωπαίοι μελέτησαν τον τύπο αυτό χάλυβα που τους επέτρεψε να τυποποιήσουν και να βελτιώσουν τις δικές τους διεργασίες παρασκευής χάλυβα, γεγονός που είχε ως άμεσο αποτέλεσμα την ονομαζόμενη Βιομηχανική Επανάσταση, η οποία ως βάση είχε τη χρήση χάλυβα για την κατασκευή εργαλείων, μηχανών, γεφυρών, κ.λπ.
Εκτός όμως από τη συμβολή των Ινδών στη χημεία των μετάλλων και της κατεργασίας τους, οι αλχημιστές τους (η ινδική αλχημεία είναι γνωστή ως Rasa Shastra, που στην κυριολεξία σημαίνει "η επιστήμη του υδραργύρου") ήταν διάσημοι για τα επιτεύγματά τους. 'Ηταν γνωστοί για την ποικιλία χρωστικών υλών που χρησιμοποιούσαν, την υαλουργία, την παρασκευή ενός είδους τσιμέντου, τη χημική κατεργασία δέρματος και την παρασκευή σαπουνιού.
Κατά τον 5ο - 7ο αιώνα μ.Χ., όταν η δυτική και βόρεια Ευρώπη ζούσε τις Σκοτεινές Περιόδους της ιστορίας της (Dark Ages), οι Ινδοί είχαν ήδη αναπτύξει ένα εκπληκτικό τεχνολογικό πολιτισμό και έκαναν χρήση πολλών χημικών τεχνικών. Περιγραφές των τεχνικών αυτών βρίσκονται στις Βέδες (Vedas, ~300 π.Χ., veda: γνώση, στα σανσκριτικά), που είναι αρχικά κείμενα Ινδουϊσμού και τα οποία είχαν μεγάλη επιρροή στον Βουδισμό και άλλες θρησκείες. Στις Βέδες βρίσκονται ύμνοι, μαγικές συνταγές και περιγράφονται τελετουργικές καταστάσεις από την Αρχαία Ινδία. Οι Βέδες συγκαταλέγονται μεταξύ των αρχαιότερων θρησκευτικών κειμένων και εκτός της πνευματικής τους αξίας είναι πλούσιες πηγές πληροφοριών για την καθημερινή ζωή των αρχαίων Ινδών.




O περίφημος σιδερένιος στύλος (iron pillar) του Delhi, ύψους 7 μ. και βάρους 7 τόνων. Κατασκευασμένος κατά τον 4ο αιώνα μ.Χ. και εκτεθειμένος στα καιρικά στοιχεία επί 1600 και πλέον χρόνια, παραμένει ανοξείδωτος. Τυπική απόδειξη των μεταλλουργικών γνώσεων των αρχαίων Ινδών.
Εικόνες αρχαίων κειμένων από τις Βέδες.
Τυπικά προϊόντα (φυσικές βαφές, φυτικά δηλητήρια), της Ινδικής Αλχημείας (Rasa Shastra).

Σκεύη Ινδών Αλχημιστών (σχέδια από ινδικά αλχημιστικά κείμενα)
Πηγές από το Διαδίκτυο: (1) "Indian Alchemy" (The Alchemy Web Site). (2) "Indian Alchemy" (indianalchemy.com)
7. Ιστορία της Χημείας και Κινέζικος Πολιτισμός

Αριστερά: Χρονολογίες στην Κινέζικη Αλχημεία. Δεξιά: Ο Wei Po Yang, "πατέρας" της Κινέζικης αλχημείας.
Οι Ευρωπαίοι για πολλές δεκαετίες αγνοούσαν τη συνεισφορά του Κινέζικου πολιτισμού σε θέματα επιστήμης, αλχημείας και το γεγονός ότι στην Κίνα είχαν παρασκευασθεί χημικά υλικά πολύ πριν ακόμη ανακαλυφθούν στην Δύση.
'Οπως οι αλχημιστές στη Δύση έτσι και στην Κίνα οι αλχημιστές από αρχαιοτάτων χρόνων επεξεργάζονταν μέταλλα και χρησιμοποιούσαν βότανα, αρώματα και φυτικά σκευάσματα για ιατρικούς σκοπούς. Η Κινέζικη αλχημεία ήταν ένα μίγμα πρακτικών εφαρμογών και Ταοϊστικών δοξασιών για τις ιδέες της ισορροπίας και της αρμονίας. Επίσης, πολλές κινεζικές αλχημιστικές πρακτικές σχετίζονταν με την ολιστική προσέγγιση της παραδοσιακής Κινέζικης ιατρικής για την υγεία του ανθρώπου, σύμφωνα με την οποία ακόμη και ορυκτά και ανόργανα υλικά μπορούν να συμβάλλουν σε θεραπευτικές τεχνικές.
Υπάρχουν ιστορικές ενδείξεις ότι οι Κινέζοι ενδιαφέρονταν για την αλχημεία από τον 4ο αιώνα π.Χ. 'Ηδη από το 175 π.Χ. είχε εκδοθεί επίσημο διάταγμα που προειδοποιούσε τους αλχημιστές να μην κατασκευάζουν κίβδηλα χρυσά νομίσματα, πράξη που θα επέσυρε τη θανατική τους καταδίκη.
'Οπως και στις άλλες περιοχές του πλανήτη, ο χρυσός και η μετατροπή άλλων ευτελών μετάλλων σε χρυσό ήταν ένας από τους κύριους στόχους πολλών Κινέζων αλχημιστών. Υπάρχουν αναφορές για έναν αλχημιστή, ονομαζόμενο Zou Yan (305 - 240 π.Χ.), που υπόσχονταν σε πλούσιους Κινέζους και άρχοντες πρόσθετα πλούτη, δύναμη και τιμές, όπως και την ικανότητα επίκλησης υπερφυσικών δυνάμεων για να πετύχουν οι ηγεμονικές τους επιδιώξεις.

Ο μετασχηματισμός φθηνών μετάλλων σε χρυσό υπήρξε ένας από τους κύριους στόχους των αλχημιστών όλου του κόσμου. Ποτέ δεν μπόρεσε η Χημεία μόνη της να το πετύχει, ωστόσο η επιδίωξη αυτή προσέφερε πολλές νέες γνώσεις.
'Ενας άλλος αλχημιστής παρουσιάσθηκε το 133 π.Χ. στο βασιλικό παλάτι υποσχόμενος το ελιξίριο της αθανασίας. Η ιδέα της παράτασης της ζωής και της αθανασίας είχε γίνει το κεντρικό σημείο δράσης πολλών Κινέζων αλχημιστών, κατά τρόπον αντίστοιχο της ιδέας της Φιλοσοφικής Λίθου (Philosopher's Stone) των αλχημιστών στη Δύση. Ιστορικά ντοκουμέντα δείχνουν ότι το 60 π.Χ. ο αυτοκράτορας Suan ανέθεσε σε έναν αλχημιστή, με το όνομα Liu Tsiang, να χρησιμοποιήσει τις δυνάμεις του για να αυξήσει τα χρόνια ζωής του με την παρασκευή αλχημιστικού χρυσού. Αν και απέτυχε να πραγματοποιήσει τις υποσχέσεις του, μόλις απέφυγε την εκτέλεση.
Το αρχαιότερο κινεζικό αλχημιστικό κείμενο πάνω γράφτηκε από τον Wei Po Yang (140 μ.Χ.). Σε αυτό γίνεται αναφορά στις αντίθετες, πλην όμως συμπληρωματικές δυνάμεις Yin και Yang. Η Κινέζικη αλχημεία δανείστηκε πολλές ιδέες από τον παραδοσιακή ιατρική που στηρίζονταν στις βασικές αρχές του Ταοϊσμού. Η φιλοσοφία αυτή στηρίζονταν στην αντίληψη των αντίθετων δυνάμεων, το Yin και Yang, που τα θεωρούσαν ενεργά στοιχεία (Yin = αρσενικό - ενεργό, Yang = θηλυκό - παθητικό).

Πανάρχαιο φιλοσοφικό σύμβολο αρμονίας και Yin Yang
Το Yin Yang είναι ένα πανάρχαιο σύμβολο. Εμφανίστηκε για πρώτη φορά σε κινέζικα ιστορικά έγγραφα ηλικίας περίπου 3000 χρόνων. H αυθεντική ονομασία του συμβόλου αυτού, που όλοι οι άνθρωποι είναι οικείοι μαζί του με την ονομασία Yin Yang, είναι Tai Chi Tu.
Στο Yin Yang o κύκλος συμβολίζει την ολότητα και το άπειρο του Chi (ζωτική ενέργεια). Δεν υπάρχει ούτε αρχή ούτε τέλος, διαπερνά μέσα από την ολότητα. Ο εξωτερικός αυτός κύκλος είναι το Σύμπαν που εμπεριέχει το Yang (φως) και το Yin (σκοτάδι). Η διαχωριστική γραμμή ανάμεσα σε αυτούς τους δύο κυκλικούς τομείς είναι καμπυλοειδής. Αυτό δηλώνει μια αέναη κίνηση και ροή του Yin μέσα στο Yang και αντίστροφα. H αναλογία των χρωμάτων είναι ίδια, επομένως τα δύο στοιχεία εξισορροπούν μεταξύ τους.
Οι Κινέζοι αλχημιστές έγραψαν αρκετά έργα Αλχημείας (Ko-Huang, 254-334 μ.Χ.), με περιγραφές χημικών διεργασιών που αφορούσαν την παρασκευή διάφορων υλικών, ελιξίριων ζωής, τον "μετασχηματισμό" μετάλλων και την περιγραφή βοτάνων με μαγικές θεραπευτικές ιδιότητες. Γνώριζαν το κιννάβαρι (HgS), τις θειούχες ενώσεις του αρσενικού (ερυθρά σανδαράχη, As2S2, και κίτρινη σανδαράχη, As2S3), την κιμωλία, χρωστικές από τα όστρακα των μυδιών (πορφύρα), το θείο, την πυρίτιδα, την άσφαλτο και πλήθος αλάτων. Επίσης περιγράφουν διάφορες τεχνικές μετασχηματισμού ευτελών μετάλλων σε χρυσό. Σε όλες αυτές τις διαδικασίες χρησιμοποιούσαν τεχνικές απόσταξης, σύντηξης και εξάχνωσης.
Ο αριθμός πέντε φαίνεται πως υπήρξε ο ιερός αριθμός της κινεζικής αλχημείας. Οι Κινέζοι αλχημιστές υποστήριζαν την ύπαρξη πέντε στοιχείων: ξύλο, πυρ, γη, μέταλλο και νερό και τα συνδυάζανε με πέντε χρώματα. Επίσης είχαν πέντε κατευθύνσεις (πορείες) που τα συνέδεαν με πέντε μέταλλα: χρυσός, άργυρος, μόλυβδο, χαλκό και σίδηρο. Ως αποτέλεσμα, κάθε αλχημιστική τεχνική διακρινόταν σε πέντε στάδια.



Χρήση νερόμυλου για τη διαβίβαση αέρα σε υψικάμινο χάλυβα
Παρασκευή χάλυβα, στάδιο απομάκρυνσης σκωρίας
Μεταλλικά κινεζικά σπαθιά (τα περισσότερα από σίδηρο)
Πηγές από το Διαδίκτυο: (1) "Ancient Chinese Alchemy" (Experiment-Resorces.com). (2) "Chemistry in Ancient China: Alchemy" (Hu Zhang)



Geber (Jaber Ibn Hayan, 721(;)-815, Βαγδάτη)
Αβικένας (Ibn Sina Avicenna,
980 -1037, Περσία)
Αβερρόης (Ibn Rushd Averroes, 1126 Cordova Ισπανίας - 1198, Marrakes)
8. Ιστορία της Χημείας στις Αραβικές Χώρες και Αλχημεία
Οι 'Αραβες χρησιμοποίησαν με επιτυχία πρώτοι τις διάφορες ανακαλύψεις, που παρέλαβαν από τους Ινδούς, τους Κινέζους και τους Αιγύπτιους (πυρίτιδα, πυξίδα, χαρτί, άρδευση χωραφιών, αρώματα, χρωστικές ύλες, καλλιέργεια δένδρων) και τα μετέφεραν στην Ευρώπη, όταν κατέλαβαν την Ισπανία. Οι 'Αραβες δεν μετέφεραν απλώς γνώσεις από την Ανατολή, αλλά συνέβαλαν ουσιαστικά στη Χημεία, όπως και σε άλλες θετικές επιστήμες, μια εποχή (μεσαίωνας 700-1400 μ.Χ.), που στην Ευρώπη κυριαρχούσαν η δεισιδαιμονία και οι θρησκευτικές προκαταλήψεις.
Αραβική ανακάλυψη είναι ένα πλήθος χημικών αντιδραστηρίων, που στη συνέχεια χρησιμοποίησαν οι Ευρωπαίοι αλχημιστές, όπως το νιτρικό και το θειικό οξύ και η ποτάσα (potash, K2CO3). Επίσης, τελειοποίησαν πολλές τεχνικές, όπως την υφαντουργία, τη μεταλλουργία, την παρασκευή χρωστικών υλών, την αγγειοπλαστική, την υαλουργία και την αρωματοποιία. Ονομαστά αραβικά προϊόντα ήταν τα λινά υφάσματα, οι μουσελίνες της Μοσούλης και τα περίφημα ξίφη της Δαμασκού, για τα οποία η μεταλλουργική τεχνική κατασκευής τους παραμένει ακόμη ένα επιστημονικό αίνιγμα.
Επίσης, οι 'Αραβες ανακάλυψαν σπουδαίες θεωρίες και τεχνικές για την ιατρική, τη γεωμετρία, την αστρονομία. Επινόησαν την άλγεβρα (al-jabr: επανόρθωση, αποκατάσταση), μελέτησαν το εκκρεμές και εισήγαγαν τα ψηφία-σύμβολα του δεκαδικού συστήματος αρίθμησης (αραβικά ψηφία). Τέλος, συνέβαλαν στην ανάπτυξη της οπτικής και της τριγωνομετρίας και βέβαια της αλχημείας.
Μέχρι την περίοδο των Αράβων, η αλχημεία ήταν ένα μίγμα φιλοσοφικών θεωριών, αλληγοριών, συμβόλων και κωδικοποιημένων γλωσσών. Κατά την περίοδο των Αράβων (από τον 8ο αιώνα μ.Χ. και μετά), η αλχημεία άρχισε να γίνεται μια συστηματική τεχνική με συγκεκριμένες πρακτικές πλευρές.

Τα περίφημα χαλύβδινα "Δαμασκηνά σπαθιά" (Damascus' swords), με τα χαρακτηριστικά μοτίβα τους, υπήρξαν διάσημα για την αντοχή τους και την εξαιρετικά αιχμηρή λεπίδα τους. Η παράδοση λέει ότι μπορούσαν με ένα κτύπημα να κόψουν τα ευρωπαϊκής κατασκευής σπαθιά, όπως και βράχους. Η κατασκευή τους (1100-1700 μ.Χ.) παραμένει ένα μυστήριο παρά το πλήθος των σχετικών ερευνών.
Ο 'Αραβας Τζαμπίρ Ιμπν Χαγιάν (Jaber Ibn Hayan, 721(;)-815, Βαγδάτη), μετέπειτα γνωστός στην Ευρώπη ως Geber, γνωστός και ως ο πρώτος των αλχημιστών, εισήγαγε τη μεθοδική και πειραματική προσέγγιση μιας αλχημιστικής επιστημονικής έρευνας που πραγματοποιούνταν σε ένα εργαστήριο. Ο Geber θεωρείται ως ο πατέρας της Αλχημείας. Ο Geber θεωρούσε ότι όλα τα μέταλλα αποτελούνταν από υδράργυρο και θείο και ότι ο υδράργυρος καθόριζε τη μεταλλικότητά τους και το θείο την αναφλεξιμότητά τους.
Οι ανακαλύψεις του Geber υπήρξαν πολύ σημαντικές και καταγράφηκαν στα πολυάριθμα βιβλία και σημειώσεις που άφησε. Μεταξύ άλλων, ανακάλυψε την ποτάσα, περιέγραψε μέθοδο απομόνωσης του καυστικού νατρίου, όπως και των ισχυρών οξέων, δηλ. του θειικού, του νιτρικού και του υδροχλωρικού οξέος. Στον Geber αποδίδεται η απομόνωση του αρσενικού και του αντιμονίου. Βελτίωσε τις τεχνικές κρυστάλλωσης, απόσταξης, σύντηξης, εξάχνωσης και εξάτμισης. Επίσης, εφηύρε ένα είδος άκαυστου χαρτιού, βρήκε ένα τρόπο προστασίας του σιδήρου από την οξείδωση, όπως ένα τρόπο διαχωρισμού του χρυσού από τον άργυρο με τη βοήθεια οξέων.
Πιστεύεται ότι ο Geber έγραψε πάνω από 200 βιβλία, τα οποία για αιώνες υπήρξαν για τους Ευρωπαίους αλχημιστές πηγές ανεκτίμητων πληροφοριών για διάφορες χημικές ουσίες.
O διάσημος 'Αγγλος φιλόσοφος και αλχημιστής Roger Bacon (1214-1294) τον αναγνώρισε ως τον πρωτοπόρο δάσκαλο της επιστήμης της Χημείας, ενώ, πολύ αργότερα, ο Γάλλος χημικός Marcellin Berthelot (1827-1907) είπε ότι ο Αριστοτέλης καθιέρωσε τη φιλοσοφία της λογικής και ο Geber τη Χημεία.
Ονομαστοί 'Αραβες φιλόσοφοι και ιατροί ήταν ο Αβικένας (Ibn Sina Avicenna, 980 -1037, Περσία) και ο Αβερρόης (Ibn Rushd Averroes, 1126 Cordova Ισπανίας - 1198 Marrakes, Μαρόκο). O Αβικένας είχε συντάξει ένα μεγάλο κατάλογο των μέχρι τότε γνωστών ουσιών, όπου περιέγραφε και τη φαρμακολογική δράση τους. Ο Αβερρόης έγραψε μια ιατρική εγκυκλοπαίδεια και σχεδόν για όλα τα έργα του Αριστοτέλη. Πρέπει να σημειωθεί ότι οι 'Αραβες θεωρούσαν τον Αριστοτέλη μεγάλο φιλόσοφο, τα έργα του οποίου διασώθηκαν και έγιναν γνωστά στην Ευρώπη από αραβικές μεταφράσεις και σχολιασμούς.
Αυτοί οι 'Αραβες σοφοί θεωρούνται ότι ήταν οι πρώτοι που ασχολήθηκαν συστηματικά με τη Χημεία και τις χημικές τεχνικές και συνέβαλαν αποφασιστικά στην πρόοδο της επιστήμης της Χημείας. Διέσωσαν τις αρχαίες γνώσεις αλχημείας και τις εμπλούτισαν. Ωστόσο, δεν υπήρξαν αποκλειστικά αλχημιστές. Αυτοί οι άνθρωποι ήταν στην κυριολεξία "πανεπιστήμονες", ήταν φιλόσοφοι και συγχρόνως γιατροί, θεολόγοι και συγχρόνως φυσικοί και μαθηματικοί, ποιητές και συγχρόνως μηχανικοί. 'Ηταν ένα σπάνιο είδος ανθρώπων, που συνέβαλαν αποφασιστικά στην πρόοδο της ανθρωπότητας.
Σελίδες από αραβικά αλχημιστικά κείμενα



Το πιο γνωστό "χημικό επίτευγμα" των Βυζαντινών χρόνων, σίγουρα είναι το περίφημο "υγρό πυρ" (greek fire). Η σύνθεση του ήταν επτασφράγιστο μυστικό και μόνο εικασίες ως προς αυτήν μπορούν σήμερα να γίνουν. Δεν φαίνεται πάντως να ήταν ένα απλό καύσιμο μίγμα νάφθας και θείου. Υπάρχουν μαρτυρίες που αναφέρουν την αυτανάφλεξή του όταν ερχόταν σε επαφή με το νερό. 'Ετσι, διατυπώθηκε η υπόθεση ότι ένα δραστικό συστατικό του θα πρέπει να ήταν το φωσφίδιο του ασβεστίου (Ca3P2). Το φωσφίδιο αυτό σε επαφή με το νερό υδρολύεται παρέχοντας το αέριο φωσφίνη (PH3). Η φωσφίνη αυταναφλέγεται στον αέρα προκαλώντας ανάφλεξη και στα υπόλοιπα καύσιμα υλικά του μίγματος. Τώρα, το πώς θα μπορούσε να παρασκευασθεί το φωσφίδιο (που απαιτεί ισχυρότατα αναγωγικές συνθήκες ή ακόμη και μεταλλικό ασβέστιο για τη σύνθεσή του) παραμένει μυστήριο.

'Αμβυκας: Η τυπική διαχρονική συσκευή απόσταξης σε διάφορες "εκδοχές" (αρχαία ελληνική λέξη: άμβυξ, αραβική παραλλαγή: al ambic ή alambic και ως αντιδάνειο: λαμπίκος ή λαμπίκο).

Αλχημιστής σε αναζήτηση της Φιλοσοφικής Λίθου. Ζωγραφικός πίνακας (1771) του Joseph Wright, όπου απεικονίζεται ο αλχημιστής Hennig Brand (1630-1710)να ανακαλύπτει τον φωσφόρο. Αυτό συνέβη "κατά λάθος", όταν ο Brand αναζητούσε τη Φιλοσοφική Λίθο στο στερεό υπόλειμμα μεγάλης ποσότητας ούρων.
9. Ιστορία της Χημείας κατά την Περίοδο των Αλχημιστών
Η λέξη Αλχημεία, όπως αναφέρθηκε στην εισαγωγή, προέρχεται από το οριστικό αραβικό άρθρο Αλ και τη Χημεία. Λιγότερο πιθανές, αλλά ενδιαφέρουσες είναι άλλες θεωρίες για την προέλευσή της. 'Ετσι, πολλοί πιστεύουν ότι έχει κινεζική προέλευση ή ακόμη και ελληνική (Αριστοτέλης: 'Εστι δε πάσι αρχή μία και ουσία: Αρχή μία Αρχημία
Αρχημία  Αλχημία
Αλχημία  Αλχημεία).
Αλχημεία).
Η ανάπτυξη της Αλχημείας και των αλχημιστών ήταν κάτι το αναμενόμενο κατά τον Μεσαίωνα, αφού οι ειδικές γνώσεις σε θέματα μεταλλουργίας γενικά και χρήσεις των φαρμακευτικών βοτάνων για τη θεραπεία ασθενειών, υπήρξαν πάντοτε σημαντικοί παράγοντες πλουτισμού. Η επιστήμη της Χημείας από αντικείμενο επιστημονικής γνώσης και αναζήτησης μετατράπηκε σε εμπορευματικό προϊόν με μεγάλη ζήτηση και χρηματική αξία.

Το αλχημιστικό σύμβολο της φιλοσοφικής λίθου (σύνθεση άλλων επιμέρους συμβόλων).
Οι αλχημιστές πίστευαν ότι υπάρχουν τέσσερα βασικά στοιχεία-ουσίες: η φωτιά, ο αέρας, η γη και το νερό και τρία αιθέρια στοιχεία: το θειάφι, το αλάτι και ο υδράργυρος. Η Αλχημεία ήταν ιδιαίτερα διαδεδομένη στην μεσαιωνική Ευρώπη. Πολλά από τα αλχημιστικά βιβλία ήταν γεμάτα με ανούσια μαγικά ξόρκια, επικλήσεις και άλλα αποκρυφιστικά στοιχεία.
Οι σημαντικότεροι στόχοι των αλχημιστών ήταν η ουτοπική μετατροπή (μετουσίωση) των κοινών μετάλλων σε χρυσό ή ασήμι, όπως και η δημιουργία του ελιξιρίου της ζωής (από την αρχαία ελληνική λέξη: ξήριον -ουσία που "ξηραίνει" τα τραύματα- και στη συνέχεια την αραβική: el iksir), το οποίο θα θεράπευε όλες τις ασθένειες και θα παρέτεινε τη ζωή του ανθρώπου. Η Φιλοσοφική Λίθος (lapis philosophorum) ήταν μια μυθική ουσία και βασικό συστατικό για την επίτευξη των στόχων αυτών. Για τους αλχημιστές αντιπροσώπευε το πέμπτο στοιχείο ή την πέμπτη ουσία ή την πεμπτουσία (quinta essentia ή quintessence), την ύπαρξη της οποίας δεχόταν ο Αριστοτέλης. Επίσης, οι αλχημιστές αναζητούσαν ένα παγκόσμιο διαλύτη, δηλαδή μια ουσία που θα μπορούσε να διαλύσει κάθε άλλη (azoth, alkahest). 'Ολες αυτές οι ουτοπικές έννοιες και ουσίες συχνότατα συγχέονται μεταξύ τους και σημαίνουν το ίδιο πράγμα και συνδυάζουν όλες τις παραπάνω ιδιότητες.
Οι αλχημιστές δεν επεδίωκαν μόνο τη βελτίωση κάποιων ιδιοτήτων των υλικών ή την παράταση του χρόνου ζωής, αλλά έδιναν και μια πνευματική διάσταση στις αναζητήσεις τους. Για παράδειγμα, η μετατροπή του "ευτελούς" μολύβδου σε "ευγενή" χρυσό, παραλληλιζόταν με την ψυχική ανύψωση και τον εξευγενισμό του πνεύματος.
Τα εργαστήρια των αλχημιστών ήταν γεμάτα με όργανα απόσταξης, φούρνους, φιάλες με χημικές ουσίες, διαλύτες και οξέα και πολλά συγγράμματα χημείας κυρίως Αραβικής προέλευσης. Πολλές υπήρξαν οι "παράπλευρες" χημικές ανακαλύψεις των αλχημιστών κατά τη διάρκεια των παράδοξων αναζητήσεών τους. Τυπικό παράδειγμα αποτελεί η ανακάλυψη του φωσφόρου (1669) από τον Γερμανό αλχημιστή Hennig Brand (1630-1710), όταν θέρμανε σε υψηλή θερμοκρασία το στερεό υπόλειμμα, που συνέλεξε μετά την εξάτμιση μιας μεγάλης ποσότητας ούρων. Προφανώς, στην υψηλή θερμοκρασία του φούρνου πραγματοποιήθηκε αναγωγή των φωσφορικών αλάτων από τον άνθρακα των οργανικών ουσιών του υπολείμματος. 'Οταν διαπίστωσε αυτή η κηρώδης ουσία καιγόταν με έντονο λαμπρό φως και κυρίως ότι από μόνη της λαμποκοπούσε στο σκοτάδι, την ονόμασε phosphorus mirabilis (θαυμαστή ουσία που φέρει φώς).
Οι αλχημιστές συνήθιζαν να κρατούν ως επτασφράγιστα μυστικά τις λεπτομέρειες των τεχνικών τους και να κρατούν σημειώσεις με "κρυπτογραφικά" σύμβολα. Αυτό είχε ως αποτέλεσμα να ταυτιστούν με μυστικιστικές ομάδες και συντεχνίες με "ύποπτους σκοπούς". Αλλά και οι ίδιοι οι αλχημιστές, τις περισσότερες φορές σκόπιμα και για λόγους εντυπωσιασμού και βιοπορισμού, δεν επεδίωξαν να διαχωρίσουν την "τέχνη" τους από το υπερφυσικό, το μαγικό και τη δεισιδαιμονία.
Οι αλχημιστές υπέστησαν πολλούς διωγμούς ανά τους αιώνες (συχνότατα δικαιολογημένους) και η εξάσκηση της αλχημιστικής τέχνης πολλές φορές απαγορεύτηκε από θεσμικά πρόσωπα όπως ο Πάπας Ιωάννης XXII (1317) ή ο Ερρίκος ο IV της Αγγλίας (1403).



Αριστερά-μέσον: Δύο από τις άφθονες ζωγραφικές απεικονίσεις αλχημιστών και των εργαστηρίων. Δεξιά: Ο δρόμος των αλχημιστών ή ο δρόμος του χρυσού (Zlata Ulicka, Golden Lane). Ένας στενός δρόμος με μικρά σπιτάκια-εργαστήρια χρυσοχόων, που βρίσκονται μέσα στο κάστρο της Πράγας. Ο θρύλος λέει ότι εκεί ζούσαν και αλχημιστές (στην πραγματικότητα αυτοί βρίσκονταν σε άλλα μέρη του κάστρου). Οι ηγεμόνες της Βοημίας (σημερινής Τσεχίας) κρατούσαν χρυσοχόους και αλχημιστές σε μια κατάσταση ημιαιχμαλωσίας και συνεχούς επιτήρησης.
Οι αλχημιστές αποτυπώνονταν σε έργα ζωγραφικής ή περιγράφονταν σε κείμενα ως άνθρωποι αναξιόπιστοι. Δεν ήταν λίγες οι φορές που Ευρωπαίοι ηγεμόνες πλήρωναν αδρά αλχημιστές για να τους εξασφαλίσουν "φθηνό" χρυσό ή ελιξίρια μακροζωίας. Δεν ήταν ακόμη λίγες οι φορές που αλχημιστές-απατεώνες ζητούσαν ποσότητες γνήσιου χρυσού από τους ηγεμόνες αυτούς για να τον χρησιμοποιήσουν ως "προζύμι" στα πειράματά τους και τελικά εξαφανίζονταν με τον χρυσό αυτό.
Μετά τις σημαντικές επιστημονικές ανακαλύψεις της Χημείας από τον 18ο αιώνα και μετά, η μεταστοιχείωση με καθαρά χημικά μέσα έχει αποκλεισθεί οριστικά, όπως και η ύπαρξη της φιλοσοφικής λίθου. Ωστόσο, ακόμη και σήμερα γίνεται μερική χρήση αλχημιστικών θεωριών, σε θεραπευτικές πρακτικές όπως είναι η ομοιοπαθητική, η αρωματοθεραπεία και η κρυσταλλοθεραπεία.




Roger Bacon (1214-1294), 'Αγγλος
Albertus Magnus (1193/1206-1280), Βαυαρός
Nicolas Flamel (1330-1418), Γάλλος
Paracelsus (1493-1541), Ελβετός
Μεταξύ των πιο διάσημων αλχημιστές όλων των εποχών (πέραν από τους προαναφερθέντες Geber, Αβικένα και Αβερρόη) θεωρούνται οι: Wei Boyang (Κίνα), που έκανε την πρώτη γραπτή αναφορά για την πυρίτιδα (142 μ.Χ.), ο Ζώσιμος ο Πανοπολίτης ('Ελληνας ή Αιγύπτιος, 4ος-5ος αιώνας μ.Χ.), ο Muhammad ibn Zakariya al-Razi (Περσία, 865-925 μ.Χ.), διάσημος φαρμακοποιός και γιατρός της εποχής του, ο Nagarjuna (Ινδία, 10ος αιώνας μ.Χ.), διάσημος μεταλλουργός (συνέγραψε διατριβή για τον υδράργυρο).
Διάσημοι δυτικοευρωπαίοι αλχημιστές ήταν ο Βαυαρός Albertus Magnus, (1193/1206-1280), ο 'Αγγλος Roger Bacon (1214-1294) γνωστός και ως "Doctor Mirabilis" (: ο θαυμάσιος δάσκαλος), ο Γάλλος Nicolas Flamel (1330-1418) και ο Ελβετός Θεόφραστος Παράκελσος (Theophrastus Bombastus von Hohenheim, 1493-1541).
Ο Παράκελσος θεωρείται ένας από τους μεγαλύτερους αλχημιστές, αστρολόγους, και αποκρυφιστές όλων των εποχών. Ωστόσο, ήταν και από τους πρώτους αλχημιστές που πίστεψε ότι η αναζήτηση της φιλοσοφικής λίθου για την παρασκευή χρυσού ήταν ματαιοπονία και ότι οι αλχημιστές θα έπρεπε να στρέψουν την έρευνά τους στην αναζήτηση φαρμάκων. Ήταν ο πρώτος ο οποίος δίδαξε ότι η ζωή η ίδια δεν είναι παρά μια σειρά χημικών διεργασιών και ότι κάθε αρρώστια στην ουσία είναι μια χημική δυσλειτουργία.
Θεωρείται ως ο "πατέρας" της τοξικολογίας και είχε διατυπώσει την περίφημη φράση "η δόση κάνει το δηλητήριο" (dosis facit venemum). Το 1536, εξέδωσε το Die grosse Wundartzney (το μεγάλο βιβλίο της Χειρουργικής). Ως σημαντικότερο έργο του θεωρείται το Philosofia sagax (υπάρχει και με τον τίτλο Astronomia magna, που είναι γραμμένο στα γερμανικά).
Μετά το θάνατό του Παράκελσου, το επιστημονικό έργο του άρχισε να αναγνωρίζεται και να εκτιμάται από πολλούς ιατρούς της Γερμανίας και της Γαλλίας, οι οποίοι του προσέδωσαν την προσωνυμία του "Λούθηρου της Ιατρικής". Αντίθετα οι εχθροί του, που δημιούργησε αρνούμενος να δεχθεί τις αντιλήψεις των ιατρών της εποχής του, τον αποκαλούσαν "φιλόσοφον ά-λογον" (χωρίς λογική) και τα δε ιατρικά του συγγράμματα ως προϊόντα διανοητικής ανισορροπίας.
Πηγές από το Διαδίκτυο: (1) "Alchemy" (Wikipedia). (2) "The Alchemy web site on Levity.com".







Οι θεμελιωτές της σύγχρονης Χημείας: Robert Boyle (1627-1691) και
Antoine Lavoisier (1743-1794)
10. Η Χημεία κατά τον 17ο και 18ο Αιώνα
Η ιστορία της Χημείας με τους αλχημιστές είχε φτάσει στα όρια μιας ψευδο-επιστήμης με πολλές δεισιδαιμονίες, παρανοήσεις και τυφλά πειράματα για χημικές μετατροπές που δεν έδιναν αποτελέσματα ή έδιναν, αλλά δεν ήταν τα επιζητούμενα και συχνά αγνοούνταν. Οι πρωτοπόροι και "πατέρες" της πραγματικής επιστήμης της Χημείας, με πραγματικά πειράματα, παρατήρηση, λεπτομερή καταγραφή μετρήσεων, αλλά και με έλεγχο της ακρίβειας των μετρήσεων, θεωρούνται ο Robert Boyle (1627-1691) στην Αγγλία και ο Antoine Lavoisier (1743-1794) στη Γαλλία.
Η σύγχρονη λέξη Χημεία εδραιώνεται τον 17ο αιώνα με το έργο του Robert Boyle, που θεωρείται ως ο τελευταίος των αλχημιστών και συγχρόνως ο πρώτος των χημικών, στο βιβλίο που εξέδωσε το 1661 "Ο Σκεπτικιστής Χυμικός" (The Skeptical Chymist), που έγινε βασικό σύγγραμμα-οδηγός για τους χημικούς που ακολούθησαν. Το πλήρες βιβλίο είναι διαθέσιμο στο διαδίκτυο από εδώ (βιβλιοθήκη του Πανεπιστημίου της Πενσυλβάνιας).
Ο Robert Boyle ήταν κατά τον 17ο αιώνα ένας φυσικός φιλόσοφος (όπως αποκαλούνταν οι επιστήμονες την εποχή εκείνη) με γνώσεις φυσικής, χημείας και θεολογίας.
Αν και επικρατούσε σε όλους τους πειραματιστές της εποχής εκείνης μια μηχανοκρατική αντίληψη, ο Robert Boyle προχώρησε περισσότερο από οποιονδήποτε χημικό της γενιάς του, αμφισβητώντας τη δομή της επικρατούσας χημικής θεωρίας. Ο μεγάλος αυτός ερευνητής χρησιμοποίησε χημικές μεθόδους για να αποδείξει ότι διαφορετικά σώματα διασπώνται σε διαφορετικές ουσίες. Ο Robert Boyle δεν ξέφυγε πολύ από τις επικρατούσες αντιλήψεις (δηλ. την πεποίθηση ότι υπήρχαν "άτομα" φωτιάς) που σχετίζονταν με την καύση και την αναπνοή των ζώων. Μετά από πολλές περιηγήσεις σε διάφορες χώρες κατέληξε στην Οξφόρδη το 1667, όπου εφηύρε την αντλία αερίων. Με την αντλία αυτή έκανε πειράματα σε κενό και διατύπωσε τους νόμους των αερίων, την περίφημη σχέση PV = σταθερά, υπό σταθερή θερμοκρασία, μια κοινή γνώση σήμερα, σημαντικό όμως εύρημα για εκείνη την εποχή.



O Johannes (John) Mayow (1641-1679) και τα σκεύη που χρησιμοποιούσε για τα περίφημα πειράματά του πάνω στην αναπνοή των ζώων
Ο Robert Hooke (1635-1703) και το μικροσκόπιό του. 'Ισως δεν είναι ευρύτερα γνωστό ότι είναι ο πρώτος που παρατήρησε τα κύτταρα. Ο όρος cell (για τα κύτταρα) οφείλεται στον Hook. Με τον όρο cell (κελί) ήθελε να παρομοιάσει τα κύτταρα με τα κελιά των μοναχών.
Ο Robert Boyle συνεργάσθηκε με τους επίσης φυσικούς φιλόσοφους της Οξφόρδης, τον Robert Hooke (1635-1703), έναν πανεπιστήμονα (φυσικός, χημικός, βιολόγος, αστρονόμος, μηχανικός, αρχιτέκτονας), ευρύτερα γνωστό κυρίως από τον νόμο της ελαστικότητας ο οποίος φέρει το όνομά του, όπως και τον John Mayow (1641-1679). Αυτοί οι δύο ερευνητές πραγματοποιούσαν μελέτες, ο πρώτος στα προϊόντα καύσης ενός κεριού και ο δεύτερος στην αναπνοή των ζώων, κλείνοντας τα πειραματόζωά του μέσα σε ένα δοχείο. Και στις δύο περιπτώσεις παρατηρούσαν όμοια αποτελέσματα και κατέληγαν στο συμπέρασμα ότι για να διατηρηθεί τόσο η καύση, όσο και η αναπνοή σε ένα κλειστό χώρο, ήταν απαραίτητη η συνεχής παροχή αέρα, αλλιώς το κερί θα έσβηνε και το ζώο θα πέθαινε.
Την ουσία που συντηρούσε την καύση ονομάστηκε από τον Mayow νιτρο-αερώδες πνεύμα (spiritu nitro-aereo), επειδή ο ερευνητής (σωστά) συσχέτιζε τα φαινόμενα αυτά με κάποιες ουσίες που περιέχονται στο "νίτρο" (KNO3). Ο Mayow θεωρούσε ότι το νιτρο-αερώδες πνεύμα είχε σχέση με τους σεισμούς, τους κεραυνούς και την κατάψυξη. Χρειάστηκαν άλλα 100 χρόνια για να ανακαλυφθεί το οξυγόνο από τον Lavoisier και να γίνει αντιληπτό ότι αυτό το αέριο τροφοδοτούσε την καύση και τη ζωή.


Οι θεμελιωτές της φλογιστικής θεωρίας: Johann Joachim Becher (1635-1682) και Georg Ernst Stahl (1660-1734).
10.1. Φλογιστική θεωρία. Το 1667 δύο Γερμανοί αλχημιστές - χημικοί, οι Johann Joachim Becher (1635-1682) και Georg Ernst Stahl (1660-1734), δημιούργησαν τη μυστικιστική θεωρία για το φλογιστόν (phlogiston) για να ερμηνεύσουν το φαινόμενο της καύσης. Σύμφωνα με τη θεωρία τους υπάρχει μια ιδιαίτερη μορφή ύλης, μια ουσία, το φλογιστόν, η οποία βρίσκεται σε κάθε υλικό που μπορεί να καεί. Το φλογιστόν χάνεται στον αέρα εν μέρει ή συνολικά κατά την καύση της ουσίας.
Η αντίληψη ότι η φλόγα απομακρύνει κάτι από το καιόμενο σώμα υπήρχε ήδη από την αρχαιότητα. Η αντίληψη αυτή συναντάται στην αριστοτελική θεωρία των τεσσάρων στοιχείων "γη, ύδωρ, πυρ και αήρ", αλλά και στα έργα του Παράκελσου για τις δύο εκπνοές της Γης. Το καθαρό συμπέρασμα ήταν ότι ό,τι καίγεται περιέχει την ουσία "φλογιστόν", το οποίο αποβάλλει κατά την καύση. 'Ετσι ίσχυαν "αντιδράσεις" όπως:
ξύλο στάχτη + φλογιστόν, σίδηρος
στάχτη + φλογιστόν, σίδηρος  σκουριά + φλογιστόν,
σκουριά + φλογιστόν,
κάρβουνο φλογιστόν, θειάφι
φλογιστόν, θειάφι  στάχτη (αεριώδης) + φλογιστόν
στάχτη (αεριώδης) + φλογιστόν
'Οταν διαπιστώθηκε ότι για να υπάρξει καύση ήταν απαραίτητη και η παρουσία αέρα και ότι από αυτόν ένα μέρος ουσιαστικά δεν χρησιμοποιείται για τις καύσεις, εισήχθησαν οι έννοιες του φλογιστικοποιημένου (phlogistated), που στην ουσία ήταν το CO2, και του αποφλογιστικοποιημένου (dephlogistated) αέρα, που στην ουσία ήταν το Ο2, καθώς και του μεφιτικού αέρα (mephitic, από το λατινικό mephitis: τοξικός, δύσοσμος), που στην ουσία ήταν το Ν2. Οπότε ήταν:
ξύλο + κοινός αέρας στάχτη + φλογιστικοποιημένος αέρας
στάχτη + φλογιστικοποιημένος αέρας
και κοινός αέρας = μεφιτικός αέρας + αποφλογιστικοποιημένος αέρας, οπότε:
φλογιστικοποιημένος αέρας = αποφλογιστικοποιημένος αέρας + φλογιστόν



Ο διάσημος 'Αγγλος φυσιοδίφης, θεολόγος, ιερέας και χημικός Joseph Pristley (1733-1804). Ο πρώτος που απομόνωσε το οξυγόνο, αν και δεν το αναγνώρισε ως ξεχωριστό στοιχείο, επηρεασμένος από τη φλογιστική θεωρία της οποίας υπήρξε ένθερμος οπαδός. Δεξιά: Τα σκεύη που χρησιμοποίησε στις μελέτες πάνω στα διάφορα "είδη" αέρα.
Η φλογιστική θεωρία επικράτησε ουσιαστικά σε όλη τη διάρκεια του 18ου αιώνα, αν και προς το τέλος του αιώνα άρχισαν να εμφανίζονται κάποιες ασυνέπειες στη δομή της. Για παράδειγμα, είχαν ήδη διαπιστώσει ότι ο "αποφλογιστικοποιημένος" υδράργυρος, δηλαδή το οξείδιο του υδραργύρου, μπορούσε με απλή θέρμανση να ξαναδώσει υδράργυρο χωρίς κάποια "πηγή φλογιστού", όπως π.χ. άνθρακα, που χρειαζόταν για να ληφθούν άλλα μέταλλα από τα οξείδιά τους.
Ακόμη, είχε πλέον διαπιστωθεί ότι η καύση των μετάλλων στον αέρα, οδηγούσε σε προϊόν μεγαλύτερου βάρους, σε αντίθεση με ό,τι συνέβαινε π.χ. με το ξύλο. Αυτό οδήγησε πολλούς να πιστεύουν ότι το φλογιστόν, που "έχαναν" κατά την καύση, μπορεί να είχε και αρνητικό βάρος. 'Ολα αυτά άρχισαν να δημιουργούν σοβαρά "ρήγματα" στη θεωρία του φλογιστού.
Θα πρέπει εδώ να τονιστεί ότι οι οπαδοί της θεωρίας του φλογιστού δεν ήταν παραδοξολόγοι και ευφάνταστοι αλχημιστές, ούτε τσαρλατάνοι. Οι περισσότεροι ήταν σοβαροί επιστήμονες που προσπαθούσαν να απαντήσουν σε βασικές χημικές ερωτήσεις πραγματοποιώντας προσεκτικά πειράματα και σχολαστικές μετρήσεις, αξιοποιώντας στον μέγιστο δυνατό βαθμό τις περιορισμένες γνώσεις της εποχής. Μεταξύ των πλέον διάσημων και ένθερμων υποστηρικτών της και μέχρι τέλους της ζωής του ήταν ο διάσημος Joseph Pristley (1733-1804), ο οποίος υπεράσπιζε τη θεωρία ακόμη και όταν οι "αντι-φλογιστές" (με επικεφαλής τον Lavoisier) φαινόταν ότι είχαν αρχίσει πλέον να επικρατούν.
Η φλογιστική θεωρία, όσο και αν για τα σημερινά δεδομένα μας φαίνεται εξαιρετικά παράδοξη, σε κάποιο βαθμό είχε πλησιάσει την αλήθεια. Το φλογιστόν στην ουσία αντιπροσώπευε την "τάση" ή τη "δίψα" μιας ουσίας να προσλάβει οξυγόνο. 'Ετσι, η αντίδραση μιας ουσίας με το οξυγόνο, αντί να γραφεί συμβατικά ως: Α + [Ο] Β, θα μπορούσε να γραφεί και ως: Α
Β, θα μπορούσε να γραφεί και ως: Α  Β + [-Ο]. Αυτό το "αρνητικό" οξυγόνο ή "αντι-οξυγόνο" αντιπροσωπεύεται από το φλογιστόν.
Β + [-Ο]. Αυτό το "αρνητικό" οξυγόνο ή "αντι-οξυγόνο" αντιπροσωπεύεται από το φλογιστόν.
10.2. Μετρήσεις ακριβείας. Από τις αρχές του 18ου αιώνα οι ερευνητές άρχισαν να γίνονται πιο σχολαστικοί στα πειράματά τους και άρχισαν πλέον να κάνουν συστηματική χρήση του ζυγού. Την αρχή έκανε ο ο Σκωτσέζος χημικός Joseph Black (1728-1799), ο οποίος θεωρείται ως ο εφευρέτης του αναλυτικού ζυγού και άρχισε να περιγράφει τα πειράματά του παρουσιάζοντας ακριβείς ποσοτικές σχέσεις. Αλλά ο Antoine-Laurent Lavoisier (1743-1794), έκανε το ζύγισμα με ακρίβεια αναπόσπαστο τμήμα της επιστήμης της Χημείας και διέλυσε τους γρίφους της αλχημιστικής αντίληψης.
Ο Lavoisier σε ηλικία 26 ετών έγινε γνωστός όταν κατέρριψε τη μέχρι τότε επικρατούσα θεωρία ότι το νερό μετατρέπεται σε "γη" κατά την επαναλαμβανόμενη απόσταξη. Για 100 ημέρες έβραζε νερό και μετέφερε το απόσταγμα που συνέλεγε, ξανά στον βραστήρα, έτσι ώστε να μην υπάρχει κάποια απώλεια. Ζυγίζοντας την αποστακτική συσκευή με το νερό πριν και μετά την όλη διαδικασία, όπως και το στερεό υπόλειμμα που είχε μαζευτεί στην αποστακτική συσκευή, έδειξε ότι το στερεό αυτό προϊόν προερχόταν από τα γυάλινα σκεύη και όχι από το νερό.


Ο Σκωτσέζος χημικός Joseph Black (1728-1799) εισήγαγε τους ζυγούς ακριβείας (αναλυτικούς ζυγούς) στα χημικά εργαστήρια.
Το 1772, ο Lavoisier άρχισε να εξετάζει τον ρόλο του αέρα στην καύση. Με καύση διάφορων υλικών (P, S, Pb) σε κλειστά δοχεία και προσεκτικές ζυγίσεις (η ακρίβεια ζύγισης που είχε πετύχει ήταν 0,5 mg) διατύπωσε την σωστή άποψη ότι το υλικό που καίγεται δεν αποβάλλει φλογιστόν, αλλά ενώνεται με ένα μέρος του αέρα, δηλαδή οξειδώνεται.
Ο Lavoisier υπήρξε εισηγητής και ένθερμος υποστηρικτής της αντι-φλογιστικής θεωρίας. Σύντομα, το φλογιστόν δεν είχε πλέον θέση στη θεωρία και σταδιακά τέθηκε στο περιθώριο, παρά το ότι μερικοί αξιόλογοι ερευνητές της εποχής, όπως ο Pristley, συνέχισαν να το θεωρούν θεμέλιο της χημικής θεωρίας. Η φλογιστική θεωρία, παρά τις αντιφάσεις της, διατηρήθηκε για ορισμένο διάστημα γιατί εξυπηρετούσε ιδεολογικές αντιλήψεις μερικών γνωστών επιστημόνων της εποχής.

Ο Antoine Lavoisier και η σύζυγός του Marie-Anne (Πίνακας του Jacques-Louis David, 1788). Ο Lavoisier θεμελίωσε τη σύγχρονη Χημεία. Μεταξύ πολλών άλλων, απέδειξε με σχολαστικά πειράματα και διατύπωσε τον βασικό νόμο της Χημείας για τη διατήρηση της μάζας. 'Ομως καρατομήθηκε, αφού "Η Δημοκρατία δεν χρειαζόταν ούτε επιστήμονες, ούτε χημικούς".
Ο Lavoisier αργότερα κατέληξε στο συμπέρασμα ότι ο αέρας ήταν μίγμα αερίων, όπου το 20% ήταν ένα αέριο, που το ονόμασε οξυγόνο, χρήσιμο στην καύση ενώ το υπόλοιπο ήταν ένα αέριο που δεν μπορούσε να διατηρήσει την καύση. Το ονόμασε oxygenium, με βάση την εσφαλμένη αντίληψη της εποχής, ότι αποτελεί συστατικό όλων των οξέων, δηλαδή ότι είναι το στοιχείο που "παράγει οξέα". Το 1787, με το βιβλίο του Méthode de Nomeclature Chimique καθιέρωσε ένα μεθοδικό και συστηματικό τρόπο ονοματοδοσίας των χημικών στοιχείων. Το 1789 δημοσίευσε το πρώτο βασικό εγχειρίδιο Χημείας το Traité Elémentaire de Chimie.
Ο Lavoisier, αν και ενεργός υποστηρικτής της Γαλλικής επανάστασης, αφενός μεν λόγω της αριστοκρατικής του καταγωγής, αφετέρου λόγω της άτυχης επαγγελματικής ενασχόλησής του σε σώμα φοροεισπρακτόρων, συνελήφθη και καταδικάστηκε σε θάνατο κατά τα χρόνια της τρομοκρατίας του Ροβεσπιέρου.
'Ισως, η μοίρα του Lavoisier είχε σφραγισθεί από κάποια χρόνια πριν, όταν είχε απορρίψει ως απαράδεκτη μια "επιστημονική" εργασία του Jean-Paul Marat, ενός από τους φανατικότερους ηγέτες της Γαλλικής Επανάστασης κατά την περίοδο της τρομοκρατίας, στερώντας του τη θέση μέλους της Γαλλικής Ακαδημίας των Επιστημών.
'Οταν ζητήθηκε από το δικαστήριο να του χαριστεί η ζωή για να συνεχίσει τα πειράματά του, ο δικαστής απέρριψε την αίτηση με την περίφημη φράση: "Η Δημοκρατία δεν χρειάζεται ούτε επιστήμονες, ούτε χημικούς". Καρατομήθηκε αμέσως μετά την απόφαση, στις 8 Μαΐου του 1794, μαζί με άλλους 27 καταδικασμένους ανθρώπους. Το σώμα του ρίχτηκε σε έναν κοινό τάφο.
Ο μαθηματικός Lagrange σχολιάζοντας την είδηση της εκτέλεσης του Lavoisier είπε "χρειάσθηκε μια στιγμή για να κοπεί αυτό το σπάνιο κεφάλι, αλλά και εκατό χρόνια να περάσουν δεν θα γεννηθεί άλλο αντάξιό του".

Διεξαγωγή πειράματος στο εργαστήριο του Lavoisier πάνω στην ανθρώπινη αναπνοή (σκίτσο της Marie-Anne Lavoisier, που φαίνεται δεξιά να κρατά σημειώσεις).
10.3. Ανακάλυψη Αερίων. Σημαντικό στάδιο εξέλιξης της επιστήμης της Χημείας αποτέλεσαν οι πειραματικές προσπάθειες για την ανακάλυψη αερίων και της σύστασης του αέρα. Από το 1624 ο Φλαμανδός ιατρός Jan Baptist van Helmont (1579-1644) διαπίστωσε ότι υπάρχουν διαφορετικά αέρια με διαφορετικές ιδιότητες. Ο van Helmont ανακάλυψε το διοξείδιο του άνθρακα (CO2), ως προϊόν της καύσης ξύλου και άλλων οργανικών ενώσεων και αρχικά το ονόμασε ξυλαέριο (ονομάσθηκε δεσμευμένος αέρας, fixed air, και φλογιστικοποιημένος αέρας, phlogisticated air).
Ο van Helmont ήταν εκείνος που εισήγαγε τον όρο-λέξη gas στο επιστημονικό λεξιλόγιο για την περιγραφή των διαφόρων "ειδών" αερίων ή "πνευμάτων". Πρέπει να σημειωθεί ότι αυτή η κοινή πλέον λέξη σε πολλές γλώσσες (gas: αγγλικά, γερμανικά, ισπανικά, ιταλικά, gaz: γαλλικά, газа: ρωσικά), έχει Ελληνική ρίζα και προέρχεται από τη λέξη χάος.
Τα πειράματά του van Helmont βοήθησαν τον Joseph Black και αργότερα τον Lavoisier να προτείνουν ότι ο ατμοσφαιρικός αέρας δεν είναι ένα αέριο, αλλά είναι μίγμα αερίων. Η πρόταση αυτή ήταν πολύ τολμηρή για την εποχή της, αφού βρισκόταν σε αντίθεση με την αριστοτέλεια αντίληψη, ότι ο αέρας δεν είναι μίγμα, αλλά είναι ένα από τα τέσσερα στοιχεία (γη, πυρ, αέρας, νερό).

Πειραματική διάταξη που χρησιμοποίησε ο Pristley για την παρασκευή οξυγόνου με θέρμανση οξειδίου του υδραργύρου
Ο Ο Joseph Pristley παρασκεύασε, απομόνωσε και χαρακτήρισε πολλούς "αέρες", όπως: Τον νιτρώδη αέρα (nitrous air, δηλ. το NO), τον ατμό του πνεύματος του άλατος ή όξινο αέρα (vapor of spirit of salt, acid air, δηλ. το HCl), τον αλκαλικό αέρα (alkaline air, δηλ. την ΝΗ3), τον αποφλογιστικοποιημένο νιτρώδη αέρα (dephlogisticated nitrous air, δηλ. το N2O) και κυρίως τον αποφλογιστικοποιημένο αέρα (dephlogisticated air, δηλ. το Ο2). 'Ετσι, αν και απομόνωσε το οξυγόνο (με θερμική διάσπαση του HgO στους 350 ºC), δεν αναγνώρισε τη στοιχειακή του φύση ως οπαδός της φλογιστικής θεωρίας.
Το υδρογόνο (H2) ανακαλύφθηκε αρχικά από τον Robert Boyle, αλλά μελετήθηκε συστηματικά από τον 'Αγγλο Henry Cavendish (1731-1810) που το αποκάλεσε εύφλεκτο αέρα και κάποια εποχή ταυτίστηκε με το φλογιστόν. Ο Cavendish, επινόησε μέθοδο παραγωγής και αποθήκευσης υδρογόνου πάνω από υδράργυρο και επίσης έδειξε ότι το νερό είναι το προϊόν της εκρηκτικής αντίδρασης μεταξύ υδρογόνου και το οξυγόνου. Υπήρξε ο πρώτος που εξέτασε σχολαστικά στη σύνθεση του αέρα και κατέληξε στο συμπέρασμα ότι "ο αέρας αποτελείται κατά ένα μέρος από αποφλογιστικοποιημένο αέρα [εννοώντας το οξυγόνο] και κατά τέσσερα μέρη από φλογιστικοποιημένο αέρα [εννοώντας το άζωτο]" (1785). Ακόμη, παρατήρησε ότι με δέσμευση του οξυγόνου και του αζώτου, παρέμενε αδέσμευτο το 1/120 του αρχικού όγκου αέρα. Την παρατήρηση αυτή αξιοποίησαν οι Rayleigh και Ramsay μετά από 100 χρόνια για να ανακαλύψουν αρχικά το αργόν και στη συνέχεια τα υπόλοιπα ευγενή αέρια (βλ. παρακάτω).
Ο Σουηδός φαρμακοποιός Carl Wilhelm Scheele (1742-1786) προσδιόρισε ότι ο αέρας ήταν μίγμα δύο αερίων, από τα οποία μόνο το ένα μπορούσε να συντηρήσει την καύση. 'Ηταν ο πρώτος που παρέλαβε καθαρό οξυγόνο, αλλά δεν το αναγνώρισε ως στοιχείο. Αργότερα παρασκεύασε και μελέτησε το υδροφθόριο (HF), το υδρόθειο (H2S), το υδροκυάνιο (HCN ), ενώ το 1774 απομόνωσε το κιτρινοπράσινο αέριο χλώριο (Cl2), το οποίο ονόμασε "αποφλογιστικοποιημένο μουριατικό οξύ" (μουριατικό οξύ: υδροχλωρικό οξύ). Επίσης ανακάλυψε τα αέρια: αμμωνία (NH3), διοξειδίου του θείου (SO2) και το υδροχλώριο (HCl). Το 1772, παρασκεύασε το "αεριούχο νερό", δηλαδή υπέρκορο διάλυμα διοξειδίου του άνθρακα (CO2) σε νερό.
Η συνεισφορά του Scheele στη Χημεία ήταν μεγάλη. Πέραν από την ανακάλυψη του οξυγόνου και του χλωρίου, ανακάλυψε ακόμη τα στοιχεία βάριο (1774), μαγγάνιο (1774), μολυβδαίνιο (1778) και βολφράμιο (1781). Παρά το ότι ο Scheele δεν είχε στη διάθεσή του τα εξελιγμένα χημικά όργανα που διέθετε το εργαστήριο του Lavoisier, με τη δουλειά του συνεισέφερε στην κατάρριψη της φλογιστικής θεωρίας. Ο θάνατός του σε σχετικά μικρή ηλικία (44 ετών) αποδίδεται στη συνεχή ενασχόλησή του με τοξικές ενώσεις βαρέων μετάλλων (μολύβδου, υδραργύρου), η επικινδυνότητα των οποίων δεν είχε ακόμη εκτιμηθεί σωστά.
Το άζωτο ανακαλύφθηκε αργότερα από τον μαθητή του Black, Daniel Rutherford (1749-1819), ο οποίος παρατήρησε ότι μετά από μια καύση σε κλειστό δοχείο, παραμένει ένα άγνωστο αέριο που δεν μπορούσε να συντηρήσει την καύση, αλλά και τη ζωή οργανισμών (α+ζωή). Το αέριο αυτό το ονόμασε "βλαβερό αέρα" ή "φλογιστικοποιημένο αέρα".




Jan Baptist van Helmont
(1579-1644)
Henry Cavendish
(1731-1810)
Carl Wilhelm Scheele
(1742-1786)
Daniel Rutherford
(1749-1819)
Οι ανακαλύψεις αυτές ήταν εξαιρετικής σημασίας για την εποχή τους. Παρά τις δυσκολίες να καταλάβουν τη φύση των στοιχείων και τα μίγματα, οι πειραματιστές της εποχής εκείνης έκαναν μεγάλες προόδους στην κατανόηση των βασικών αρχών της Χημείας. 'Ηταν μια εποχή κατά την οποία επικρατούσε πλήθος εσφαλμένων θεωριών λόγω της ιδεαλιστικής αντίληψης των πραγμάτων και του θρησκευτικού δογματισμού. Χρειαζόταν ένας Lavoisier, οι κορυφαίες ανακαλύψεις του οποίου καθιέρωσαν τη Χημεία ως θετική επιστήμη και διέλυσαν πολλούς "επιστημονικούς μύθους".
Πηγές από το Διαδίκτυο: (1) "Phlogiston Theory" (Jim Loy, 1996). (2) "Considerations on the Doctrine of Phlogiston and the Decomposition of Water" (Joseph Priestly, 1796). (3) "Death of Lavoisier" (John H. Lienhard).





Joseph Louis Proust
(1754-1806)
Claude Louis Berthollet
(1748-1822)
John Dalton
(1766-1844)
Amedeo Avogardo
(1776-1856)
Jöns Jakob Berzelius
(1779-1848)


'Ατομα και μόρια όπως απεικονίζονται στο σύγγραμμα του Dalton "A New System of Chemical Philosophy" (1808) (αποσπάσματα).
11. 18ος - 19ος αιώνας: Ατομική Θεωρία και Περιοδικός Πίνακας
Στις αρχές του 18ου αιώνα άρχισε να διαμορφώνεται η πεποίθηση μεταξύ των χημικών της εποχής εκείνης ότι οι χημικές ενώσεις έχουν συγκεκριμένη σύνθεση και ότι αποτελούνται από συγκεκριμένα στοιχεία και σε σταθερές αναλογίες μεταξύ τους ("νόμος καθορισμένων αναλογιών"). Ο κύριος υποστηρικτής αυτής της ιδέας υπήρξε ο Γάλλος χημικός Joseph Louis Proust (1754-1806).
Το 1797, ο Γάλλος χημικός Claude Louis Berthollet (1748-1822), απέρριψε τον νόμο των καθορισμένων αναλογιών, θεωρώντας ότι η αναλογία των στοιχείων σε μια ένωση καθορίζεται από την αναλογία υπό την οποία λαμβάνονται τα αντιδρώντα. Η άρνηση του Berthollet (ο οποίος βρισκόταν σε μόνιμη επιστημονική διαμάχη με τον Proust), η γνώμη του οποίου μέτραγε πολύ στην επιστημονική κοινότητα, καθυστέρησε την αποδοχή της ορθής θεωρίας του Proust.
Το θέμα ξεκαθάρισε σε μεγάλο βαθμό το 1808 με τη διατύπωση της ατομική θεωρίας του 'Αγγλου χημικού John Dalton (1766-1844). Ο Dalton υποστήριξε ότι τα στοιχεία αποτελούνται από μικροσκοπικά, άτμητα και άφθαρτα σωματίδια, συνδυασμοί των οποίων δημιουργούν τις διάφορες ουσίες. Στο κάθε στοιχείο ο Dalton είχε αποδώσει ένα σύμβολο.
Η θεωρία του Dalton, στην ουσία της, βασίζεται στην ιδέα της ατομικής θεωρίας του Δημόκριτου, και είχε σημαντική επίδραση στην εξέλιξη της Χημείας, αφού άρχισαν πλέον να αποδίδονται συγκεκριμένα ατομικά βάρη στα διάφορα στοιχεία. 'Ολα αυτά περιγράφονται στο περίφημο βιβλίο του Dalton Νέο Σύστημα της Χημικής Φιλοσοφίας (A New System of Chemical Philosophy).
Τιμητικά, το όνομα του Dalton διατηρείται στις μονάδες μοριακής μάζας κυρίως μεγαλομοριακών ενώσεων, π.χ. η πρωτεΐνη αιμοσφαιρίνη Α αναφέρεται ότι έχει μοριακή μάζα 68 kilodalton (kDa).
Κατά τη διάρκεια του 19ου αιώνα οι χημικοί είχαν χωρισθεί σε δύο στρατόπεδα γύρω από την ατομική θεωρία. Ο διάσημος Ιταλός χημικός Amedeo Avogardo (1776-1856) και ο Αυστριακός φυσικός Ludwig Edward Boltzmann (1844-1906) υπήρξαν ένθερμοι υποστηρικτές της ατομικής θεωρίας και συνεισέφεραν σε αυτήν με ανακαλύψεις στον τομέα των αερίων. Εναντίον της θεωρίας ήταν οι χημικοί Wilhelm Ostwald και Ernst Mach. O Avogadro πρότεινε τον διάσημο νόμο που φέρει το όνομά του, ότι "ίσοι όγκοι αερίων, κάτω από την ίδια πίεση και θερμοκρασία, περιέχουν ίσο αριθμό μορίων". Ως σταθερά ή αριθμός Avogadro (NA) αναφέρεται και ο αριθμός των μορίων που περιέχονται σε ένα γραμμομόριο μιας χημικής ένωσης
Το 1808, ο Σουηδός χημικός Jöns Jakob Berzelius (1779-1848) στο βιβλίο του Lãrbok I Kemien, πρότεινε τα σημερινά χημικά σύμβολα των στοιχείων (όσων είχαν μέχρι τότε βρεθεί) σε αντικατάσταση των γεωμετρικών συμβόλων, που χρησιμοποιούσε o Dalton. Ακόμη, καθιέρωσε τον σημερινό τρόπο αναγραφής των χημικών αντιδράσεων (μια μικρή διαφορά ήταν ότι ο αριθμός των ατόμων ενός στοιχείου σε ένα μόριο γραφόταν ως άνω δείκτης και όχι ως κάτω δείκτης), καθώς και την έννοια των ατομικών βαρών των στοιχείων .
Ο Berzelius ήταν αυτός που καθιέρωσε στη Χημεία χημικούς όρους με ελληνικές ρίζες, που περιγράφουν τα φαινόμενα όπως, π.χ. η κατάλυση, ο πολυμερισμός, ο ισομερισμός και αλλοτροπισμός.
Για αρκετές δεκαετίες η ανακάλυψη νέων στοιχείων υπήρξε ένα σημαντικό γεγονός στη Χημεία και ο αριθμός των χημικών στοιχείων αυξάνονταν, με μέσο ρυθμό ενός στοιχείου για κάθε έτος κατά την περίοδο 1840-1870. Καθώς οι φυσικές και οι χημικές ιδιότητες των στοιχείων άρχισαν να γίνονται γνωστά, ορισμένοι χημικοί άρχισαν να παρατηρούν κάποιες ομοιότητές τους κατά ομάδες, όπως και κάποια "περιοδικότητα" στις ιδιότητές, όταν τα στοιχεία εξετάζονταν κατά σειρά αυξανόμενου ατομικού βάρους. 'Οπως είναι γνωστό, εκείνη την εποχή δεν υπήρχε η παραμικρή ιδέα για την ηλεκτρονιακή δομή των ατόμων.



Robert Bunsen (1811-1899)
Gustav Kirchhoff (1824-1887)
Μια από τις αρχικές μορφές φασματοσκόπιου, εφεύρεση των Bunsen και Kirchhoff (1859)
Το 1864, ο Γερμανός Lothar Meyer (1830-1895) ήταν ο πρώτος που ασχολήθηκε με την κατάταξη των στοιχείων σε μια πρωταρχική μορφή "περιοδικού πίνακα", αλλά υπήρχαν και σημαντικά κενά σε πολλά σημεία του. Πέντε χρόνια αργότερα, το 1869, με το θέμα της περιοδικότητας των ιδιοτήτων των χημικών στοιχείων ασχολήθηκε ο Ρώσος χημικός Dmitri Mendeleev (1834-1907).
Τόσο ο Meyer, όσο και ο Mendeleev είχαν σπουδάσει υπό τον διάσημο χημικό Robert Bunsen (1811-1899). Θα πρέπει εδώ να σημειωθεί ότι ο Bunsen μαζί με τον επίσης διάσημο φυσικό Gustav Kirchhoff (1824-1887), θεωρούνται οι θεμελιωτές της φασματοσκοπίας, μέσω της οποίας ανακάλυψαν δύο ακόμη στοιχεία: το 1860 το καίσιο (Cs) και το 1861 το ρουβίδιο (Rb), που κάλυψαν δυο κενές θέσεις της 1ης ομάδας του περιοδικού πίνακα (ομάδα αλκαλίων).
To 1869, ο Mendeleev μελέτησε συστηματικά (τότε ήταν πλέον γνωστά 63 στοιχεία) τον πίνακα του Meyer και άρχισε να συγκεντρώνει πληροφορίες για τα κενά. Εξετάζοντας την περιοδικότητα διάφορων φυσικών και χημικών ιδιοτήτων των στοιχείων, ήταν σε θέση να προβλέψει τις φυσικές και χημικές ιδιότητες των στοιχείων (και των ενώσεών τους), που βρίσκονταν στον πίνακά του κάτω από το πυρίτιο, το αργίλιο και το βόριο και δεν είχαν ακόμη ανακαλυφθεί. Μάλιστα τους είχε δώσει τα "προσωρινά" ονόματα: εκα-πυρίτιο, εκα-αργίλιο και εκα-βόριο.
Ο Mendeleev χρησιμοποιούσε στα προσωρινά ονόματα τα προθήματα eka-, dvi- και tri- (στα σανσκριτικά: ένα, δύο, τρία) για να δηλώσει τον αριθμό θέσεων κάτω από το στοιχείο που ακολουθεί (π.χ. εκα-πυρίτιο: το στοιχείο που βρίσκεται μία θέση κάτω από το πυρίτιο). 'Οταν αργότερα ανακαλύφθηκαν τα στοιχεία αυτά (γερμάνιο, γάλλιο και σκάνδιο), οι προβλέψεις του Mendeleev αποδείχθηκαν εξαιρετικά ακριβείς.
Για να εκτιμηθεί το μέγεθος του επιτεύγματος της σχεδίασης του πρώτου περιοδικού πίνακα, θα πρέπει να ληφθεί υπόψη το γεγονός ότι την εποχή εκείνο οι επιστήμονες είχαν πλήρη άγνοια ως προς την δομή των ατόμων και ως προς την ύπαρξη των ηλεκτρονίων. Οι Mendeleev και Meyer βραβεύθηκαν ισάξια για το επιστημονικό αυτό επίτευγμα από την Royal Society της Μ. Βρετανίας (το 1883) με το τιμητικό για εκείνη την εποχή Davy Medal. Ο Mendeleev τιμήθηκε επίσης όταν το ραδιενεργό στοιχείο με ατομικό αριθμό 101 ονομάστηκε Μεντελέβιο (Mendelevium, Md).



Lothar Meyer (1830-1895)
Dmitri Mendeleev (1834-1907)
Οι 5 πρώτες περίοδοι του Περιοδικού Πίνακα του Mendeleev (με αστερίσκο σημειώνονται οι κενές θέσεις στοιχείων των οποίων προέβλεψε τις ιδιότητες)

Friedrich Wöhler
(1800-1882)
12. Οργανική Χημεία και ο Βιταλισμός
Μετά την επικράτηση της ατομικής θεωρίας και των ποσοτικών σχέσεων που συνέδεαν τα χημικά στοιχεία στις διάφορες ενώσεις τους, η Χημεία έγινε επιστημονικός κλάδος με πειραματικά τεκμηριωμένο περιεχόμενο. Παρ' όλα αυτά ακόμη και μέχρι σχεδόν τα μέσα του 19ου αιώνα επικρατούσαν ακόμη κάποιες "βιταλιστικές" απόψεις, που είχαν τις βάσεις τους σε αριστοτελικές θεωρίες περί ζωής. Μέχρι το 1828 υπήρχε η γενική πεποίθηση ότι δεν είναι δυνατή η παρασκευή οργανικών ουσιών στο εργαστήριο. Για την παρασκευή του χρειαζόταν μια ζωική δύναμη (vis vitalis), μια δύναμη ακαθόριστης προέλευσης και φύσης που έδινε "ψυχή" στα οργανικά σώματα.
Παράλληλα, αρκετά διαδεδομένη ήταν και η θεωρία της αυτόματης γένεσης ή αβιογένεσης (spontaneous generation, abiogenesis), σύμφωνα με την οποία οι ζωντανοί οργανισμοί γεννούνται από ανόργανη ύλη (χώμα, λάσπη, φυτική ύλη) με "θεϊκή παρέμβαση". 'Ολα αυτά ήταν αποτέλεσμα εσφαλμένης ερμηνείας της εμφάνισης μικροοργανισμών και υδρόβιων μικρών ζώων (σκουλήκια, σκαθάρια, κ.λπ.) στις λάσπες αγρών, όπως και κατά τη σήψη φυτικής και ζωικής ύλης.
Οι οργανικές ενώσεις που είχαν απομονωθεί από διάφορα φυσικά προϊόντα ή μετά από φυσικές διεργασίες, όπως π.χ. η αιθανόλη, το οξικό οξύ, η ακετόνη, διάφορα σάκχαρα, ήταν άφθονες. Ο μοριακός τύπος πολλών από τις ενώσεις αυτές ήταν σε γενικές γραμμές γνωστός, ωστόσο το δόγμα της ζωικής δύναμης εκ των προτέρων απέτρεπε κάθε επιδίωξη σύνθεσής τους.
Το 1828, ο νεαρός Γερμανός χημικός Friedrich Wöhler διαπίστωσε ότι μπορούσε να παρασκευάσει στο εργαστήριο μία οργανική ένωση. Αυτό το πέτυχε τυχαία, όταν με θέρμανση κυανικού αμμωνίου (NH4OCN) παρασκεύασε την ουρία (H2NCONH2), η οποία είναι οργανική ένωση, σύμφωνα με την ακόλουθη αλληλουχία:
AgOCN + NH4Cl AgCl + NH4OCN NH4OCN
AgCl + NH4OCN NH4OCN  H2NCONH2.
H2NCONH2.
Είναι χαρακτηριστικό το "θριαμβευτικό" γράμμα που έστειλε στον σεβαστό καθηγητή του Berzelius, που υπήρξε ένθερμος οπαδός του βιταλισμού: "Πρέπει να σας πω ότι μπορώ να παρασκευάσω ουρία χωρίς να χρειαστώ νεφρά, ούτε άνθρωπο, ούτε σκύλο. Το κυανικό αμμώνιο είναι η ουρία!".
Ακολούθησαν βέβαια αντιδράσεις από τον Berzelius και άλλους υποστηρικτές του βιταλισμού, του τύπου "η ουρία βρίσκεται στο μεταίχμιο μεταξύ οργανικών και ανόργανων ενώσεων", αλλά το ρήγμα στη βιταλιστική θεωρία είχε ήδη γίνει. Και μια ακόμη εσφαλμένη θεωρία - τροχοπέδη καταρρίφθηκε. Το έτος 1828 θεωρείται πλέον το έτος έναρξης της Οργανικής Σύνθεσης. Στις μέρες μας, ο "παραδοσιακός" διαχωρισμός σε της Χημείας σε Ανόργανη και Οργανική εξακολουθεί να υφίσταται, αλλά καθαρά για λόγους συστηματικότερης εκμάθησης.



Αριστερά: Ο Jean Louis Pasteur (1822-1895) πειραματιζόμενος με τις περίφημες φιάλες χάρις στις οποίες κατέρριψε τη θεωρία της "αυτόματης γέννησης". Μέσον: Ο Pasteur έβρασε τον ζωμό σε μια φιάλη και στη συνέχεια έδωσε στο λαιμό το σχήμα S ("λαιμός κύκνου") με τη βοήθεια φλόγας. Αυτό αποτρέπει την εισαγωγή μικροοργανισμών του αέρα στη φιάλη, αλλά επιτρέπει τη μερική αναταλλαγή αέρα. 'Οταν ο "λαιμός κύκνου" έσπαζε, άρχιζε η ανάπτυξη μικροοργανισμών. Το θόλωμα στο ζωμό είναι ένδειξη ανάπτυξης μικροοργανισμών στον αρχικά διαυγή ζωμό κρέατος (περισσότερα). Δεξιά: Οι δύο κατοπτρικές κρυστάλλων του μικτού άλατος με αμμώνιο και νάτριο του D,L-τρυγικού οξέος ("ρακεμικού οξέος"), που διαχώρισε ο Pasteur με το χέρι και με απλή οπτική παρατήρηση (περισσότερα).
Το επόμενο σημαντικό θέμα που αντιμετωπίστηκε ήταν το θέμα της αυτόματης γένεσης των ζωντανών ειδών. Το θέμα αυτό είχε επηρεάσει αρνητικά την πρόοδο της βιοχημείας και της βιολογίας αλλά και άλλων επιστημών. Μάλιστα είχε επηρεάσει επιστήμονες και ιδεαλιστές φιλόσοφους (όπως ο Καντ, ο Χέγκελ) που είχαν συμβάλλει με σπουδαίες ανακαλύψεις. Τελικά, το θέμα έγινε τόσο σημαντικό ώστε η Γαλλική 'Ακαδημία Επιστημών προκήρυξε βραβείο σε όποιον θα κατόρθωνε με τεκμηριωμένα πειράματα να δείξει τι ακριβώς ισχύει.
Το βραβείο κέρδισε ο Γάλλος χημικός-μικροβιολόγος Jean Louis Pasteur (1822-1895) με τα απλά και ευφυή πειράματα που διεξήγαγε κατά το 1862-63. Ο Pasteur έδειξε ότι ζωμός κρέατος, που έχει βραστεί καλά και έχει προφυλαχθεί από μικροοργανισμούς του αέρα (χάρις σε φιάλες ειδικής κατασκευής που απέκλειαν την είσοδο αέρα) ήταν αδύνατο να αναπτυχθούν μικρόβια και άλλοι μικροοργανισμοί και μπορούσε ο ζωμός να μείνει αναλλοίωτος (και μάλιστα, όπως αποδείχθηκε, για χρόνια). Με αυτό το απλό πείραμα, που έμεινε στην ιστορία της Επιστήμης ως το πείραμα με τη φιάλη με "λαιμό κύκνου" ("swan neck" flask experiment), έδειξε ότι αυτόματη γένεση ζωής δεν υπάρχει, τερματίζοντας ένα ακόμη θέμα που ενέπλεκε την επιστήμη με παραδοξολογίες μυστικιστικού χαρακτήρα.
Το 1848, είχε προηγηθεί η επίλυση ενός άλλου χημικού προβλήματος από τον Pasteur. Είχε διαπιστωθεί ότι τρυγικό οξύ που λαμβανόταν από φυσικά προϊόντα (το L(+)-τρυγικό οξύ) είχε επακριβώς τις ίδιες χημικές ιδιότητες με το συνθετικά παρασκευαζόμενο τρυγικό οξύ ή το "παρατρυγικό οξύ" ή "ρακεμικό οξύ" (το D,L-τρυγικό οξύ), το οποίο μπορούσε να ληφθεί επίσης -κάτω υπό ορισμένες συνθήκες- και ως φυσικό προϊόν κατά τη ζύμωση του γλεύκους. Ωστόσο, το πρώτο έστρεφε το επίπεδο πόλωσης φωτός σε αντίθεση με το δεύτερο, που εμφανιζόταν ως "οπτικώς ανενεργό". Να σημειωθεί ότι το επίθετο "ρακεμικό" επεκτάθηκε αργότερα σε κάθε ισομοριακό μίγμα οπτικών αντιπόδων μιας ένωσης, αρχικά όμως αφορούσε το οπτικώς ανενεργό τρυγικό οξύ, δηλ. το D,L-τρυγικό οξύ.
O Pasteur κατάφερε εξοπλισμένος με τη βοήθεια ενός μεγεθυντικού φακού, με ένα τσιμπιδάκι και με μεγάλη υπομονή να διαχωρίσει τις δύο κατοπτρικές μορφές των κρυστάλλων του μικτού άλατος του ρακεμικού οξέος με αμμώνιο και νάτριο, το οποίο εμφανιζόταν ως οπτικώς ανενεργό. Διαπίστωσε στη συνέχεια ότι τα διαλύματα των δύο διαφορετικών κρυστάλλων είχαν ακριβώς αντίθετες στροφικές ικανότητες, ενώ ισομοριακό μίγμα τους δεν παρουσίαζε στροφική ικανότητα. 'Ετσι, ο Pasteur έδειξε έτσι το ρακεμικό οξύ αποτελείται από δύο "οπτικούς αντίποδες", αποδεικνύοντας έτσι την ύπαρξη χειραλικών ενώσεων. Ο Pasteur στάθηκε τυχερός διότι το άλας που χρησιμοποίησε είναι μια από τις λίγες ρακεμικές ουσίες που διαχωρίζονται σε οπτικούς αντίποδες κατά την κρυστάλλωση. Να σημειωθεί ότι τότε απολύτως τίποτα δεν ήταν γνωστό για τη στερεοχημεία των ενώσεων του άνθρακα, την τετραεδρική διάταξη των δεσμών του και φυσικά για τα D-, L- ή D,L-ισομερή.

Το κανονικό τετράεδρο των απλών δεσμών του άνθρακα (μόριο μεθανίου)
13. Οργανική Χημεία, Χημικοί Δεσμοί του 'Ανθρακα και Οργανικές Ενώσεις
Η Οργανική Χημεία έχει ως αντικείμενο μελέτης τις ενώσεις του άνθρακα. Ο άνθρακας παρουσιάζει κάποιες ξεχωριστές ιδιότητες σε σχέση με τα άλλα στοιχεία. Είναι το μοναδικό στοιχείο του οποίου τα άτομα μπορούν να σχηματίσουν δεσμούς μεταξύ τους δημιουργώντας επιμήκεις ανθρακικές αλυσίδες και δακτυλίους. Ο άνθρακας έχει τη δυνατότητα να σχηματίζει μια τεράστια ποικιλία χημικών ενώσεων, από το απλό μεθάνιο μέχρι τις πρωτεΐνες και τα νουκλεϊνικά οξέα με μοριακά βάρη της τάξης μερικών εκατομμυρίων. Αυτός είναι και ο λόγος που οι οργανικές ενώσεις είναι τα κύρια συστατικά μόρια των ζωντανών οργανισμών. Αλλά και η βιομηχανική επανάσταση δημιούργησε μεγάλο αριθμό χημικών βιομηχανιών με βάση τις οργανικές ενώσεις για φάρμακα, χρώματα, πολυμερή, φυτοφάρμακα, και βιοχημικά αντιδραστήρια.
Από τα μέσα του 19ου αιώνα άρχισε η ραγδαία ανάπτυξη της Οργανική Χημείας. Οι επιστήμονες άρχισαν να ενδιαφέρονται για τις δυνάμεις και τους δεσμούς που συγκρατούν τα άτομα άνθρακα μεταξύ τους και σχηματίζουν αυτήν την τεράστια ποικιλία ενώσεων. Το 1858, ο Γερμανός χημικός August Kekulé (1829-1896) και ο Σκώτος χημικός Archibald Couper (1831-1892), ανεξάρτητα ο ένας από τον άλλο, διατυπώνουν τις απόψεις τους για τις "τέσσερις μονάδες συγγένειας" ή δεσμούς του κάθε ατόμου άνθρακα. Η τετρασθένεια του άνθρακα ήταν δεδομένη και οι ενώσεις του σταθερές. Το 1865, ο Kekulé εισηγήθηκε ότι οι ανθρακικές αλυσίδες μπορούν να σχηματίσουν δακτυλίους με αναδίπλωση των δεσμών, ιδέα που ήταν αρκετά προχωρημένη για την εποχή του
Η θεωρία Kekulé για το τετρασθενές του άνθρακα ολοκληρώθηκε αργότερα με την παρέμβαση του Ολλανδού χημικού Jacobus van't Hoff (1852-1911, Nobel Χημείας του 1901) και του Joseph Le Bel (1847-1930), που επιβεβαίωναν ότι ο άνθρακας συνδέεται με άλλα τέσσερα άτομα τοποθετημένα στις 4 γωνίες ενός κανονικού τετραέδρου, με το άτομο του άνθρακα στο κέντρο του. Η πυραμιδική διάταξη φαίνεται ξεκάθαρα στην απλούστερη δυνατή περίπτωση, το μόριο μεθανίου (CH4).
Αρκετά, αργότερα οι χημικοί με μεγάλο αριθμό δεδομένων κατέληξαν οι 4 δεσμοί είναι ισοδύναμοι και σχηματίζονται με "ανάμιξη" ενός τροχιακού s και τριών τροχιακών p (υβριδισμός sp3). Ο υβριδισμός βοηθάει στον σχηματισμό 4 ισοδύναμων μοριακών τροχιακών τετραεδρικής διευθέτησης.


August Kekulé (1829-1896)
Η δομή του βενζολίου που προτάθηκε από τον Kekulé.
Η σημαντικότερη συμβολή του August Kekulé στην Οργανική Χημεία υπήρξε η θεωρία του για τη δομή του βενζολίου. Από τον 19ο αιώνα ήταν γνωστό ότι το βενζόλιο είχε τον μοριακό τύπο C6H6 και παρά την εμφανέστατη "ακορεστότητά" του, παρουσιαζόταν ως μια εξαιρετικά σταθερή ένωση με σημαντικές διαφοροποιήσεις ως προς τη χημική του συμπεριφορά, σε σχέση με άλλες γνωστές ακόρεστες οργανικές ενώσεις. Οι ιδιαιτερότητες αυτές αναφέρονται ως αρωνατικότητα ή αρωματικός χαρακτήρας.
Το 1865, ο Kekulé διατύπωσε την άποψη ότι το βενζόλιο αποτελείται από ένα εξαμελή δακτύλιο ανθράκων με τρεις διπλούς δεσμούς. Η ερμηνεία του ήταν ότι τρεις διπλοί δεσμοί "ταλαντώνονται" ταχύτατα μεταξύ δύο θέσεων. Η δομή αυτή γνώρισε την εποχή εκείνη πολλές επικρίσεις. Παρ' όλο που ερμήνευε ικανοποιητικά τον αριθμό των δισ-υποκατεστημένων βενζολίων, δεν μπορούσε να ερμηνεύσει την ελάχιστη δραστικότητα του βενζολίου σε σχέση με εκείνη των άλλων αλκενίων και ακόρεστων ενώσεων. Η ασυνήθιστη σταθερότητα του βενζολίου αποτέλεσε δυσεπίλυτο αίνιγμα για τους χημικούς της εποχής εκείνης.
Τελικά, απάντηση στο ερώτημα στο ερώτημα αυτό έδωσε η θεωρία του συντονισμού (ή μεσομέρειας), σύμφωνα με την οποία το βενζόλιο μπορεί να περιγραφεί ως ένα υβρίδιο δύο ισοδύναμων δομών, στις οποίες κάθε σύνδεση C-C αντιστοιχεί κατά μέσο όρο σε 1,5 δεσμό, δηλαδή σε μια ενδιάμεση κατάσταση μεταξύ απλού και διπλού δεσμού. Οι δομές συντονισμού διαφέρουν μόνο ως προς τις θέσεις των ηλεκτρονίων τους. Η πραγματική δομή βρίσκεται ανάμεσα στις δύο ακραίες εκδοχές.
Τελικά, η θεωρία του Kekulé για τη δομή του βενζολίου επικράτησε και οδήγησε στην υιοθέτηση ανάλογων τύπων για όλες τις αρωματικές ενώσεις. Το 1890, η "Εταιρεία των Γερμανών Χημικών" οργάνωσε ειδική τελετή, με το όνομα Benzolfest (: γιορτή για το βενζόλιο), για να τιμήσει τον Kekulé με την ευκαιρία της 25ης επετείου από τη δημοσίευση του πρώτου άρθρου του που πρότεινε τη δομή του βενζολίου. Στην ομιλία του, ο Kekulé αναφέρθηκε στο περίφημο "όνειρό" του (για τον "ουροβόρο όφι", πανάρχαιο αλχημιστικό σύμβολο του σύμπαντος), από το οποίο εμπνεύστηκε τη δομή του βενζολίου. Το όνειρο αυτό είναι ίσως ένα από τα ωραιότερα "παραμύθια" της χημείας (βλ. Χημική ένωση του μήνα: Βενζόλιο).





Γραμματόσημα που εκδόθηκαν προς τιμήν του Kekulé. Ο ίδιος και το περίφημο "όνειρό του" υπήρξαν θέματα πολλών χιουμοριστικών σκίτσων.

Justus von Liebig
(1803-1873)

Jean Baptiste Dumas
(1800-1884)

Charles Adolphe Wurtz
(1817-1884)

Edward Frankland
(1825-1899)
14. Εξελίξεις στη Χημεία κατά τον 19ο αιώνα
Η Χημεία απαλλαγμένη πλέον από παραδοξολογίες του παρελθόντος, από τα μέσα του 19ου αιώνα και μετά είναι πλέον μια καθιερωμένη και κοινωνικά αποδεκτή επιστήμη, αλλά συγχρόνως και ένα "παρθένο" έδαφος, το οποίο η ανθρώπινη διανόηση είναι πλέον έτοιμη να γονιμοποιήσει. Εμφανίζεται πλέον πλήθος λαμπρών επιστημόνων, ενδεχομένως με κάποιες προκαταλήψεις από διδασκαλίες και παραδοχές του παρελθόντος, αλλά αποκλειστικά επιστημονικού και μόνο χαρακτήρα, όπως και με νέες έξοχες ιδέες που χρειάζεται κάποιος αγώνας για να έρθουν στο προσκήνιο και να γίνουν αποδεκτές. Οι ανταγωνισμοί και οι αγώνες για την "προτεραιότητα" ιδεών είναι αναπόφευκτοι και συγχρόνως αποδοτικοί.

Το διάσημο σκεύος Kaliapparat, που επινόησε ο Liebig για τη δέσμευση του CO2 κατά τον στοιχειακό προσδιορισμό άνθρακα σε οργανικές ενώσεις.
Η Οργανική Χημεία επεκτάθηκε με ταχύτατο ρυθμό κατά τον 19ο και 20ο αιώνα με σημαντικό αριθμό νέων ανακαλύψεων και πειραματικών τεχνικών. Στην άνθιση της Οργανικής Χημείας συνέβαλε μια σειρά από έξοχους οργανικούς χημικούς που βελτίωσαν τις μέχρι τότε εργαστηριακές συσκευές, όπως ο Γερμανός Justus von Liebig (1803-1873) που συνεισέφερε πολλά στον τομέα του προσδιορισμού της στοιχειακής σύνθεσης των οργανικών ενώσεων.
Ο Γάλλος Jean Baptiste Dumas (1800-1884) καθιερώνει ως μονάδα το ατομικό βάρος του υδρογόνου, προσδιορίζει τα ατομικά βάρη του άνθρακα και του οξυγόνου και άλλων στοιχείων (συνολικά 30) και αναπτύσσει μέθοδο προσδιορισμού του αζώτου σε οργανικές ενώσεις.
Ο Γάλλος (Αλσατός) Charles Adolphe Wurtz (1817-1884) συνεισφέρει πολλά στην ανόργανη και στην οργανική σύνθεση και μένει στην ιστορία της Οργανικής Χημείας γνωστός χάρις στην ομώνυμη αντίδραση παρασκευής υδρογονανθράκων με την αντίδραση αλκυλαλογονιδίων με το μεταλλικό νάτριο.
Ο 'Αγγλος Edward Frankland (1825-1899), στην προσπάθειά του να απομονώσει οργανικές ρίζες (αλκύλια) αναφέρει το 1848 την πρώτη σύνθεση οργανομεταλλικής ένωσης (δηλ. ένωσης με απ' ευθείας δεσμό άνθρακα-μετάλλου), του διαιθυλο-ψευδαργύρου και αναγνωρίζει τις δυνατότητες εφαρμογής των οργανομεταλλικών ενώσεων αυτών στην οργανική σύνθεση, δυνατότητας που αργότερα φέρει στα όρια της τελειότητας ο Victor Grignard. Δικαιολογημένα ο Frankland θεωρείται ως ο "πατέρας της Οργανομεταλλικής Χημείας".


William Henry Perkin (1838-1907)
Παλαιό φιαλίδιο με στερεή μωβεΐνη και
φόρεμα βαμμένο με το χρώμα αυτό.
Σταθμός στην εφαρμοσμένη οργανική σύνθεση υπήρξε και το έτος 1856. Ο μόλις 18-χρονος τότε 'Αγγλος φοιτητής της Χημείας William Henry Perkin (1838-1907) στην προσπάθειά του να συνθέσει την περιζήτητη τότε κινίνη, οξείδωσε με διάλυμα διχρωμικού καλίου σε θειικό οξύ μίγμα διάφορων αρωματικών αμινών (ανιλίνες, τολουιδίνες). Διαπίστωσε ότι προέκυψε ένα σκουρόχρωμο προϊόν, που του λέρωσε τα γυάλινα σκεύη που χρησιμοποιούσε. Ο Perkin, προσπαθώντας να τα καθαρίσει με αλκοόλη, παρέλαβε ένα διάλυμα που μπορούσε εύκολα και ανεξίτηλα να βάψει μωβ μεταξωτά και άλλα υφάσματα. Το προϊόν αυτό υπήρξε το πρώτο συνθετικό οργανικό χρώμα, η μωβεΐνη (ή ιώδες της ανιλίνης). Αυτή ήταν η αρχή της βιομηχανικής παρασκευής οργανικών χρωμάτων που έμελλε να οδηγήσει σε βιομηχανίες χρωμάτων-κολοσσούς. 50 χρόνια μετά την "κατά λάθος" ανακάλυψη της μωβεΐνης, ήδη είχαν παρασκευασθεί 2000 συνθετικές χρωστικές ύλες.
Πολλοί υπήρξαν οι πρωτεργάτες πάνω στο νέο πεδίο της Χημείας, τη Φυσικοχημεία που ερμηνεύει χημικά φαινόμενα με καθιερωμένες γνώσεις από τη Φυσική και κυρίως από τη Θερμοδυναμική. Ο Αμερικανός χημικός, φυσικός και μαθηματικός Josiah Willard Gibbs (1839-1903) θεωρείται ο θεμελιωτής της Χημικής Θερμοδυναμικής. Ο Γάλλος Henri Louis Le Chatêlier (1850-1936) διατυπώνει περί τα τέλη του 19ου αιώνα την περίφημη αρχή του που διέπει κάθε χημική ισορροπία: "Εάν ένα χημικό σύστημα βρίσκεται σε ισορροπία, θα αντιδράσει σε κάθε αλλαγή συγκέντρωσης, θερμοκρασίας ή πίεσης κατά τρόπο που να ελαχιστοποιεί την αλλαγή αυτή".
Ο Ολλανδός οργανικός χημικός και φυσικοχημικός Jacobus Henricus van't Hoff (1852-1911) συνεισέφερε πολλά σε θέματα χημικής κινητικής και ισορροπίας. Το 1874 δημοσίευσε το βιβλίο με τίτλο "La chimie dans l' éspace" (η Χημεία στον χώρο), το οποίο θεωρείται η απαρχή της στερεοχημείας και όπου θεμελιώνεται η τετραεδρική δομή των κορεσμένων ενώσεων του άνθρακα, αν και αρχικά υπήρξε αντικείμενο σφοδρών επικρίσεων. Υπήρξε ο πρώτος επιστήμονας που τιμήθηκε το 1901 με το Nobel Χημείας για τις εργασίες σε θέματα χημικής δυναμικής και της ωσμωτικής πίεσης σε διαλύματα.
Στις αρχές του 20ου αιώνα, ο Γερμανός (από τη Λιθουανία) Wilhelm Ostwald (1853-1932) διατυπώνει τις θεωρίες του πάνω στη χημική ισορροπία, τη χημική κινητική και την κατάλυση και για το έργο του αυτό τιμήθηκε με το Nobel Χημείας του 1909.






Josiah Willard Gibbs
(1839-1903)
Henri Louis Le Chatêlier
(1850-1936)
Jacobus Henricus
van't Hoff (1852-1911)
Wilhelm Ostwald
(1853-1932)
Svante August Arrhenius
(1859-1927)
Walter Nernst
(1864-1941)
Το 1884, ο Σουηδός Svante August Arrhenius (1859-1927), στη διδακτορική διατριβή που υπέβαλε στο Πανεπιστήμιο της Ουψάλας, διατυπώνει τη θεωρία του για την ηλεκτρολυτική διάσταση, τον ιοντισμό και την ύπαρξη ιόντων. Η ιδέα του αυτή ήταν τόσο ριζοσπαστική για την εποχή της, που μόλις και κατάφερε να γίνει δεκτή η διατριβή του και μάλιστα με χαμηλό βαθμό. Σήμερα, η ηλεκτρολυτική διάσταση π.χ. των αλάτων σε διαλύματά τους αποτελεί κοινή γνώση, τότε όμως η ιδέα αυτή πολεμήθηκε σφοδρότατα.
Ο Arrhenious βρήκε ένθερμο υποστηρικτή της θεωρίας του στο πρόσωπο του Ostwald και αργότερα τιμήθηκε για αυτήν με το Nobel Χημείας του 1903 και στον van't Hoff, ο οποίος το 1889 απέδειξε πειραματικά την ορθότητα της θεωρίας της διάστασης των ηλεκτρολυτών.
Αυτό που ίσως δεν είναι ευρύτερα γνωστό για τον Arrhenious είναι το ότι πρώτος, ήδη από 1896, είχε προβλέψει ότι η καύση ορυκτών καυσίμων και η αύξηση του ατμοσφαιρικού CO2 θα οδηγήσει στο φαινόμενο της υπερθέρμανσης της ατμόσφαιρας του πλανήτη. Μάλιστα είχε υπολογίσει ότι διπλασιασμός της περιεκτικότητας της ατμόσφαιρας σε CO2 θα αυξήσει τη μέση θερμοκρασία της ατμόσφαιρας κατά 5ºC.
Ο Γερμανός φυσικοχημικός Walter Nernst (1864-1941), τιμήθηκε με το Nobel Χημείας του 1920 για τη θεωρία του πάνω στον 3ο θερμοδυναμικό νόμο (η εντροπία του τέλειου κρυστάλλου τείνει προς το μηδέν, όσο η θερμοκρασία του τείνει προς το απόλυτο μηδέν). Συνεισέφερε πολλά στη Φυσικοχημεία και είναι γενικότερα γνωστός για την περίφημη εξίσωση του, που είναι η βασική εξίσωση σε θέματα οξειδοαναγωγής και γενικότερα στον χώρο της Ηλεκτροχημείας.



John William Strutt, Λόρδος Rayleigh
(1842-1919)
William Ramsay
(1852-1916)
Σωλήνες ηλεκτρικής εκκένωσης με
διάφορα ευγενή αέρια.
Το 1896, ο 'Αγγλος φυσικός John William Strutt, Λόρδος Rayleigh (1842-1919) και ο Σκότος χημικός William Ramsay (1852-1916), διαπίστωσαν μια μικρή διαφορά στην πυκνότητα μεταξύ του αζώτου που λαμβάνεται με χημικές μεθόδους, σε σχέση με την πυκνότητα του αζώτου που λαμβάνεται από τον αέρα (μετά την απομάκρυνση του οξυγόνου και του διοξειδίου του άνθρακα). Το πρώτο ήταν μόλις κατά 0,5% ειδικώς ελαφρότερο από το δεύτερο. Με προσεκτικές μετρήσεις διαπίστωσαν ότι αυτή η μικρή διαφορά δεν ήταν κάτι το τυχαίο, αλλά εμφανιζόταν συστηματικά. Κατάλαβαν ότι η διαφορά αυτή οφειλόταν σε κάποιο άλλο συστατικό της ατμόσφαιρας, γεγονός που τους οδήγησε στην ανακάλυψη του αέριου στοιχείου αργόν.
Τα επόμενα 4-5 χρόνια ο Ramsey ανακάλυψε και τα υπόλοιπα ευγενή αέρια, δηλ. το νέον, το κρυπτόν, το ξένον, όπως και το ελαφρύτερο απ' όλα, το ήλιο, που ήταν ήδη γνωστή η παρουσία του στον ήλιο από φασματοσκοπικά δεδομένα. Ο Ramsey διαπίστωσε ότι τα αέρια αυτά ήταν χημικώς αδρανή και τα ονόμασε ευγενή αέρια. Αρκετά αργότερα, το 1910, απομόνωσε και το σχετικά βραχύβιο ραδιενεργό ευγενές αέριο, το ραδόνιο. O Rayleigh τιμήθηκε με το Nobel Φυσικής του 1904 gια τις μελέτες του πάνω στην πυκνότητα των αερίων και την ανακάλυψη του αργού. Με το Nobel Χημείας του ίδιου έτους τιμήθηκε ο Ramsey για την ανακάλυψη των ευγενών αερίων και την κατάταξή τους στον περιοδικό πίνακα.
Περίπου 60 χρόνια αργότερα διαπιστώθηκε ότι τα ευγενή αέρια δεν είναι και τόσο "ευγενή", όταν ο 'Αγγλος χημικός Neil Bartlett (1932-2008) διαπίστωσε ότι σχετικά εύκολα μπορούσαν να παρασκευαστούν φθοριούχες ενώσεις του ξένου. Σήμερα, είναι πλέον γνωστές ανάλογες ενώσεις του ραδονίου (σταθερότερες, αλλά βραχύβιες λόγω της ραδιενεργού διάσπασης του ραδονίου) και του κρυπτού (εξαιρετικά ασταθείς).
Ο Γερμανός χημικός Hermann Emil Fischer (1852-1919), τιμήθηκε με το Nobel Χημείας του 1902 για τη μεγάλη συνεισφορά στη χημεία των αμινοξέων, των πεπτιδίων και των πρωτεϊνών. Υπήρξε ο πρώτος που αναγνώρισε τη φύση του πεπτιδικού δεσμού, όπως και ο πρώτος που συνέθεσε πεπτίδια, φθάνοντας μέχρι και 18-πεπτίδιο, ένωση που έμοιαζε πλέον στις ιδιότητές της με πρωτεΐνη.


Η χημεία των αμινοξέων, πεπτιδίων και των πρωτεϊνών ξεκίνησε με τις ερευνητικές εργασίες του Hermann Emil Fischer
Hermann Emil Fischer
(1852-1919)
15. Συμβολή της Φυσικής στη Χημεία: Η Φύση των Ατόμων και του Χημικού Δεσμού
Κατά τα τέλη του 19ου αιώνα τα πράγματα είχαν φτάσει σε σημείο που δεν επαρκούσαν πλέον οι παρατηρήσεις και οι απλοί χημικοί στοιχειομετρικοί υπολογισμοί για να δώσουν την απάντηση στο θεμελιώδες ερώτημα: Πώς και γιατί συνδέονται τα άτομα και σχηματίζουν τις ενώσεις. 'Επρεπε πλέον να διευκρινιστεί πρώτα απ' όλα η φύση του ίδιου του ατόμου και η επιστήμη της Φυσικής είχε πλέον τα κατάλληλα εργαλεία και τους ανθρώπους που θα έδιναν τις απαντήσεις αυτές. Οι ανακαλύψεις στο θέμα αυτό άρχισαν να έρχονται με ραγδαίο ρυθμό.




Antoine Henri Becquerel (1852-1908)
Αμαύρωση φωτογραφικού φιλμ από τη ραδιενέργεια άλατος ουρανίου. Το περίγραμμα ενός χάλκινου σταυρού έδειξε ότι ορισμένα υλικά ήταν "αδιαφανή" ως προς την ακτινοβολία αυτή (περισσότερα).
Joseph John Thomson (1856-1940)
Ο σωλήνας Crookes με τον οποίο ο Thomson πραγματοποίησε τα πειράματά του (περισσότερα).
Η αρχή έγινε το 1896 με την ανακάλυψη της φυσικής ραδιενέργειας από τον Γάλλο φυσικό Antoine Henri Becquerel (1852-1908), όταν τυχαία διαπίστωσε ότι ενώσεις του ουρανίου προκαλούσαν αμαύρωση σε προστατευμένα από το φως φωτογραφικά φιλμ. 'Ηταν ήδη γνωστό ότι αντίστοιχο φαινόμενο μόνο οι ακτίνες Χ μπορούσαν να προκαλέσουν. Τιμήθηκε με το Nobel Φυσικής του 1903.

Ernst Rutherford
(1871-1937)

Hans Geiger
(1882-1945)

Ernest Marsden
(1889-1970)

Η εκτροπή ενός πολύ μικρού ποσοστού των α-σωματιδίων που προσπίπτουν σε ένα λεπτότατο φύλλο χρυσού (πάχους 0,4 μm), αποδεικνύει την παρουσία σημείων "πυκνού" θετικού φορτίου στο φύλλο, δηλαδή των πυρήνων των ατόμων χρυσού (περισσότερα).
Το 1897, ακολούθησε η ανακάλυψη του ηλεκτρονίου από τον 'Αγγλο φυσικό Joseph John Thomson (1856-1940), ως αποτέλεσμα των πειραμάτων που πραγματοποιούσε πάνω στην επίδραση του ηλεκτρικού πεδίου πάνω στις "καθοδικές ακτίνες" ενός σωλήνα Crookes. Η ανακάλυψη των ηλεκτρονίων προηγήθηκε περίπου 12 χρόνια της ανακάλυψης του πυρήνα. Ο Thomson τιμήθηκε για την ανακάλυψη αυτή με το Nobel Φυσικής του 1906. Οι ανακαλύψεις αυτές άρχισαν να αναδεικνύουν τη στενή συγγένεια μεταξύ των επιστημών της Φυσικής και της Χημείας.
Η Γαλλίδα (Πολωνικής καταγωγής) φυσικός και χημικός Marie Skłodowska Curie (1867-1934) υπήρξε η πρώτη γυναίκα που τιμήθηκε με το βραβείο Nobel. Είναι επίσης η μόνη γυναίκα που τιμήθηκε με δύο Nobel. Τo 1903, η Curie μοιράστηκε το Nobel Φυσικής με τον Becquerel για την ανακάλυψη της ραδιενέργειας και το 1911, τιμήθηκε με το Nobel Χημείας για την ανακάλυψη των στοιχείων ράδιο και πολώνιο. Στο πρόσωπο της Κιουρί αποδείχθηκε η άρρηκτη συγγένεια Φυσικής και Χημείας. Η Curie τιμήθηκε επίσης όταν το ραδιενεργό στοιχείο με ατομικό αριθμό 96 ονομάστηκε Κιούριο (Curium, Cm).
Το 1907, τιμήθηκε με το Nobel Φυσικής ο Ernst Rutherford (1871-1937) για την ανακάλυψη της διάσπασης των ραδιενεργών στοιχείων και ο οποίος θεωρείται σήμερα ο πατέρας της Πυρηνικής Φυσικής. 'Ετσι, η ουσιαστική φύση του ατόμου αποκαλύφθηκε από τα πειράματα των Thomson και Rutherford. Ο Rutherford τιμήθηκε επίσης όταν το ραδιενεργό στοιχείο με ατομικό αριθμό 104 ονομάστηκε Ραδεφόρντιο (Rutherfordium, Rf).
Το 1909, ο Αμερικανός φυσικός Robert Millikan (1868-1953), με το περίφημο πείραμα της "αιωρούμενης σταγόνας λαδιού", υπολογίζει με εξαιρετική ακρίβεια το ηλεκτρικό φορτίο του ηλεκτρονίου. Η τιμή που έδωσε ο Millikan ήταν μόλις 0,6% μικρότερη από τη σημερινή αποδεκτή τιμή (qe = 1.602176 x 10-19 C).



Robert Millikan
(1868-1953)
Henry Moseley
(1887-1915)
Niels Bohr
(1885-1962)
Το 1911, ο Αγγλο-Νεοζηλανδός χημικός και φυσικός Ernest Rutherford (1871-1937), ο Γερμανός φυσικός Hans Geiger (1882-1945), γνωστός από τον ανιχνευτή ραδιενέργειας που φέρει το όνομά του, και ο Αγγλο-Νεοζηλανδός φυσικός Ernest Marsden (1889-1970) ανακοινώνουν τα αποτελέσματα των πειραμάτων τους (το περίφημο πείραμα με το "φύλλο χρυσού") και επιβεβαιώνουν το ατομικό μοντέλο των ατόμων, με τον θετικά φορτισμένο μικροσκοπικό πυρήνα που περιβάλλεται από το αρνητικά φορτισμένο ηλεκτρονιακό νέφος.
Η ανακάλυψη της ύπαρξης πυρήνα στα άτομα κατέρριψε το λεγόμενο μοντέλο του σταφιδόψωμου (plum pudding) που προτάθηκε αρχικά από τον J. J. Thomson, σύμφωνα με το οποίο το άτομο ήταν μια θετικά φορτισμένη σφαίρα μέσα στην οποία κινούνταν τα αρνητικώς φορτισμένα ηλεκτρόνια. Τα άτομα πλέον άρχισαν να αποκτούν μορφή.
Το 1913, ο νέος 'Αγγλος χημικός Henry Moseley (1887-1915), εξετάζοντας τα φάσματα των ακτίνων Χ, που λάμβανε χρησιμοποιώντας διάφορα μεταλλικά στοιχεία ως στόχους, διαπίστωσε τη συστηματική μαθηματική σχέση μεταξύ του μήκους κύματος των ακτίνων Χ και ενός νέου χαρακτηριστικού του κάθε στοιχείου, του ατομικού αριθμού. 'Ετσι, έγινε γνωστό ότι κάθε στοιχείο, εκτός από το ατομικό βάρος, χαρακτηρίζεται και από τον ατομικό αριθμό. Από τα κενά στους ατομικούς αριθμός, προέβλεψε την ύπαρξη των στοιχείων άφνιο και ρήνιο λίγα χρόνια πριν την ανακάλυψή τους.
Το 1915, ο Moseley σε ηλικία μόλις 27 ετών, διέκοψε τις έρευνές του για να καταταγεί στον Βρετανικό στρατό. Λίγους μήνες αργότερα χάνει τη ζωή του πολεμώντας στη μάχη της Καλλίπολης κατά τον 1ο Παγκόσμιο Πόλεμο. Ο θάνατος στέρησε από τον ίδιο ένα βέβαιο Nobel και την επιστήμη από έναν εξαιρετικό επιστήμονα. Το γεγονός αυτό υπήρξε αφορμή να περάσει νόμος στην Βρετανία (και στη συνέχεια σε πολλά άλλα κράτη) που εξαιρούσε νέους λαμπρούς επιστήμονες από τη μάχιμη στρατιωτική υπηρεσία.
Τέλος, ο Δανός φυσικός Niels Bohr (1885-1962) για τη δομή των ατόμων έκανε ένα ακόμη σημαντικό βήμα ερμηνεύοντας τις γραμμές που παρουσιάζονται στο φάσμα εκπομπής του υδρογόνου και εισάγοντας την έννοια της τροχιάς των ηλεκτρονίων. Ο Bohr τιμήθηκε επίσης όταν το ραδιενεργό στοιχείο με ατομικό αριθμό 107 ονομάστηκε Μπόριο (Bohrium, Bh).




Φωτογραφίες της Marie Skłodowska Curie (1867-1934): 1η, 2η στο εργαστήριό της. 3η: Η Marie Curie και ο σύζυγός της, ο φυσικός Pierre Curie (1859-1906). 4η: Η Marie Curie και η κόρη της Irène Joliot-Curie (1897-1956), που με τον σύζυγό της Frederic Joliot-Curie (1900-1958) τιμήθηκαν με το Nobel Χημείας του 1935 για τις έρευνές τους στην τεχνητή ραδιενέργεια.


Mikhail Semyonovich Tsvet (1872-1919)
Σχηματική αναπαράσταση του πρώτου χρωματογραφικού διαχωρισμού του Tsvet
16. Σταθμοί στην Εξέλιξη της Χημείας κατά τον 20ο αιώνα
Ο 20ος αιώνας χαρακτηρίζεται από ραγδαία πορεία ανακαλύψεων τόσο για εφαρμογές στη χημική βιομηχανία, όσο και για το θεωρητικό υπόβαθρο της Χημείας. Την ίδια περίοδο ξεκινάει μία εκπληκτική πορεία ανακαλύψεων της κβαντικής χημείας, των νέων και ευαίσθητων αναλυτικών τεχνικών, της σύνθεσης πολύπλοκων οργανικών ενώσεων και πολυμερών που διαδραματίζουν σημαντική πρόοδο για την Χημεία.
Οι σημαντικότερες ανακαλύψεις στον τομέα της Χημείας και ορισμένες εμβληματικές ανακαλύψεις της φυσικής και της βιοχημείας παραθέτονται παρακάτω κατά χρονολογική σειρά:
16.1. Περίοδος 1900-1915
Το 1900, ο Γάλλος χημικός François Auguste Victor Grignard (1871-1932) ανακοινώνει μέθοδο σύνθεσης με τη βοήθεια οργανομαγνησιακών ενώσεων, που αποδείχθηκαν πολύ πιο εύχρηστες και ασφαλείς σε σχέση με άλλες δραστικές οργανομεταλλικές ενώσεις. Ο Grignard τιμήθηκε με το Nobel Χημείας του 1912.
Το 1903, ο Ρώσος βοτανολόγος Mikhail Semyonovich Tsvet (1872-1919), εξετάζοντας τις φυτικές χρωστικές ουσίες, ανακαλύπτει τη χρωματογραφία, μια εξαιρετικά χρήσιμη τεχνική τόσο για τον διαχωρισμό και ανάλυση πολύπλοκων χημικών μιγμάτων, όσο και για τον καθαρισμό χημικών ενώσεων.


Το φωτοηλεκτρονικό φαινόμενο ερμηνεύεται με την αποδοχή της σωματιδιακής φύσης του φωτός.
Το 1905, οι Γερμανοί χημικοί Fritz Haber (1868-1934) and Carl Bosch (1874-1940) αναπτύσσουν βιομηχανική μέθοδο παρασκευής αμμωνίας από το ατμοσφαιρικό άζωτο και υδρογόνο. Η μέθοδος αυτή έπαιξε ακρογωνιαίο ρόλο στην ανάπτυξη της χημικής βιομηχανίας και των λιπασμάτων για τη γεωργία, αλλά και των εκρηκτικών. Ο Haber τιμήθηκε με το Nobel Χημείας το 1918 και ο Bosch το 1931.
Το 1905, ο διάσημος Γερμανός φυσικός Albert Einstein (1879-1955) ερμηνεύει το φωτοηλεκτρικό φαινόμενο, δηλαδή την απόσπαση ηλεκτρονίων από την επιφάνεια μετάλλων (ιδιαίτερα έντονη στην περίπτωση των αλκαλίων), όταν αυτά δέχονται οπτική ακτινοβολία. Ο Einstein το ερμήνευσε κάνοντας δεκτή τη σωματιδιακή φύση του φωτός. Η λογική είναι απλή: Είναι αδύνατον η ενέργεια της οπτικής ακτινοβολίας "απλωμένη" (ως κύμα) σε όλη την φωτοευαίσθητη επιφάνεια ενός μετάλλου να επαρκεί, ώστε να επιτευχθεί η απόσπαση ηλεκτρονίου από τα επιμέρους άτομα, αφού η ενέργεια που δέχεται το κάθε άτομο είναι ελάχιστη. Αντίθετα, εάν η ενέργεια της ακτινοβολίας προσπίπτει στην επιφάνεια σε μορφή "πακέτων-βομβών", η απόσπαση αυτή καθίσταται ενεργειακά εφικτή για κάθε άτομο μετάλλου που δέχεται ένα ενεργειακό πακέτο, δηλ. το φωτόνιο. Για το έργο του αυτό τιμήθηκε με το Nobel Φυσικής του 1921. Ο Einstein τιμήθηκε επίσης όταν το ραδιενεργό στοιχείο με ατομικό αριθμό 99 ονομάστηκε Αϊνσταΐνιο (Einsteinium, Es).
Το 1907, ο Βέλγος χημικός Leo Hendrik Baekeland (1863-1944) ανακαλύπτει τον βακελίτη, πολυμερές προϊόν αντίδρασης φορμαλδεΰδης και φαινόλης, το πρώτο εμπορικά διαθέσιμο πλαστικό. Τα πολυμερή παύουν να θεωρούνται μόνο ενοχλητικά παραπροϊόντα της οργανικής σύνθεσης, αλλά προϊόντα με πολύτιμές ιδιότητες και πλήθος εφαρμογών. 'Εναρξη της Χημείας των Πολυμερών.
Το 1909, ο Δανός χημικός Søren Peder Lauritz Sørensen (1868-1939) προτείνει την έννοια του pH για τον χαρακτηρισμό της οξύτητας διαλυμάτων, όπως και δύο μεθόδους μέτρησής του: με τη βοήθεια έγχρωμων δεικτών και με ηλεκτροχημικά μέσα.






Victor Grignard
(1871-1932)
Leo Hendrik Baekeland (1863-1944)
William Henry Bragg
(1862-1942)
William Lawrence Bragg (1890-1971)
Peter Debye
(1884-1966)
Frederick Soddy
(1877-1956)
Το 1912, ο Βρετανός φυσικός και χημικός William Henry Bragg (1862-1942) και ο γιος του φυσικός William Lawrence Bragg (1890-1971) παρουσιάζουν την κρυσταλλογραφία ακτίνων-Χ, ένα σπουδαίο εργαλείο για τον προσδιορισμό της δομής κρυσταλλικών χημικών ενώσεων και διατυπώνουν τον περίφημο νόμο του Bragg (διάθλαση ακτίνων Χ από τους κρυστάλλους) πάνω στον οποίο βασίζεται η πανίσχυρη αυτή τεχνική. Για την εργασία τους τιμήθηκαν με το Nobel Φυσικής του 1915.
Την ίδια χρονιά, ο Ολλανδός φυσικοχημικός Peter Debye (1884-1966) ανακοινώνει τη θεωρία του για το μοριακό δίπολο και τη διπολική ροπή, για να περιγράψει την κατανομή των ηλεκτρικών φορτίων σε ασύμμετρα μόρια, που ευνοεί ορισμένες διπολικές έλξεις και διαμοριακές δυνάμεις, όπως ο δεσμός υδρογόνου. Προς τιμήν του, η διπολική ροπή ενός μορίου εκφράζεται σε μονάδες debye (D). O Debye τιμήθηκε με το Nobel Χημείας του 1936 για τις μελέτες του στις μοριακές δομές.
Το 1913, ο 'Αγγλος ραδιοχημικός Frederick Soddy (1877-1956) εξετάζοντας τα προϊόντα διάσπασης του ουρανίου προτείνει την ιδέα ότι ένα ραδιενεργό στοιχείο μπορεί να έχει περισσότερες από μία ατομικές μάζες και πρότεινε τον όρο "ισότοπο". Ισότοπα βέβαια έχουν και τα μη ραδιενεργά στοιχεία. Ο Soddy τιμήθηκε με το Nobel Χημείας του 1921.
Την ίδια χρονιά, ο 'Αγγλος φυσικός Joseph John Thomson (1856-1940) (γνωστότερος ως "J-J Thomson") εφαρμόζει τις γενικές θεωρίες περί θετικά φορτισμένων σωματιδίων που προκύπτουν από τον βομβαρδισμό με ταχύτατα ηλεκτρόνια και μπορούν να διαχωριστούν με βάση τον λόγο μάζας προς φορτίο (m/z). Τα πειράματά του οδήγησαν στην ανακάλυψη της φασματομετρίας μαζών. Ο Thomson τιμήθηκε με το Nobel Φυσικής του 1906 για τις εργασίες πάνω στην αγωγιμότητα των αερίων.




O Δανός Søren Sørensen (1868-1939) πρότεινε το 1909 την κλίμακα pH για τον χαρακτηρισμό της οξύτητας υδατικών διαλυμάτων. Ο προσδιορισμός του pH (στην περίπτωση άχρωμων διαλυμάτων) μπορεί να πραγματοποιηθεί με περιορισμένη ακρίβεια με τη βοήθεια οξεοβασικών δεικτών ή (ακριβέστερα) με ηλεκτροχημικές μετρήσεις. Σήμερα πραγματοποιείται σχεδόν αποκλειστικά ποτενσιομετρικά με τη βοήθεια του ονομαζόμενου "ηλεκτροδίου υάλου" και πεχαμέτρου.
16.2. Περίοδος 1916-1935
Κατά την περίοδο 1916-1923 ο Αμερικανός χημικός Gilbert N. Lewis (1875-1946) δημοσιεύει το πρωτοποριακό βιβλίο του "Το 'Ατομο και το Μόριο" (The Atom and the Molecule), που θέτει τα θεμέλια για τη θεωρία του χημικού δεσμού, ενώ το 1923 με τον Merle Randall (1888-1950) δημοσιεύουν το βιβλίο τους "Θερμοδυναμική και η Ελεύθερη Ενέργεια των Χημικών Ενώσεων" (Thermodynamics and the Free Energy of Chemical Substances), που αποτελεί το πρώτο κλασικό βιβλίο Χημική Θερμοδυναμικής. Το 1923 ο Lewis αναπτύσσει τη θεωρία περί οξέων και βάσεων με βάση την ηλεκτρονιακή δομή των χημικών ενώσεων.
Οι Irving Langmuir (1881-1957), Nobel Χημείας του 1932, και ο διάσημος Αμερικανός χημικός Linus Pauling (1901-1994), Nobel Χημείας του 1954 και Nobel Ειρήνης του 1962, προώθησαν τις ηλεκτρονιακές θεωρίες για τους χημικούς δεσμούς, το σθένος των στοιχείων και τα μοριακά τροχιακά.






Gilbert N. Lewis
(1875-1946)
Louis de Broglie
(1892-1987)
Erwin Schrödinger
(1887-1961)
Fritz London
(1900-1954)
Wallace Carothers
(1896-1937)
Erich Hückel
(1896-1980)
Η περίοδος 1924-1926 είναι ιδιαίτερα σημαντική για την Κβαντική Φυσική και Χημεία. Ο νεαρός Γάλλος φυσικός Louis de Broglie (1892-1987), Nobel Φυσικής του 1929, προτείνει την επαναστατική άποψη για την εποχή εκείνη, περί της κυματικής φύσης του ηλεκτρονίου, και αναπτύσσει την αντίληψη της δυαδική φύσης της ακτινοβολίας. Αργότερα, ο Αυστριακός Erwin Schrödinger (1887-1961) προτείνει την περίφημη εξίσωσή του, που αποτελεί τη μαθηματική θεμελίωση για την κυματική φύση της ατομικής δομής της ύλης. Ο Schrödinger τιμήθηκε με το Nobel Φυσικής του 1933.
Το 1927, οι Γερμανοί θεωρητικοί φυσικοί Fritz London (1900-1954) and Walter Heitler (1904-1981) εφαρμόζουν τις αρχές της νεοδιατυπωθείσας θεωρίας της κβαντομηχανικής για να ερμηνεύσουν τον ομοιοπολικό δεσμό στο μόριο του υδρογόνου, όπως και τις ενδομοριακές και διαμοριακές δυνάμεις (δυνάμεις London). Με τον τρόπο αυτό εγκαινιάσθηκε η γέννηση της Κβαντικής Χημείας.


Η πρώτη ένδειξη ύπαρξης του δευτερίου. Αριστερά από μια γραμμή Balmer του Η (πάνω από το βέλος) διακρίνεται η ασθενής γραμμή του D σε δείγμα φυσικού υδρογόνου ελαφρά εμπλουτισμένου σε D, που προέκυψε με εξάτμιση του υγροποιημένου αερίου (βλ. Χημική 'Ενωση του μήνα: Βαρύ ύδωρ).
Harold Clayton Urey
(1883-1981)
Το 1930, ο Linus Pauling (1901-1994) σε μια επιπλέον μεγάλη του συνεισφορά στη Χημεία προτείνει τους βασικούς κανόνες για τη χρήση της κρυσταλλογραφίας ακτίνων Χ στη μελέτη των χημικών δομών.
Το 1930, ο Αμερικανός χημικός της πολυεθνικής εταιρείας DuPont, ο Wallace Carothers (1896-1937) ανακαλύπτει το νάϋλον (nylon), το πολυμερές που έφερε επαναστατικές αλλαγές στα χημικά συνθετικά υλικά και το εμπορικά επιτυχέστερο προϊόν της χημικής βιομηχανίας.
Το 1931, ο Γερμανός φυσικοχημικός Erich Hückel(1896-1980) προτείνει τον κανόνα Hückel (4n +2), με τον οποίο προβλέπεται πότε ένα μονοκυκλικό, επίπεδο και με συζυγιακούς δεσμούς μόριο (με ένα τροχιακό p σε κάθε άτομο) έχει αρωματικό χαρακτήρα (όπου το n είναι ακέραιος αριθμός).
Το 1931, ο Αμερικανός χημικός Harold Clayton Urey (1883-1981) ανακαλύπτει το δευτέριο (deuterium, D), εξετάζοντας φασματοσκοπικά το συμπύκνωμα από τη σταδιακή εξάτμιση του υγρού υδρογόνου. Για την ανακάλυψη αυτή τιμήθηκε με το Nobel Χημείας του 1934 (βλ. Χημική 'Ενωση του μήνα: Βαρύ ύδωρ).
Το 1932, ο 'Αγγλος φυσικός James Chadwick (1891-1974) ανακαλύπτει το νετρόνιο. Για την ανακάλυψη αυτή τιμήθηκε με το Nobel Φυσικής του 1935. Ολοκληρώνεται πλέον η γνώση της βασική δομής των ατόμων.
Κατά την περίοδο 1932-1934 οι χημικοί Linus Pauling και Robert Mulliken (1896-1986, Nobel Χημείας του 1966) παρουσιάζουν μια ποσοτική θεώρηση της ηλεκτροαρνητικότητας των στοιχείων και διατυπώνουν μια κλίμακα ηλεκτροαρνητικότητας που φέρει το όνομά τους.


Glenn T. Seaborg (1912-1999)
Η πρώτη ορατή ποσότητα ένωσης του αμερικίου
(λίγα μg Am(OH)3).
16.3. Περίοδος 1936-1960
Το 1937 υπήρξε μια ιδιαίτερα αποδοτική χρονιά για την πετροχημική βιομηχανία. Ο Γάλλος χημικός μηχανικός Eugene Houdry (1892-1962) αναπτύσσει με επιτυχία μέθοδο κλασματικής καταλυτικής απόσταξης (διύλιση πετρελαίου, καταλυτική πυρόλυση). Οι τεχνική αυτή οδηγεί στη ραγδαία ανάπτυξη της πετροχημικής βιομηχανίας πετρελαίου και στην παρασκευή υψηλής ποιότητας καυσίμων για τροχοφόρα.
Το 1939, ο διάσημος Αμερικανός χημικός Linus Pauling (1901-1994) δημοσιεύει το πρωτοποριακό βιβλίο "Η Φύση του Χημικού Δεσμού" (The Nature of the Chemical Bond). Είναι ένα από τα σημαντικότερα συγγράμματα Χημείας, τόσο για τη φύση του ομοιοπολικού χημικού δεσμού, όσο και για τη θεωρία της υβριδοποίησης τροχιακών και τη θεωρία του συντονισμού, μέσω της ηλεκτραρνητικότητας των στοιχείων.
Το 1941, ο Αμερικανός χημικός Glenn T. Seaborg (1912-1999) με τη μέθοδο της δέσμευσης νετρονίων σε πυρηνικές αντιδράσεις κατάφερε να δημιουργήσει και να απομονώσει 9 στοιχεία που ανήκουν στα υπερουράνια στοιχεία, όπως και δεκάδες ισοτόπων. Το 1940 το πλουτώνιο (Pu) και στο διάστημα 1944-1958 το αμερίκιο (Am), το κιούριο (Cm), το μπερκέλιο (Bk), το καλιφόρνιο (Cf), το αϊνσταΐνιο (Es), το φέρμιο (Fm), το μεντελέβιο (Md) και το νομπέλιο (No).
Ο Seaborg υπήρξε ισχυρή επιστημονική φυσιογνωμία με τις πολυάριθμες ανακαλύψεις του στον τομέα των πυρηνικών καυσίμων και επιστημονικός σύμβουλος πολλών αμερικανών προέδρων. Για την ανακάλυψη των υπερουράνιων στοιχείων και τη μελέτη της χημείας τους ο Seaborg τιμήθηκε με Nobel Χημείας του 1935, το οποίο μοιράσθηκε με τον Αμερικανό φυσικό Edwin Mattison McMillan (1907-1991). Ο Seaborg τιμήθηκε επίσης όταν το ραδιενεργό στοιχείο με ατομικό αριθμό 106 ονομάστηκε Σιμπόργκιο (Seaborgium, Sg). Στο διαδίκτυο υπάρχει μια ωραία συλλογή άρθρων του Seaborg σχετικών με την ανακάλυψη και απομόνωση των υπερουράνιων στοιχείων.
Κατά τη διετία 1945-1946, o Ελβετός φυσικός Felix Bloch (1905-1983) και ο Αμερικανός φυσικός Edward Mills Purcell (1912-1997) ανακαλύπτουν τον Πυρηνικό Μαγνητικό Συντονισμό (Nuclear Magnetic Resonance, NMR), μια σημαντικότατη φασματοσκοπική τεχνική για τον προσδιορισμό της δομής οργανικών ενώσεων. Οι Bloch και Purcell τιμήθηκαν για την ανακάλυψή τους με το Nobel Φυσικής του 1952. Το 1954, ο Bloch υπήρξε ο πρώτος Γενικός Διευθυντής του Κέντρου Πυρηνικών Μελετών και Ερευνών (CERN) στη Γενεύη.




Felix Bloch
(1905-1983)
Edward Mills Purcell
(1912-1997)
'Ενα από τα πρώτα συστήματα NMR
(συνεχούς κύματος, 40 MHz) του 1961
Σύγχρονο σύστημα NMR (800 MHz) που χρησιμοποιείται σε δομικές μελέτες πρωτεϊνών
Το 1951, ο Linus Pauling (1901-1994) εξέτασε τη δυνατότητα χρήσης της φασματοσκοπίας των ακτίνων Χ για τον προσδιορισμό της δομής των πρωτεϊνών στον χώρο. Η δυνατότητα προσδιορισμού της δομής των πρωτεϊνών υπήρξε ανακάλυψη πρωταρχικής σημασίας για την κατανόηση της δράσης των ενζύμων και του ρόλου τους στα βιολογικά συστήματα. Για αυτήν την πρωτοποριακή έρευνα τιμήθηκε με το Nobel Χημείας του 1954.


Linus Pauling
(1901-1994)
Για την επιστημονική πολυπραγμοσύνη του Pauling και την εν γένει προσφορά του στην Επιστήμη και την Ανθρωπότητα, μπορεί να αναζητηθεί άφθονο υλικό στο διαδίκτυο, όπως ο ιστότοπος αυτός.
Θα πρέπει να σημειωθεί ότι η επιστημονική κοινότητα "όφειλε" στον Pauling το Nobel για δεκαετίες. Ενώ εμφανιζόταν συνεχώς ως υποψήφιος για το βραβείο, έβλεπε νεότερούς του επιστήμονες, να βραβεύονται ακόμη και για μικρότερης σημασίας επιστημονικά επιτεύγματα. Ουσιαστικά, το Nobel που έλαβε τελικά το 1954 δεν αφορούσε αυτή τη συγκεκριμένη ερευνητική ανακάλυψη, αλλά επιβράβευε μια ολόκληρη ζωή συνεχούς προσφοράς στην Επιστήμη της Χημείας σε πολλούς τομείς.
Ο Pauling υπήρξε ο μόνος επιστήμονας που τιμήθηκε με δεύτερο Nobel, που δεν είχε σχέση με τις Φυσικές Επιστήμες. Το 1963 τιμήθηκε με το Nobel Ειρήνης για την επιτυχή εκστρατεία του για την κατάργηση των πυρηνικών δοκιμών στην ατμόσφαιρα. Ο φιλειρηνικός ακτιβισμός του Pauling του είχε στοιχίσει τη στέρηση του διαβατηρίου του από το Υπουργείο Εξωτερικών των ΗΠΑ (1952), το οποίο του απεδόθη λίγο αργότερα, όταν χρειάστηκε να μεταβεί στη Σουηδία για την παραλαβή του πρώτου του βραβείου Nobel.
Το 1944, ο Αμερικανός χημικός Robert Burns Woodward (1917-1979) με τον συνεργάτη του William von Eggers Doering (1917-2011) ανακοίνωσαν τη σύνθεση της κινίνης, γεγονός που για εκείνη την εποχή ήταν μεγάλο επίτευγμα οργανικής σύνθεσης. Τη δεκαετία του 1940, στο εργαστήριο του Woodward συνέθεσαν σημαντικές οργανικές ενώσεις, όπως η χοληστερόλη, η κορτιζόνη, η στρυχνίνη, το λυσεργικό οξύ, η ρεσερπίνη και άλλα φυσικά προϊόντα με αρκετά πολύπλοκη μοριακή δομή. Στην αρχή της δεκαετίας του 1960 ο Woodward και συνεργάτες συνέθεσαν με πολυάριθμα στάδια το εξαιρετικά πολύπλοκο μόριο της Βιταμίνης Β12. Ο Woodward τιμήθηκε για το πολύπλευρο συνθετικό του έργο με το Nobel Χημείας του 1965.
Το 1952 ο Robert Burns Woodward (1917-1979), ο 'Αγγλος χημικός Geoffrey Wilkinson (1921-1996) και ο Γερμανός χημικός Ernst Otto Fischer (1918-2007) διευκρίνισαν τη δομή του φερροκενίου και καθιέρωσαν την Οργανομεταλλική Χημεία ως ιδιαίτερο κλάδο της Χημείας. Οι Geoffrey Wilkinson και Ernst Otto Fischer τιμήθηκαν το 1973 με το Nobel Χημείας για τις ανακαλύψεις τους, που συνέβαλαν στην αλματώδη ανάπτυξη της Οργανομεταλλικής Χημείας.

Robert Burns Woodward (1917-1979)

Geoffrey Wilkinson
(1921-1996)

Ernst Otto Fischer
(1918-2007)


Η σύνθεση και στη συνέχεια η διευκρίνιση της δομής του φερροκενίου (η πρώτη γνωστή ένωση "σάντουιτς") κατά τη δεκαετία του 1950, έδωσε σημαντική ώθηση στο πεδίο της Οργανομεταλλικής Χημείας (βλ. Χημική ένωση του μήνα: φερροκένιο).
Το 1953 υπήρξε μια ιδιαίτερα σημαντική χρονιά για την επιστήμη. Οι Αμερικάνος βιολόγος James Watson (1928), ο 'Αγγλος βιοφυσικός Francis Crick (1916-2004), ο Νεοζηλανδός βιολόγος Maurice Wilkins (1916-2004) και η Αγγλίδα βιοφυσικός Rosalind Franklin (1920-1958) με την τριπλή δημοσίευση των ερευνητικών τους εργασιών στο περιοδικό Nature πρότειναν τη δομή της διπλής έλικας για το μόριο του DNA (δυο αλληλοσυγκρατούμενοι πολυνουκλεοτιδικοί κλώνοι). Η ανακάλυψη αυτή θεωρήθηκε εξαιρετικά σημαντική για την κατανόηση της κληρονομικότητας. 'Ετσι, έγινε κατανοητό πλέον ότι οι γενετικές πληροφορίες ενός οργανισμού αποθηκεύονται στην αλυσίδα του μορίου DNA, υπό τη μορφή της αλληλουχίας των δεοξυριβονουκλεοτιδίων. Αυτό ονομάσθηκε "κεντρικό δόγμα της μοριακής γενετικής". Οι Watson, Crick και Wilkins τιμήθηκαν με το Nobel Ιατρικής και Φυσιολογίας του 1963.





James Watson
(1928)
Francis Crick
(1916-2004)
Maurice Wilkins
(1916-2004)
Rosalind Franklin
(1920-1958)
Το 1953, ο Αμερικανός χημικός και βιολόγος Stanley Miller (1930-2007) και Harold Clayton Urey (που είχε ανακαλύψει το δευτέριο) στο Πανεπιστήμιο του Σικάγου έκαναν ένα πρωτοποριακό πείραμα για τη σύνθεση οργανικών ενώσεων σε προβιοτικές συνθήκες. Ο βομβαρδισμός με ηλεκτρικές εκκενώσεις μίγματος αερίων CH4, NH3, H2 και υδρατμών, δηλ. σε συνθήκες που προσομοίαζαν εκείνες της αρχέγονης ατμόσφαιρας της Γης, έδωσε έναν "ζωμό" που περιείχε μια ποικιλία αμινοξέων και άλλων οργανικών ουσιών, πρόδρομων ενώσεων μορίων βιολογικής σημασίας (πρωτεϊνών, DNA). Το πείραμα των Miller-Urey περιγράφεται στις εισαγωγικές σελίδες σχεδόν κάθε βιβλίου Βιοχημείας και αποτέλεσε ένα σημαντικό βήμα στην αναζήτηση μιας τεκμηριωμένης θεωρία ως προς την προέλευση της ζωής στον πλανήτη Γη πριν από 3,5-4 δισεκατομμύρια χρόνια.




O Stanley Miller (1930-2007) και η περίφημη πειραματική διάταξη προσομοίωσης της αρχέγονης ατμόσφαιρας της Γης.
Ο Frederick Sanger (1918) και το μόριο της ινσουλίνης στο οποίο προσδιόρισε την αλληλουχία των αμινοξέων.
Κατά την περίοδο 1951-1953 ο 'Αγγλος βιοχημικός Frederick Sanger (1918) βρήκε τρόπο προσδιορισμού της αλληλουχίας των αμινοξέων της ινσουλίνης (βλ. Χημική ένωση του μήνα: Ινσουλίνη), που αποτελείται από δύο πεπτιδικές αλυσίδες συνδεόμενες με δύο δισουλφιδικές γέφυρες. Ο Sanger τιμήθηκε για την ανακάλυψή του αυτή με το Nobel Χημείας του 1958. Το 1980 ο Sanger μαζί με τον Αμερικανό βιοχημικό, φυσικό και μοριακό βιολόγο Walter Gilbert (1932) μοιράσθηκαν το Nobel Χημείας για τη συμβολή τους στον προσδιορισμό της ακολουθίας των νουκλεϊνικών βάσεων στα νουκλεϊνικά οξέα (DNA), ενώ το άλλο μισό του βραβείου απονεμήθηκε στον Paul Berg (1926) για τις βασικές βιοχημικές έρευνες στον τομέα των νουκλεϊνικών οξέων και ιδιαίτερα του ανασυνδυασμένου DNA.



Karl Waldemar Ziegler
(1898-1973)
Giulio Natta
(1903-1979)
Με τους καταλύτες Ziegler-Natta (εδώ μεταλλοκένιο Ti ή Zr), ελέγχεται ο βαθμός πολυμερισμού των α-ολεφινών και η στερεο- χημεία του λαμβανόμενου πολυμερούς.
Η δεκαετία του 1950-1960 συνέβη μια ανακάλυψη ιδιαίτερα μεγάλης επιστημονικής και οικονομικής σημασίας για τη βιομηχανία των πολυμερών. Ο Γερμανός χημικός Karl Waldemar Ziegler (1898-1973), σε συνεργασία με τον Ιταλό χημικό μηχανικό Giulio Natta (1903-1979), βρήκαν τους περίφημους καταλύτες, γνωστούς πλέον ως καταλύτες Zigler-Natta. Με τους καταλύτες αυτούς (οργανομεταλλικές ενώσεις του αργιλίου, του τιτανίου και ζιρκονίου) μπορούσαν να ελέγξουν τον πολυμερισμό α-ολεφινών (και κυρίως του αιθυλενίου και του προπυλενίου) για σχηματισμό πολυμερών καθορισμένης περιοχής μοριακού βάρους και στερεοχημείας (τακτικότητας). Για την ανακάλυψή τους αυτοί οι Ziegler και Natta τιμήθηκαν με το Nobel Χημείας του 1963.
16.4. Περίοδος 1961-1995
Το 1962 ο Αμερικανός βιοχημικός Robert Bruce Merrifield (1921-2006), καθηγητής στο Ινστιτούτο Ροκφέλλερ, Νέα Υόρκη, ανακοίνωσε για πρώτη φορά την ανακάλυψη της αυτοματοποιημένης πεπτιδικής σύνθεσης (σύνθεση στερεάς φάσης κατά Merrifield) σε υπόστρωμα πολυστυρενίου, που απλούστευσε κατά πολύ την παρασκευή πεπτιδίων. Ο Merrifield τιμήθηκε με το Nobel Χημείας του 1984.
Κατά την περίοδο 1953-1960, στα Πανεπιστήμια του Καίμπριτζ και της Οξφόρδης, ο Αυστριακής καταγωγής Βρετανός μοριακός βιολόγος Max Perutz (1914-2002) και ο 'Αγγλος χημικός John Kendrew (1917-1997) πραγματοποιούν μελέτες σφαιρικών πρωτεϊνών με ακτίνες-Χ. Είναι η "χρυσή περίοδος" της μελέτης των πρωτεϊνικών κρυστάλλων μεγάλης σημασίας βιολογικών μορίων σε ερευνητικά εργαστήρια. Οι δύο επιστήμονες επιβραβεύονται με το Nobel Χημείας του 1962 για τη εξακρίβωση της τρισδιάστατης δομής της αιμοσφαιρίνης και της μυοσφαιρίνης.
Το 1962, ο 'Αγγλος χημικός Neil Bartlett (1932-2008) στο πανεπιστήμιο Berkeley της Καλιφόρνιας συνέθεσε για πρώτη φορά φθοριωμένες ενώσεις ευγενών αερίων, που μέχρι τότε θεωρούσαν ότι ήταν τελείως αδρανή. Αρχικά συνέθεσε την ένωση εξαφθορολευκοχρυσικό ξένον, Xe+[PtF6]- και στη συνέχεια φθοριωμένες ενώσεις ξένου (XeF2, XeF4 και XeF6). Ακολούθησαν η σύνθεση του οξειδίου του ξένου(VI), του υπερξενικού οξέος (H4XeO6) και αλάτων του.

Robert Bruce Merrifield
(1921-2006)

Μια από τις πειραματικές διατάξεις που χρησιμοποίησε ο Merrifield για την αυτοματοποιημένη σύνθεση πεπτιδίων.

Neil Bartlett
(1932-2008)

Τη δεκαετία του 1960 προκάλεσε έκπληξη η σύνθεση των πρώτων σταθερών ενώσεων του ευγενούς αερίου ξένον. Σήμερα, πολλές από τις ενώσεις αυτές είναι εμπορικά διαθέσιμες (στη φωτογραφία φιάλες με XeF2)
Το ίδιο έτος, o Ούγγρος χημικός George Andrew Olah (1927) ανακαλύπτει τρόπο παρασκευής και σταθεροποίησης των καρβοκατιόντων μέσω αντιδράσεων υδρογονανθράκων με σουπεροξέα, όπως το περίφημο "μαγικό οξύ" (μίγμα SbF5 - HSO3F), τα οποία χαρακτηρίζονται από μια ισχυρότατη πρωτονιοδοτική ικανότητα. Ο Olah βραβεύθηκε για τη σημαντική του συμβολή στη χημεία των καρβοκατιόντων και των αντιδράσεων τους με το Nobel Χημείας του 1994 (βλ. Χημική ένωση του μήνα: Μαγικό οξύ).
Το 1964, η Βρετανίδα χημικός Dorothy Mary Crowfood-Hodgkin (1910-1994) τιμήθηκε με το Nobel Χημείας για τις πολυετείς έρευνές της πάνω στην εξακρίβωση της τριτογενούς δομής πρωτεϊνών με κρυσταλλογραφία ακτίνων Χ. Η Hodgkin, με κρυσταλλογραφία ακτίνων Χ, συνέβαλε στη μελέτη της ινσουλίνης, πενικιλίνης και της βιταμίνης Β12.




Max Perutz
(1914-2002)
John Kendrew
(1917-1997)
George Andrew Olah
(1927)
Dorothy Mary Crowfood-Hodgkin (1910-1994)
Το 1964, ο Ελβετός φυσικοχημικός Richard Robert Ernst (1933) πρότεινε την εφαρμογή του Ταχέος Μετασχηματισμού Fourier (Fast Fourier Transform, FFT) στη φασματοσκοπία του Πυρηνικού Μαγνητικού Συντονισμού (NMR). Με την εφαρμογή σύντομων και ισχυρών παλμών κατά τη λήψη του φάσματος, αντί της συνεχούς σάρωσης, βελτιώνεται η ευαισθησία της λήψης του φάσματος και με μαθηματική επεξεργασία του λαμβανόμενου σήματος (σήμα ως προς χρόνο) λαμβάνεται το φάσμα NMR (σήμα ως προς συχνότητα). Η μέθοδος αργότερα βρήκε σημαντική εφαρμογή στο NMR δύο διαστάσεων (2D-NMR) και της απεικόνισης μαγνητικού συντονισμού, γνωστότερης ως Μαγνητική Τομογραφία (Magnetic Resonance Imaging, MRI) με εφαρμογές στην ιατρική διάγνωση ασθενειών. Ο Ernst τιμήθηκε με το Nobel Χημείας του 1991.
Το 1965, οι Αμερικανοί χημικοί Robert Burns Woodward (1917-1979) και Roald Hoffmann (1937) πρότειναν τους κανόνες Woodward-Hoffmann (rules), οι οποίοι χρησιμοποιούν τη συμμετρία των μοριακών τροχιακών για να ερμηνεύσουν τη στερεοχημεία των χημικών αντιδράσεων και ιδιαίτερα των περικυκλικών αντιδράσεων. Οι Roald Hoffman και ο Ιάπωνας χημικός Kenichi Fukui (1918-1998), ο οποίος εισήγαγε μια απλοποιημένη προσέγγιση στα μοριακά τροχιακά για τις περικυκλικές αντιδράσεις με την εξέταση των μετωπικών τροχιακών, HOMO και LUMO, τιμήθηκαν για τις ανακαλύψεις στον τομέα των μοριακών τροχιακών με το Nobel Χημείας του 1981.
Κατά τις δεκαετίες 1950, 1960 και 1970 ένα από τα πιο διάσημα εργαστήρια οργανικών συνθέσεων και ανακάλυψης νέων συνθετικών μεθόδων υπήρξε το εργαστήριο του Elias James Corey (1928) στο Πανεπιστήμιο Harvard. Η ομάδα του εργαστηρίου Corey, στην οποία εργάστηκαν πολυάριθμοι χημικοί, υπήρξε εξαιρετικά δραστήρια. Στο εργαστήριο αυτό αναπτύχθηκαν περισσότερες από 300 συνθετικές μέθοδοι και πραγματοποιήθηκαν περισσότερες από 300 ολικές συνθέσεις πολύπλοκων οργανικών ενώσεων. Ο Corey ανέπτυξε τη μεθοδολογία της ρετροσυνθετικής ανάλυσης στη χημική σύνθεση. Το 1989, οι Corey EJ και Chen X-M δημοσίευσαν το σημαντικό βιβλίο "The Logic of Chemical Synthesis", που αποτελεί σταθμό στην οργανική σύνθεση. Ο Corey τιμήθηκε με το Nobel Χημείας του 1990, για την ανάπτυξη της ρετροσυνθετικής ανάλυσης.
Το 1971, ο Γάλλος χημικός Yves Chauvin (1930) ερμηνεύει τον μηχανισμό της ολεφινικής μετάθεσης, δηλαδή ενός είδους ανακατανομής των θραυσμάτων αλκυλενίου κατά τη σχάση του διπλού δεσμού άνθρακα-άνθρακα σε ολεφίνες. Η ανακάλυψη έπαιξε σημαντικό ρόλο στην έρευνα της οργανικής σύνθεσης και στη Βιομηχανική Χημεία (πετρέλαια, φάρμακα, πολυμερή). Ο Chauvin μαζί με τους Richard R. Schrock (1945) και Robert H. Grubbs (1942) τιμήθηκαν για τη συμβολή τους στο πεδίο της ολεφινικής μετάθεσης με το Nobel Χημείας του 2005.






Richard Robert Ernst
(1933)
Roald Hoffmann
(1937)
Kenichi Fukui
(1918-1998)
Elias James Corey
(1928)
Yves Chauvin
(1930)
Karl Barry Sharpless
(1941)
To 1975, ο Αμερικανός χημικός Karl Barry Sharpless (1941) και οι συνεργάτες τους ανακάλυψαν τις αντιδράσεις της στερεοεκλεκτικής οξείδωσης, συμπεριλαμβανομένης της εποξείδωσης Sharpless, της ασυμμετρικής διϋδροξυλίωσης και οξυαμίνωσης Sharpless. To 2001 τιμήθηκε με Nobel Χημείας για τη συμβολή του στην ανακάλυψη των στερεοεκλεκτικών αντιδράσεων.
Το 1985, η επιστημονική κοινότητα εξεπλάγη όταν ο Βρετανός χημικός Harold Kroto (1939), ο Αμερικανός χημικός Robert Curl (1933) και ο Αμερικάνος χημικός, φυσικός και αστρονόμος Richard Smalley (1943-2005) ανακάλυψαν τα φουλερένια, μια άγνωστη μέχρι τότε μορφή άνθρακα, όπου τα άτομα είναι συνδεμένα μεταξύ τους κατά τρόπο που να σχηματίζονται μόρια με τη μορφή μπάλας, με επιφάνειες αποτελούμενες από πενταμελείς ή εξαμελείς ανθρακικούς δακτυλίους. Η πλέον γνωστή ένωση είναι αυτή με 60 άτομα άνθρακα (C60). Οι ενώσεις αυτές είναι οι μόνες μορφές άνθρακα που παρουσιάζουν κάποια διαλυτότητα σε διάφορους οργανικούς διαλύτες. Το όνομα "φουλερένια" προέρχεται από την ομοιότητα των μορίων αυτών με τους "γεωδετικούς" θόλους κτηρίων, που σχεδίασε ο αρχιτέκτονας Richard Buckminster Fuller (1895-1983). Οι Harold Kroto, Robert Curl και Richard Smalley τιμήθηκαν για αυτήν την ανακάλυψή τους με το Nobel Χημείας του 1996.





Harold Kroto
(1939)
Robert Curl
(1933)
Richard Smalley
(1943-2005)
Μόριο του φουλερένιου C60
Ο αρχιτέκτονας Richard Buckminster Fuller (1895-1983) μπροστά σε ένα γεωδετικό θόλο
Το 1994-1996, πραγματοποιήθηκε η πρώτη ολική σύνθεση του αντικαρκινικού φαρμάκου Taxol (υπάρχει ως φυσικό προϊόν στον φλοιό του κορμού ενός είδους ελάτου) από τις ερευνητικές ομάδες του Κύπριου χημικού Kyriakos C. Nicolaou (1946) και των Αμερικανών χημικών Robert A. Holton και Samuel Danishefskiy (1936) (βλ. Χημική ένωση του μήνα: Ταξόλη).




Οι πρωταγωνιστές της ολικής σύνθεσης της ταξόλης: Αριστερά: Robert A Holton, Πολιτειακό Πανεπιστήμιο Φλόριντα. Μέσον: Kyriacos C. Nicolaou (1946, Κύπρος), Πανεπιστήμιο Καλιφόρνιας, στο San Diego. Δεξιά: Samuel J. Danishefsky (1936), Πανεπιστήμιο Columbia Νέας Υόρκης.
Το μόριο της ταξόλης, η ολική σύνθεση της οποίας περιλαμβάνεται πλέον στα αριστουργήματα της Οργανικής Σύνθεσης.
16.5. Οι σχετικά νεότερες εξελίξεις μέσω των Nobel Χημείας 1990-2010
Τα Βραβεία Nobel Χημείας των τελευταίων 15 χρόνων και η αιτιολογήσεις τους, όπως περιγράφονται από τη Επιτροπή Nobel της Βασιλικής Σουηδικής Ακαδημίας Επιστημών, αποτελούν ένα τρόπο συνοπτικής καταγραφής των σημαντικότερων επιτευγμάτων και ανακαλύψεων στους διάφορους τομείς της χημείας που πραγματοποιήθηκαν κατά τα τελευταία 30-40 χρόνια. Στις ανακαλύψεις αυτές σημαντικό υπάρχουν ανακαλύψεις με βιολογικά μόρια και βιοχημικές διεργασίες, νέες μεθόδους, νέα υλικά και ρύπανση του περιβάλλοντος. Τα βραβεία αυτά και η συνοπτική-τυπική αιτιολόγησή τους έχουν ως εξής:
1990, Elias James Corey: "Για την ανάπτυξη της θεωρίας και της μεθοδολογίας στην οργανική σύνθεση".
1991, Richard R. Ernst: "Για τη συνεισφορά του στην ανάπτυξη της μεθοδολογίας της φασματοσκοπίας πυρηνικού μαγνητικού συντονισμού (NMR) υψηλής διακριτικής ικανότητας".
1992, Rudolf A. Marcus: "Για τη συνεισφορά του στη θεωρία των αντιδράσεων μεταφοράς ηλεκτρονίων σε χημικά συστήματα.
1993, Kary B. Moullis, Michael Smith: "Για τη συνεισφορά τους στην ανάπτυξη της χημείας που βασίζεται στο DNA", κατά το ήμισυ στον πρώτο "Για την εφεύρεση των μεθόδων που βασίζονται στην αλυσιδωτή αντίδραση πολυμεράσης (PCR)" και κατά το υπόλοιπο ήμισυ στον δεύτερο "Για τη θεμελιακή συνεισφορά του στην καθιέρωση της βασιζόμενης σε ολιγονουκλεοτίδια κατευθυνόμενη κατά θέση μεταλλαξιγένεση και στην εφαρμογή της για τη μελέτη των πρωτεϊνών".
1994, George Α. Olah: "Για τη συνεισφορά του στη χημεία των καρβοκατιόντων".
1995, Paul J. Crutzen, Mario J. Molina, F. Sherwood Rowland: "Για την εργασία τους στην ατμοσφαιρική χημεία και ειδικότερα σε ό,τι αφορά τον σχηματισμό και τη διάσπαση του όζοντος".





Paul J. Crutzen (1933)
Mario J. Molina (1943)
F. Sherwood Rowland (1927)
Οι έρευνες των Crutzen, Molina και Rowland πάνω στις καταστροφικές επιπτώσεις των χλωροφθορανθράκων στο τροποσφαιρικό όζον, είχαν ως αποτέλεσμα τη σταδιακή απαγόρευση της παραγωγής και κάθε είδους χρήσης αυτών των ουσιών (βλ. Χημική ένωση του μήνα: 'Οζον)
1996, Harold W. Croto, Robert Curt, Richard E. Smalley: "Για την ανακάλυψη των φουλερενίων".
1997, Paul D. Boyer, John E. Walker, Jens C. Skou: Το ήμισυ του βραβείου στους δύο πρώτους "Για τη διευκρίνιση του ενζυμικού μηχανισμού σύνθεσης της τριφωσφορικής αδενοσίνης (ATP)" και το υπόλοιπο ήμισυ στον τρίτο "Για την πρώτη ανακάλυψη ενός ιοντο-μεταφορικού ενζύμου της Na+,K+ - ATPάσης".
1998, Walter Kohn, John A. Pople: Στον πρώτο "Για την ανάπτυξη της συναρτισοειδούς θεωρίας" και στον δεύτερο "για την ανάπτυξη υπολογιστικών μεθόδων στην Κβαντική Χημεία".
1999, Ahmed H. Zewall: "Για τις μελέτες του στις μεταπτωτικές καταστάσεις χημικών αντιδράσεων χρησιμοποιώντας φασματοσκοπία φεμτοδευτερολέπτων".



Ahmed H. Zewall (1946)
Σύστημα υπερταχέος laser στερεάς κατάστασης (Ti : σαπφείρου) που χρησιμοποιείται
για τη μελέτη ταχύτατων αντιδράσεων
Τυπικό 3-D φάσμα (απορρόφηση ως συνάρτηση μήκους κύματος - χρόνου)
2000, Allan J. Heeger, Allan G. McDiarmidt, Hideki Shirakawa: "Για την ανακάλυψη κα την ανάπτυξη αγώγιμων πολυμερών".
2001, William S. Knowles, Ryoji Noyori, K.Barry Sharpless: Το ήμισυ του βραβείου στους δύο πρώτους "Για την εργασία του πάνω στις χειραλικά καταλυόμενες αντιδράσεις υδρογόνωσης" και το υπόλοιπο ήμισυ στον τρίτο "Για την εργασία του πάνω στις χειραλικά καταλυόμενες αντιδράσεις οξείδωσης".
2002, John B. Fenn, Koici Tanaka, Kurt Wüthrich: "Για την ανάπτυξη μεθόδων ταυτοποίησης και δομικής ανάλυσης βιολογικών μακρομορίων", κατά το ήμισυ στους δύο πρώτους "Για την ανάπτυξη των μεθόδων ιοντισμού μαλακής εκρόφησης για αναλύσεις βιολογικών μακρομορίων με φασματομετρία μάζας" και κατά το υπόλοιπο ήμισυ στον τρίτο "Για την ανάπτυξη μεθόδων μαγνητικού πυρηνικού συντονισμού για τον προσδιορισμό της τρισδιάστατης δομής βιολογικών μακρομορίων σε διάλυμα".
2003, Peter Agre, Robert MacKinnon: "Για τις ανακαλύψεις σχετικά με τις μεμβράνες των κυττάρων", στον πρώτον "για την ανακάλυψη διαύλων ύδατος" και στον δεύτερο "Για τις δομικές και μηχανιστικές μελέτες των διαύλων ιόντων".
2004, Aaron Ciechanover, Avram Hershko, Irwin Rose: "Για την ανακάλυψη της απόπτωσης των πρωτεϊνών με την παρέμβαση της ουβικιτίνης".
2005, Ives Chauvin, Robert J. Grubbs, Richard R. Schrock: "Για την ανάπτυξη μεταθετικών μεθόδων στην οργανική σύνθεση".
2006, Rodger D. Kormberg: "Για τις μελέτες του σε μοριακή βάση των μηχανισμών αντιγραφής γενετικών πληροφοριών σε ευκαρυωτικά κύτταρα".
2007, Gerhard Ertl: "Για τις μελέτες του επί των χημικών διεργασιών σε επιφάνειες στερεών".
2008, Osama Shimomura, Martin Chalfie, Rogen Y. Tsien: "Για την ανακάλυψη, ανάπτυξη και πολλαπλές εφαρμογές της πράσινης φθορίζουσας πρωτεΐνης (Green Fluorescent Protein, GFP)".
2009, Venkatraman Ramakrishnan, Thomas A. Steitz, Ada E. Yonath: "Για τις μελέτες τους πάνω στη δομή και τη λειτουργία των ριβοσωμάτων".
2010, Richard F. Heck, Erichi Negishi, Akira Suazuki: "Για τις αντιδράσεις διασταυρούμενης σύνθεσης που καταλύονται από παλλάδιο".
17. Επίλογος
Η ιστορία της Χημείας συνεχίζεται με αμείωτο ερευνητικό και επιστημονικό ενδιαφέρον. Παρά τη ραγδαία εξέλιξη των Θετικών Επιστημών και ιδιαίτερα της Χημείας, τα τελευταία 50 χρόνια, παραμένουν ανεξερεύνητες πολλές επιστημονικές περιοχές και έτσι, ακόμη και σήμερα παραμένουν πολλά ερωτήματα και πολλές ενδιαφέρουσες πλευρές των φυσικών φαινομένων που δεν έχουν εξηγηθεί επαρκώς.
'Οπως και στους άλλους κλάδους της επιστήμης, η Χημεία είχε μια εξελικτική πορεία με πολλές ανατροπές, λανθασμένες απόψεις και σφάλματα στην ερμηνεία χημικών φαινόμενων. Παρ' όλα αυτά η πολύχρονη πειραματική εργασία χιλιάδων χημικών και οι οξυδερκείς παρατηρήσεις τους διαλεύκαναν πολλές πλευρές της χημικής δομής και των χημικών ιδιοτήτων των διαφόρων ουσιών. Η Χημεία συνέβαλε αποφασιστικά στην αύξηση του προσδόκιμου ζωής του ανθρώπου, στη θεραπεία πολλών ασθενειών και στην ανακάλυψη μεθόδων και νέων υλικών, που βελτίωσαν την ποιότητα της ζωής του ανθρώπου.
Η τεκμηριωμένη πειραματική εργασία πολλών χημικών και η επανάληψη των πειραματικών δεδομένων παραμένει η μόνη ασφαλής μέθοδος για την πρόοδο της επιστήμης. Στην ιστορία της Χημείας υπήρξαν πολλοί επιστήμονες οι οποίοι με τα ευφυή πειράματά τους και την εύστοχη ερμηνεία των φυσικοχημικών αποτελεσμάτων συνέβαλαν στην πρόοδο της επιστήμης και στη διαφώτιση του ανθρώπου για τα φυσικά φαινόμενα πάνω στον πλανήτη Γη και στο Σύμπαν.
Πηγή http://www.chem.uoa.gr/
Η ιστορία της Χημείας ξεκινάει από την εποχή που οι προϊστορικοί άνθρωποι άρχισαν να ενδιαφέρονται για τα υλικά που χρησιμοποιούσαν για να κατασκευάσουν τις καλύβες τους, τα κεραμικά και γυάλινα σκεύη, τα μεταλλικά αντικείμενα και άλλα είδη καθημερινής χρήσης. Συγχρόνως, οι άνθρωποι άρχισαν να πειραματίζονται για το πως θα βελτίωναν τις ιδιότητες και την ποιότητα των υλικών και των αντικειμένων αυτών, αναμιγνύοντας διάφορα συστατικά και εφαρμόζοντας διάφορους τρόπους επεξεργασίας. Κάπου εκεί θα πρέπει να αναζητηθούν οι απαρχές της Χημείας, σε καμιά περίπτωση βέβαια ως επιστήμης, αλλά σαν μια μεθοδολογία που βασιζόταν σε εμπειρικές παρατηρήσεις του τύπου "δοκιμής και λάθους". Ωστόσο, και το τυχαίο αποδίδει, όταν διατίθεται άφθονος χρόνος.

Η Εύφορη Ημισέληνος, είναι η περιοχή που περιλαμβάνει τη Μεσοποταμία, δηλ. τις κοιλάδες των ποταμών Τίγρη και Ευφράτη. Στις περιοχές αυτές, για πρώτη φορά, αναπτύχθηκαν τουλάχιστον πριν 10.000 χρόνια διάφοροι πολιτισμοί αγροτικού χαρακτήρα.
Η ιστορία της Χημείας και τα εξελικτικά στάδιά της πέρασαν μέσα από τις εποχές των πανάρχαιων πολιτισμών των Σουμέριων και των Αιγυπτίων, τις φιλοσοφικές αναζητήσεις των υλιστικών φιλοσόφων της Αρχαίας Ελλάδας, των Ινδών και Κινέζων πειραματιστών και στη συνέχεια των Ρωμαίων και των Μουσουλμάνων, που ανακάλυψαν πλήθος νέων χημικών ουσιών και νέες πρακτικές μεθόδους παρασκευής τους.
Οι πρώτες χημικές γνώσεις διαδόθηκαν ταχύτατα στη Μεσαιωνική Ευρώπη, χάρις στους Αλχημιστές. Με μια πορεία μέσα από παρανοήσεις και λάθη, μέσα από ένα συνονθύλευμα μυστικισμού, προκαταλήψεων και παράξενων θρησκευτικών δοξασιών, κατάφερε να αναδειχθεί η Χημεία ως ένας αυτεξούσιος επιστημονικός κλάδος κάπου κατά τον 17ου αιώνα, χάρις στη δουλειά λίγων πραγματικά φωτισμένων ανθρώπων.
Η λέξη Αλχημεία προέρχεται από το αραβικό οριστικό άρθρο Αλ- και τη λέξη Χημεία (al-kimya). Η προέλευση της λέξης Χημεία παραμένει ακόμη και σήμερα αντικείμενο πολλών θεωριών και αναζητήσεων. Η επικρατέστερη εκδοχή είναι ότι σχετίζεται με τις λέξεις χημία και χυμεία.
Η "χημία" εικάζεται ότι προέρχεται από την αρχαία αιγυπτιακή λέξη κεμ (= μαύρος), διότι ως τέχνη και επιστήμη συνδέθηκε με την Αίγυπτο, που σύμφωνα με τον Πλούταρχο ονομαζόταν και ως Μαύρη Γη ή Μαύρη Χώρα. Ακόμη μπορεί να σχετίζεται με τη μετατροπή των "μαύρων" ορυκτών και μεταλλευμάτων σε χρήσιμες ουσίες και μέταλλα.
Η λέξη χυμεία (khymeia) προέρχεται από το ρήμα χέω και τη διαδικασία της χύτευσης και αναφέρονταν στην ανάμιξη χρυσού και αργύρου με σύντηξη, που εκτελούσαν οι χυμευτές. Υπάρχει Βυζαντινό έγγραφο όπου αναφέρεται ότι παλαιότερα ο Ρωμαίος Αυτοκράτορας Διοκλητιανός (245-312 μ.Χ.) είχε διατάξει την καταστροφή όλων των Αιγυπτιακών βιβλίων που σχετίζονταν με τη χυμεία, δηλ. τη σύντηξη χρυσού και αργύρου.
Μια ακόμη εκδοχή για την προέλευση της λέξης "χημεία" προσφέρεται από έναν 'Ελληνα ή Αιγύπτιο αλχημιστή των πρωτοχριστιανικών αιώνων, τον Ζώσιμο τον Πανοπολίτη (4ος-5ος αιώνας). Στο βιβλίο του με τίτλο Ιμούθ (μια από τις αποδόσεις του ονόματος του Φαραώ Imhotep, 2655-2600 π.Χ., σε ελληνικά κείμενα), γράφει για τη γένεση της Αλχημείας, σύμφωνα με την οποία ο "πρώτος των τεχνών" ήταν ο Χημεύ (με αιγυπτιακή γραφή: "Chêmi"), από τον οποίο προέρχεται "το όνομα της χημείας".

Ο χρυσός και ο χαλκός είναι από τα λίγα μέταλλα που βρίσκονται στη φύση ελεύθερα. Το γεγονός αυτό σε συνδυασμό με το χαμηλό σημείο τήξεως, δικαιολογεί το γεγονός ότι ήταν τα πρώτα μέταλλα που γνώρισε και επεξεργάστηκε ο άνθρωπος.


Διακοσμητικά μεταλλικά αντικείμενα (από χαλκό και κράματά του) από τον πολιτισμό των Σουμερίων (Πόλη Ούρ, Μεσοποταμία).
Ανεξάρτητα πάντως της προέλευσης της λέξης Χημεία, το βέβαιο είναι οι δύο αρχαίοι πολιτισμοί της Αιγύπτου και της Ελλάδας συνέβαλαν αποφασιστικά στην προώθηση και στην εξέλιξης της Χημείας.
Πηγές από το Διαδίκτυο: (1) "Etymology of Chemistry" (Journal of Chemical Education). (2) "Chemistry (etymology)" (Wikipedia). (3) "Η Αλχημία στα Βυζαντινά Χρόνια" (Νικόλαος Βασ. Λίτσας, Αρχαιολογία και Τέχνες, τχ. 107)
2. Η Απαρχή της Χημείας στη Μεσοποταμία
Η ιστορία της Χημείας ξεκινά από την εποχή της δημιουργίας των πρώτων αγροτικών πολιτισμών στην περιοχή των ποταμών Τίγρη και Ευφράτη, στην περιοχή η οποία στα ιστορικά δοκίμια αναφέρεται ως Εύφορη Ημισέληνος (Fertile Crescent).
 Στην περιοχή αυτή αναπτύχθηκαν οι πρώτοι αγροτικοί πολιτισμοί (8.000-10.000 π.Χ.). Τα νερά των ποταμών που πλημμύριζαν την κοιλάδα και η πλούσια σε θρεπτικά συστατικά λάσπη, βοηθούσαν τις συστηματικές αγροτικές καλλιέργειες και επομένως συνέβαλαν στη μόνιμη εγκατάσταση λαών που μέχρι τότε ζούσαν νομαδικά, αναζητώντας τροφή από κυνήγι και άγρια φρούτα και λαχανικά.
Στην περιοχή αυτή αναπτύχθηκαν οι πρώτοι αγροτικοί πολιτισμοί (8.000-10.000 π.Χ.). Τα νερά των ποταμών που πλημμύριζαν την κοιλάδα και η πλούσια σε θρεπτικά συστατικά λάσπη, βοηθούσαν τις συστηματικές αγροτικές καλλιέργειες και επομένως συνέβαλαν στη μόνιμη εγκατάσταση λαών που μέχρι τότε ζούσαν νομαδικά, αναζητώντας τροφή από κυνήγι και άγρια φρούτα και λαχανικά. Η Μεσοποταμία έγινε το λίκνο πλούσιων πολιτισμών και δημιουργίας μεγάλων πόλεων, όπως η Βαβέλ (Βαβυλώνα) και η Ουρ. Εκεί αναπτύχθηκε ο πανάρχαιος πολιτισμός των Σουμερίων (4η χιλιετηρίδα π.Χ.). Οι Σουμέριοι ανέπτυξαν τη γραφή σε εγχάρακτες πλάκες, την κεραμική με τη χρήση του κεραμευτικού τροχού και τη μεταλλουργία για την κατασκευή οικιακών εργαλείων και δοχείων, αλλά και όπλων.
Ευρήματα που ανάγονται στο 6.000 π.Χ., αποδεικνύουν πως από τότε ήταν ήδη γνωστές τεχνικές επεξεργασίας μεταλλευμάτων για την παρασκευή μεταλλικού χαλκού. Ακολούθησαν οι περισσότερες συστηματικές μεταλλουργικές πρακτικές και πιο εξελιγμένες τεχνικές της μεταλλουργίας (καθαρισμός μεταλλευμάτων με υψηλές θερμοκρασίες, χύτευση, εμπλουτισμός).
Στη συνέχεια διαπίστωσαν ότι ο χαλκός που παρασκευαζόταν με αναγωγή ορυκτών χαλκού αναμιγμένων με ορυκτά κασσιτέρου, ήταν σκληρότερος και ανθεκτικότερος. 'Ετσι, ανακαλύφθηκε ο ορείχαλκος, κράμα χαλκού-κασσιτέρου (με 10 έως 20% κασσίτερο). 'Ετσι, ήδη από το 3.800-4.000 π.Χ. οι Σουμέριοι γνώριζαν τα κράματα.
Με βάση αρχαιολογικά ευρήματα, εκτιμάται ότι κατά χρονολογική σειρά ανακαλύφθηκαν και άρχισε να γίνεται η χρήση των ακόλουθων μετάλλων (σε παρένθεση: η εκτιμούμενη χρονολογία κατασκευής/χρήσης του αρχαιότερου μεταλλικού αντικειμένου): Χρυσός (6.000 π.Χ.), χαλκός (4.200 π.Χ.), άργυρος (4.000 π.Χ.), μόλυβδος (3.500 π.Χ.), κασσίτερος (1.750 π.Χ.), σίδηρος (1.500 π.Χ.), υδράργυρος (750 π.Χ.).
Τότε περίπου άρχισε να γίνεται αισθητή και η ανάγκη για καύσιμα, τόσο για τις καθημερινές ανάγκες των πληθυσμών, όσο και για τη μεταλλουργία. Οι ανάγκες αυτές σε μεγάλο μέρος τους καλύπτονταν από την άσφαλτο και άλλα πισσώδη υλικά, που αφθονούσαν στην περιοχή της Μεσοποταμίας και ανάβλυζαν από ρωγμές των εδαφών.

Η τυχαία ανακάλυψη του γυαλιού και ορισμένα γυάλινα φιαλίδια της ρωμαϊκής εποχής, όταν είχε πλέον εξελιχθεί κατά πολύ η τέχνη της υαλουργίας.
Παράλληλα, οι κάτοικοι των περιοχών αυτών άρχισαν να ασχολούνται με τη βαφική. Χρησιμοποιούσαν χρώματα, που παρασκεύαζαν από εκχυλίσματα καρπών και φλοιών δέντρων ή από έγχρωμα ορυκτά υλικά, για να βάφουν υφάσματα, αλλά και το ίδιο το δέρμα τους για καλλωπιστικούς λόγους. Σύντομα διαπίστωσαν τις απορρυπαντικές ιδιότητες της στάχτης ξύλων. Βρήκαν τρόπους να παραλαμβάνουν τα αιθέρια έλαια από αρωματικά φυτά και τους καρπούς τους και να παρασκευάζουν αρώματα και καλλυντικά.
Η βυρσοδεψία ήταν μια ακόμη δραστηριότητα. Μέσω της χρήσης χημικών υλικών, βελτίωναν σημαντικά την ποιότητα και την αντοχή των δερμάτινων προϊόντων.
'Οταν διαπίστωσαν πως στις φωτιές που άναβαν καίγοντας ξύλα στην άμμο, έβρισκαν ανάμεσα στις στάχτες κάτι περίεργες σχεδόν διαφανείς συμπαγείς μάζες (αποτέλεσμα της σύντηξης της άμμου με τα ανθρακικά άλατα του καλίου από τη στάχτη των ξύλων), άρχισαν να σκέφτονται πως θα μπορούσαν να αξιοποιήσουν αυτό το περίεργο νέο υλικό που δεν ήταν άλλο από το γυαλί.

Αρχαία αιγυπτιακή τοιχογραφία με απεικόνιση εργασιών σε διάφορα εργαστήρια.
Οι παραπάνω τέχνες και τεχνικές βελτιώθηκαν με πειραματισμό και βαθμιαία καθιερώθηκαν μεθοδολογίες και πρακτικές που μεταβιβάζονταν από γενεά σε γενεά. Οι αρχαίοι τεχνίτες δεν είχαν βέβαια ιδέα για τη χημεία των υλικών, αλλά είχαν αποκτήσει με την πάροδο των χρόνων ένα πλούτο από πρακτικές γνώσεις.
Πηγές από το Διαδίκτυο: (1) "The Fertile Crescent" (University of Victoria, Canada). (2) "Sumerians" (AncientScripts.com). (3) "History of Metallurgy". (4) "A Short History of Metals" (Alan W. Cramb, Carnegie Mellon University). (5) "A Brief History of Glass" (GlassOnLine.com).
3. Η Χημεία κατά την Περίοδο της Αρχαίας Αιγύπτου
Η Αρχαία Αίγυπτος χαρακτηρίσθηκε από τον πλούσιο αρχαίο πολιτισμό της που εξελίχθηκε από τις προϊστορικές εποχές (περίπου 3.300 π.Χ.) μέχρι το 31 π.Χ., όταν η Αίγυπτος κατέστη επαρχία της Ρωμαϊκής Αυτοκρατορίας.
Η Αίγυπτος με τα πολυάριθμα σταθερά βασίλεια και με τα πολιτισμικά επιτεύγματα (3.200 π.Χ.: γραφή με ιερογλυφικά, 3.100 π.Χ.: χρήση δεκαδικού συστήματος αρίθμησης, 3.100 π.Χ.: κελάρια κρασιού, 2.700 π.Χ.: χειρουργική τεχνική, 2.500 π.Χ.: κατασκευή της μεγάλης πυραμίδας της Giza), αποτελεί ένα πλούσιο σε εξελίξεις στάδιο στην ιστορία της Χημείας. Πολλές τεχνικές που είχαν ήδη αναπτυχθεί και καθιερωθεί στη Μεσοποταμία μεταφέρθηκαν και εξελίχθηκαν ακόμη περισσότερο στην Αρχαία Αίγυπτο.
Μερικές τεχνικές της αρχαίας Αιγυπτιακής χημείας προξενούν και σήμερα το ενδιαφέρον για τις πλούσιες γνώσεις που διέθεταν για πολλά χημικά υλικά και τις ιδιότητές τους. Κατέγραφαν με λεπτομέρειες διάφορες τεχνικές και τα αποτελέσματα διάφορων δοκιμών. Οι γνώσεις πολλών από αυτών των τεχνικών, είχαν την έννοια της τέχνης παρά της επιστήμης και αποτελούσαν αποκλειστικό προνόμιο της τάξης των ιερέων.

Αιματίτης, Fe2O3

Ορυχείο κίτρινης ώχρας, ένυδρο Fe2O3

Αζουρίτης, Cu3(OH)2(CO3)2

Μαλαχίτης, Cu2CO3(OH)2

Κιννάβαρι, HgS

Ερυθρά σανδαράχη (realgar), As2S2

Κίτρινη σανδαράχη (orpiment), As2S3

Αντιμονίτης, Sb2S3

Γαληνίτης, PbS
Μερικά από τα ορυκτά που χρησιμοποιούσαν οι αρχαίοι πολιτισμοί ως χρώματα.
Η σύγχρονη Ιατρική οφείλει πολλά στους αρχαίους Αιγυπτίους. Στην αρχή, επειδή ο άνθρωπος δεν μπορούσε να εξηγήσει όλα όσα του συνέβαιναν, άρχισε να τα αποδίδει σε υπερφυσικές δυνάμεις. Οι αρρώστιες θεωρήθηκαν έργα κακών πνευμάτων ή τιμωρία από μια θεότητα. Ο Imhotep (2655-2600 BC), 'Ιμυθες για τους αρχαίους 'Ελληνες, υπήρξε ο πιο διάσημος Αιγύπτιος ιατρός-παθολόγος, που ήταν συγχρόνως αστρονόμος και αρχιτέκτονας. Ο Imhotep χρησιμοποιούσε διάφορες χημικές ουσίες για θεραπείες ασθενειών. Αργότερα, ο Imhotep λατρεύτηκε ως θεός της Θεραπείας και της Ιατρικής.
Οι Αιγύπτιοι ανέπτυξαν τις τεχνικές της μεταλλουργίας και έγιναν εξειδικευμένοι τεχνικοί για την κατεργασία του χρυσού από μεταλλεύματα και να το αναμιγνύουν με άλλα μέταλλα για να είναι σταθερότερο. Γνώριζαν την παρασκευή ορείχαλκου (μπρούτζου) από χαλκό και κασσίτερο. Ευρήματα σιδηρών αντικειμένων σε πυραμίδες δίνουν την εντύπωση ότι γνώριζαν και τρόπους παρασκευής χάλυβα (ατσάλι) ήδη από το 2.900 π.Χ.
Η υαλουργία υπήρξε ένας ακόμη τομέας στον οποίο οι αρχαίοι Αιγύπτιοι έκαναν σημαντικές προόδους. Τα ευρήματα μεγάλων φούρνων υαλουργίας (ανασκαφές στην περιοχή Tel-El-Amarna, χρονολογούμενοι γύρω στο 1400 π.Χ.) και τα διάφορα είδη υάλινων σκευών και κοσμημάτων από έγχρωμο γυαλί δείχνουν μια υψηλή τεχνική κατάρτιση και γνώση αυτών των υλικών. 'Ετσι φαίνεται ότι γνώριζαν την κατασκευή μολυβδούχου υάλου (κρυστάλλου), όπως επίσης γνώριζαν πως μπορούσαν να χρησιμοποιήσουν κοβαλτιούχα ορυκτά για την παρασκευή βαθυκύανης υάλου. Ακόμη, γνώριζαν να κατασκευάζουν υαλώματα (σμάλτα) από οξείδια διαφόρων μετάλλων και να καλύπτουν με αυτά τις επιφάνειες πήλινων δοχείων και άλλων πήλινων αντικειμένων.
Οι αρχαίοι Αιγύπτιοι σημείωσαν εξαιρετικές προόδους στην υφαντουργία, γνώριζαν την κατασκευή υφασμάτων από βαμβάκι και μαλλί και τρόπους χρώσης τους με φυσικές ουσίες. Τυπικά ανόργανα υλικά που χρησιμοποιούσαν σε βαφές ήταν ο αιματίτης (Fe2O3) για κόκκινο χρώμα, βαθυκύανο τριμμένο γυαλί (ύαλος κοβαλτίου) για μπλε, βασικά ανθρακικά άλατα χαλκού για γαλάζιο χρώμα (αζουρίτης) και πράσινο χρώμα (μαλαχίτης), κίτρινη ώχρα (ένυδρο Fe2O3) για κίτρινο. Με τα ίδια χρώματα και τα υλικά που χρησιμοποιούσαν έβαφαν ανάκτορα, ναούς, σπίτια και τάφους.
Οι Αιγύπτιοι ανέπτυξαν τεχνικές και μεθόδους για την παρασκευή χρωστικών ουσιών από ανόργανα υλικά και από φυτικές ουσίες. Χρησιμοποίησαν τη φωτιά για την ανάμιξη και τη συνθετική παρασκευή χρωμάτων (με υγρές χημικές μεθόδους και χημικά στάδια). 'Ηδη από το 3.000 π.Χ., χρησιμοποιούσαν ορυκτά, όπως ο γαληνίτης (PbS) και ο αντιμονίτης (Sb2S3) σε ψιμύθια (καλλυντικά προσώπου). Για παράδειγμα, μίγμα λειοτριβημένου αντιμονίτη και λίπους, χρησιμοποιούσαν ως καλλυντική βαφή, για να βάφουν μαύρο το περίγραμμα των ματιών. Πιθανώς επίσης γνώριζαν και τον υδράργυρο, αφού χρησιμοποιούσαν το ορυκτό κιννάβαρι (HgS) για τη ερυθρά χρώση υφασμάτων. Οι γνώσεις αυτές μεταφέρθηκαν και εφαρμόσθηκαν και στην Αρχαία Ελλάδα, αλλά ήταν ήδη τόσο προχωρημένες τεχνικές που δεν χρειάσθηκε να βελτιωθούν.
Τέλος, οι αρχαίοι Αιγύπτιοι ανέπτυξαν τις τεχνικές για την παρασκευή αρωμάτων και ελαιωδών αλοιφών για το δέρμα. Οι τεχνικές που χρησιμοποιούσαν ήταν εξαιρετικά αναπτυγμένες και οι ανακαλύψεις και οι συνθέσεις τους αξιοποιήθηκαν και από άλλους πολιτισμούς που ακολούθησαν τον Αιγυπτιακό.

(1)

(2)

(3)

(4)

(5)
Αρχαία Αίγυπτος: (1) Γυάλινο δοχείο. (2) Μεταλλικό δακτυλίδι. (3) Υαλουργικές εργασίες. (4) Συλλογή φιαλιδίων με καλλυντικά. (5) Μεταφορά φυτών μυρτιάς για την παρασκευή αρωμάτων
4. Οι Αρχαίοι 'Ελληνες Φιλόσοφοι και η Συμβολή τους στη Χημεία
Η αρχαία Ελλάδα και ο πολιτισμός της είναι ασφαλώς η συνέχεια του πολιτισμού της αρχαίας Αιγύπτου με μια όμως πολύ μεγαλύτερη δυναμική. Οι αρχαίοι 'Ελληνες αξιοποίησαν πολλά από τα επιτεύγματα των Αιγυπτίων στις τεχνικές της μεταλλουργίας, της υαλουργίας, της βαφής υφασμάτων και των αρωματικών υλών. Οι τεχνικές αυτές ήταν ήδη πολύ εξελιγμένες και δεν χρειάστηκαν ουσιαστικά να προσθέσουν νέες βελτιώσεις ή κάποιες αλλαγές στις μεθοδολογίες.
Τους αρχαίους Έλληνες απασχολούσε όχι τόσο το "πώς", αλλά το "γιατί", δηλ. η αναζήτηση της αλήθειας και των αιτίων. Σύμφωνα με τους αρχαιολόγους, η συνεισφορά των Αρχαίων Ελλήνων και διανοητών στις φυσικές επιστήμες ήταν κυρίως οι θεωρητικές έννοιες. Στην αρχαία Ελλάδα πραγματοποιήθηκε για πρώτη φορά η απόδοση των φυσικών φαινομένων σε φυσικά αίτια και η αντικατάσταση των υπερφυσικών δυνάμεων από τους φυσικούς νόμους.






Εμπεδοκλής (495 - 435 π.Χ.)
Λεύκιππος (5ος αιώνα π.Χ., δάσκαλος του Δημόκριτου)
Δημόκριτος
(460-370 π.Χ.)
Πλάτων
(428-348 π.Χ.)
Αριστοτέλης
(384-322 π.Χ.)
Επίκουρος
(341 - 270 π.Χ.)
Οι ιδέες των αρχαίων Ελλήνων φιλοσόφων ήταν η απαρχή πολλών σημερινών εννοιών των φυσικών επιστημών. Η αρχαία ελληνική φυσική φιλοσοφία είχε μεγάλη επίδραση και στη σύγχρονη χημεία, είτε άμεσα, είτε έμμεσα, έστω και μέσω των παραδοξοτήτων της αλχημείας. Μερικές από αυτές τις ιδέες που βρήκαν εφαρμογή στη χημεία ακόμη και σήμερα είναι:

Το κλασικό διάγραμμα ενός τετραγώνου εγγεγραμμένου σε ένα άλλο. Στις γωνίες του ενός βρίσκονται τα βασικά στοιχεία και στις γωνίες του άλλου βρίσκονται οι ιδιότητές τους.
(α) Η έννοια του στοιχείου. Η θεωρία των τεσσάρων βασικών στοιχείων ή ριζωμάτων (γη, ύδωρ, πυρ και αήρ) διατυπώθηκε από τον Εμπεδοκλή (495-435 π.Χ., από Ακράγαντα, Σικελία). Τα τέσσερα στοιχεία ήταν μέρος της φιλοσοφικής του συμβολής και ιδιαίτερα το ποίημα (2.000 στίχοι) "Περί Φύσεως". Τα πάντα είναι συνδυασμοί αυτών των τεσσάρων στοιχείων. Στα στοιχεία αυτά αποδίδονται κυκλικά οι ιδιότητες "υγρό", "θερμό", "ξηρό" και "ψυχρό" ως πρωτεύουσες ή δευτερεύουσες. Ο "αήρ" είναι πρωτίστως "υγρός" και δευτερευόντως "θερμός", το "πυρ" είναι πρωτίστως "θερμό" και δευτερευόντως "ξηρό", η "γη" είναι πρωτίστως "ξηρή" και δευτερευόντως "ψυχρή" και το "ύδωρ" είναι πρωτίστως "ψυχρό" και δευτερευόντως "υγρό".
(β) Η έννοια του ατόμου. Η ατομική θεωρία για τη συγκρότηση ύλης διατυπώθηκε αρχικά από τον Λεύκιππο (5ος αιώνας π.Χ., Μίλητος). Για τον Λεύκιππο είναι λίγα πράγματα γνωστά. 'Εζησε κατά την περίοδο (περίπου) 480-420 π.Χ. Παρακολούθησε την Ιονική σχολή φιλοσοφίας, σπούδασε και στην Ελέα (σήμερα Velia, στη νότια Ιταλία) και φαίνεται ότι επηρεάστηκε κυρίως από τον προσωκρατικό φιλόσοφο Ζήνωνα τον Ελεάτη (490;-430; π.Χ.). Ίδρυσε σχολή στα 'Αβδηρα της Θράκης. Η ατομική θεωρία του Λεύκιππου διατυπώθηκε πιο συστηματικά από τον μαθητή του Δημόκριτο (460-370 π.Χ., 'Αβδηρα, Θράκη). Η ατομική θεωρία όριζε ότι τα άτομα είναι τα έσχατα μόρια της ύλης. Τα άτομα (: α-στερητικό + τομή) είναι άτμητα, άφθαρτα, αναλλοίωτα και κινούνται αδιάκοπα στον χώρο. Υπάρχουν άπειρα είδη ατόμων σε συνεχή κίνηση και οποιαδήποτε μεταβολή της ύλης δεν είναι παρά ένα είδος ανασυνδυασμού των ατόμων.
(γ) Η διατήρηση της μάζας. Η θεωρία της αφθαρσίας της ύλης που διατύπωσαν παράλληλα ο Δημόκριτος και ο Διογένης ο Απολλωνιάτης (5ος αιώνας π.Χ.).

Πλάτωνας και Αριστοτέλης. Λεπτομέρεια από τον περίφημο πίνακα του Raphael "Η Σχολή των Αθηνών" (1510).
Οι ιδέες αυτές διαδόθηκαν κυρίως με τη διδασκαλία του Επίκουρου και αργότερα από το εκτενές φιλοσοφικό ποίημα του Λουκρητίου (Τίτος Λουκρήτιος Κάρος, 98-53 π.Χ., Ρωμαίος φιλόσοφος) που είχε τίτλο De Rerum Natura (Περί της Φύσεως των Πραγμάτων), όπου και εξηγούσε τις αρχές της ατομικής θεωρίας του Δημόκριτου.
Ο Επίκουρος (Σάμος 341- Αθήνα 270 π.Χ.) ήταν 'Ελληνας φιλόσοφος, ο οποίος ίδρυσε τη φιλοσοφική σχολή που έμεινε γνωστή ως "Επικούρειος Κήπος". Στόχος του Επίκουρου ήταν η αναζήτηση των αιτιών της ανθρώπινης δυστυχίας και των εσφαλμένων δοξασιών που την προκαλούν, όπως η δεισιδαιμονία.
Βασικές αρχές της διδασκαλίας του Επίκουρου είναι οι εξής: Με τον θάνατο έρχεται το τέλος όχι μόνο του σώματος αλλά και της ψυχής - οι θεοί ούτε επιβραβεύουν, ούτε τιμωρούν τους ανθρώπους. Το σύμπαν είναι άπειρο και αιώνιο - τα γενόμενα στον κόσμο συμβαίνουν τελικά, με βάση τις κινήσεις και τις αλληλεπιδράσεις των ατόμων που βρίσκονται σε έναν κενό χώρο.
Οι υλιστικές απόψεις του Επίκουρου πολεμήθηκαν άγρια από μεταγενέστερους φιλοσόφους και θεολόγους. Ο ίδιος κατασυκοφαντήθηκε και χαρακτηρίστηκε ως άτομο με ροπή προς τις ηδονές και τις απολαύσεις. Θα πρέπει να σημειωθεί ότι οι υλιστικές ιδέες και η αντίληψη περί ατόμων και αφθαρσίας της ύλης αναπτύχθηκαν περίπου την ίδια περίοδο από Ινδούς φιλοσόφους (Βεδική φιλοσοφία), αλλά με αρκετά πιο ήπιους τόνους και με ποιητική διάθεση.
Οι ατομικές θεωρίες του Δημόκριτου για την ύλη έμειναν στο περιθώριο για πολλούς αιώνες. Οι υλιστικές θεωρίες περί ατόμων, αφθαρσίας της ύλης και των στοιχείων δεν είχαν προοπτική διάδοσης, αφού έπεσαν στη δυσμένεια των φιλοσόφων Πλάτωνα (428-348 π.Χ.) και Αριστοτέλη (384-322 π.Χ.).
Ο Αριστοτέλης, ο πολυγραφότερος διαλεκτικός φιλόσοφος της αρχαιότητας, επηρέασε με τις θεωρίες του τη δυτική φιλοσοφική και επιστημονική σκέψη μέχρι και τον 17ο αιώνα. Ο Αριστοτέλης μελέτησε και έγραψε για πολλούς κλάδους (φιλοσοφία, ψυχολογία, λογική, πολιτική, φυσική, βιολογία, κ.α.). 'Εγραψε πολλά βιβλία για τη Φυσική (φυσική ακρόαση, περί ουρανού, περί γενέσεως και φθοράς, μετεωρολογικά και περί κόσμου) και τη Βιολογία (περί ζώων ιστορίας, περί ζώων μορίων, περί ζώων πορείας, περί ζώων κινήσεως, περί ζώων γενέσεως και περί φυτών).
Η φιλοσοφία του Αριστοτέλη κλείνει προς τον ιδεαλισμό και θέτει τον υλισμό σε μια μάλλον παθητική μοίρα. Σύμφωνα με τις θεωρίες του κάθε πράγμα αποτελείται από ύλη και πνεύμα, που είναι μεταξύ τους αδιάσπαστα ενωμένα. Η ύλη είναι παθητική και μόνη της παρέχει τη δυνατότητα, ενώ το πνεύμα ενεργητικό, και αποτελεί τη δύναμη που μεταβάλλει τη δυνατότητα σε πραγματικότητα.
Ο κόσμος, κατά τον Αριστοτέλη, είναι ενιαίος και αιώνιος και το σύμπαν ή ο κόσμος είναι σφαιρικός με κέντρο τη Γη. Η θεωρία αυτή ταίριαζε με τις θρησκευτικές αντιλήψεις και η γεωκεντρική εικόνα επικράτησε μέχρι την εποχή του Γαλιλαίου. Μέσω της τυπικής λογικής βλέπει την αντικειμενική πραγματικότητα "στατικά" και όχι μέσα στην αέναη μεταβολή και κίνησή της. Ο Αριστοτέλης διετύπωσε τη θεωρία της ύπαρξης του πέμπτου στοιχείου της φύσης (πέραν των τεσσάρων: γη, ύδωρ, πυρ και αήρ, που πίστευαν οι 'Ιωνες φιλόσοφοι). Ο Αριστοτέλης πρόσθεσε τον αιθέρα (: καθαρός, φρέσκος αέρας, καθαρός ουρανός) στο κέντρο του κλασικού τετραγώνου των στοιχείων. Ο αιθέρας παρουσιάζει κάποιες ιδιαιτερότητες ως στοιχείο, είναι: αγέννητος, αγήραντος, άφθαρτος, αΐδιος (αιώνιος), αναυξής και αναλλοίωτος. Ο αιθέρας θα ταυτισθεί αργότερα με τη Φιλοσοφική Λίθο των αλχημιστών. Επιπλέον εντοπίζεται στον "άνω τόπο" όπου κατοικεί η Θεότητα.

Να σημειωθεί στο σημείο αυτό, ότι η πρώτη αναφορά στην έννοια στοιχείον έγινε από τον Πλάτωνα, περίπου το 360 π.Χ. στον διάλογό του "Τίμαιος", όπου περιλαμβάνεται μια συζήτηση πάνω στη σύνθεση των ανόργανων και των οργανικών σωμάτων, μια πρωταρχική προσέγγιση πάνω στη χημεία. Ο Πλάτωνας θεωρούσε ότι το μικρότερο σωματίδιο κάθε στοιχείου αντιστοιχούσε σε ένα από τα πέντε κανονικά πολύεδρα, δηλ. κυρτά πολύεδρα με έδρες κανονικά πολύγωνα και ίδιες, τα οποία είναι γνωστά και ως "Πλατωνικά στερεά": το τετράεδρο (η φωτιά), ο κύβος (η γη), το οκτάεδρο (ο αέρας), το δωδεκάεδρο (ο αιθέρας) και το εικοσάεδρο (το νερό).
Ο Αριστοτέλης δέχεται ότι η παθητική ύλη συνδυάζεται με την ενεργητική αρχή, την εντελέχεια (ετυμολογία: εν + τέλος + έχω, η ενυπάρχουσα σε κάθε ον τάση για τελειότητα) ή ψυχή, που τη διαμορφώνει και της δίνει κίνηση. Με την αναντίρρητη εξουσία του στις φυσικές επιστήμες, οι γνώμες του επηρέασαν τη μελλοντική ιστορία των φυσικών επιστημών. Οι θεωρίες του αποτέλεσαν το υπόβαθρο της αντίληψης του κόσμου από τους θρησκευτικούς καθοδηγητές της Χριστιανικής εκκλησίας και ιδιαίτερα του Αγίου Αυγουστίνου. Η φιλοσοφική σκέψη μπορούσε να διατηρηθεί κάτω από τον μανδύα των δογματικών θρησκευτικών αντιλήψεων και η φύση γίνονταν κατανοητή όχι με την παρατήρηση και το πείραμα, αλλά από τα αναγραφόμενα στα θρησκευτικά βιβλία.

Ο προσωκρατικός φιλόσοφος Ζήνων ο Ελεάτης δείχνει στους μαθητές του τις πόρτες της αλήθειας (veritas) και του ψεύδους (falsitas). Τοιχογραφία στη Βιβλιοθήκη El Escorial της Μαδρίτης.
Πηγές από το Διαδίκτυο: (1) "The History of Ancient Chemistry" (Lois Fruen, www.realscience.breckschool.org). (2) "Atoms and Atheism - the changing ways that Christians have viewed the nature of matter".
5. Η Χημεία κατά την Περίοδο των Ρωμαίων


(α) Τίτος Λουκρήτιος Κάρος (98-55 π.Χ.). (β) Εξώφυλλο του 1ου τόμου του έργου του De Rerum Natura (έκδοση 1656).
Η συνεισφορά των Ρωμαίων στη Χημεία ήταν μάλλον περιορισμένη, αφού κυρίως ενδιαφέρονταν κυρίως για τις πρακτικές εφαρμογές των τεχνικών που ήδη γνωστές. Οι Ρωμαίοι φιλόσοφοι που συνέβαλαν κυρίως σε θέματα φυσικής και χημείας ήταν ο Λουκρήτιος και ο Πλίνιος.
Ο Τίτος Λουκρήτιος Κάρος (Titus Lucretius Carus, 98 π.Χ.- 55 π.Χ.) ήταν Ρωμαίος ποιητής και φιλόσοφος. Διατύπωσε τα διδάγματα της επικούρειας φιλοσοφίας σε ένα μνημειώδες ποίημα 7.415 στίχων στη λατινική γλώσσα, το De Rerum Natura ("Περί της Φύσεως των πραγμάτων"), το μόνο γνωστό του έργο. Ο Λουκρήτιος διαδραμάτισε σημαντικό ρόλο στη μετάδοση των ελληνικών φιλοσοφικών ιδεών και ιδιαίτερα των ατομικών θεωριών του Επίκουρου και κατ' επέκταση των υλιστικών θεωριών του Δημοκρίτου.
Ο Λουκρήτιος είχε εξαιρετικά ορθολογικές φιλοσοφικές αντιλήψεις για μια εποχή που κυριαρχούσαν μεταφυσικές ιδέες και δεισιδαιμονίες. Ο στόχος του έργου ήταν να απαλλάξει το νου των ανθρώπων από την προκατάληψη και το φόβο του θανάτου.
Ανέπτυξε διεξοδικά τις θέσεις του Επίκουρου, τον οποίον και αποθεώνει. Ο Λουκρήτιος εκφράζει τις επικούρειες απόψεις του για τη μεταφυσική, την υλιστική ατομική θεωρία και, γενικότερα, την υπεροχή των φυσικών φαινομένων ως κεντρικής ερμηνείας της λειτουργίας του κόσμου.
Ο Λουκρήτιος αντιπαθούσε και έβλεπε ως αβάσιμο κάθε είδος δεισιδαιμονίας, καθώς δεν πίστευε ότι το Σύμπαν κυβερνάται από θεϊκές παρεμβάσεις ή υπερφυσικές δυνάμεις.
Ο Πλίνιος ο Πρεσβύτερος (Pliny the Elder, 23-79 μ.Χ.), στο έργο του Φυσική Ιστορία (Naturalis Historiae, 77-79 μ.Χ.), διακρίνει τα φυσικά από τα χημικά φαινόμενα και επίσης εξετάζει θέματα ζωολογίας, βοτανικής, μεταλλουργίας και ορυκτών. Η "Φυσική Ιστορία" (31 βιβλία), είναι ένα πλήρες εγκυκλοπαιδικό σύγγραμμα φιλοσοφίας (ιδιαιτέρως φυσικής φιλοσοφίας), στο οποίο συνοψίζεται όλη η γνώση της εποχής του, ανθολογημένη από διάσπαρτα προγενέστερα ελληνικά και λατινικά συγγράμματα, στους τομείς της μεταφυσικής, της αστρονομίας, των μαθηματικών, της γεωγραφίας, της εθνογραφίας, της ανθρωπολογίας, της ζωολογίας, της βοτανολογίας, της φαρμακολογίας, της ηφαιστειολογίας, της ορυκτολογίας κ.α.



(α) Πλίνιος ο Πρεσβύτερος (23-79 μ.Χ.) (β) Εξώφυλλο του 1ου τόμου της Φυσικής Ιστορίας του Πλίνιου (έκδοση 1669). (γ) Το κιννάβαρι (HgS) οι Ρωμαίοι το εξόρυσσαν από τα ορυχεία του Almaden στην Ισπανία. Για την εξόρυξη του πολύτιμου αυτού ορυκτού αυτού χρησιμοποιούσαν μόνο κατάδικους, αφού η εργασία στα ορυχεία αυτά ισοδυναμούσε με καταδίκη σε θάνατο, λόγω της μεγάλης περιεκτικότητας της ατμόσφαιρας του ορυχείου σε ατμούς υδραργύρου. Ο Πλίνιος ήταν από τους πρώτους που αναγνώρισαν την τοξικότητα αυτού του πολύτιμου ορυκτού (το χρησιμοποιούσαν ως κόκκινη βαφή), αλλά και γενικότερα της επικινδυνότητας κάθε εργασίας με τον υδράργυρο.
Στην περιγραφή των φυτών, ο Πλίνιος μπόρεσε να συλλέξει αρκετές πληροφορίες για θεραπείες με βότανα. Στο τέλος του έργου, ως ο μοναδικός Ρωμαίος μετά τον Λουκρήτιο, που είχε για θέμα του ολόκληρο το βασίλειο της Φύσης, προσεύχεται για τις ευλογίες της παγκόσμιας μητέρας στο ολοκληρωμένο έργο του. Κατά τους αιώνες που ακολούθησαν η "Φυσική Ιστορία" χρησιμοποιήθηκε από αναρίθμητους σοφούς ως έγκυρη πηγή τόσο σε θέματα φυσικής φιλοσοφίας, όσο και ιατρικής.
Ο Πλίνιος έκανε αρκετές αναφορές σε μέταλλα και στην κατεργασία τους. Σε αυτά περιλαμβάνονται ο χρυσός, ο άργυρος, ο σίδηρος, ο μόλυβδος, ο κασσίτερος, ο υδράργυρος και το αντιμόνιο. Αναγνώρισε τις τοξικές ιδιότητες του υδραργύρου, όπως και τις διαφορές στις ιδιότητες μεταξύ του κοινών μορφών σιδήρου και του χάλυβα.
Σημαντική υπήρξε και η συνεισφορά του Πλίνιου στον τομέα των ορυκτών και των ιδιοτήτων διαφόρων μεταλλευμάτων. Μεταξύ πολλών άλλων συνεισφορών του σε θέματα χημείας και μεταλλουργίας, εισήγαγε μέθοδο διάκρισης της καθαρότητας πολύτιμων μετάλλων, όπως και ένα σύστημα χαρακτηρισμού της σκληρότητας των ορυκτών, ένα "πρώιμο" σύστημα της σημερινής κλίμακας σκληρότητας Mohs.
Ο θάνατος του Πλίνιου κατά πάσα πιθανότητα οφείλεται στην επιθυμία του να παρατηρήσει για όσο το δυνατόν μεγαλύτερο χρονικό διάστημα την έκρηξη του ηφαιστείου Βεζούβιου, που κατέστρεψε το 79 μ.Χ. την Πομπηία και το επίνειό της το Ερκουλάνουμ.
6. Η Χημεία στην Αρχαία Ινδία και τα Ιερά Κείμενα Vedas
Στην αρχαία Ινδία αναπτύχθηκε μεγάλος αριθμός χημικών διεργασιών και τεχνικών. Οι Ινδοί πειραματίσθηκαν με πλήθος διάφορων υλικών, ιδιαίτερα με φάρμακα από φυτικά εκχυλίσματα και έκαναν χρήσιμες παρατηρήσεις για τη φύση και τις ιδιότητες χημικών ουσιών για ιατρικούς σκοπούς. Οι γνώσεις αυτές αξιοποιήθηκαν αργότερα κατά την ονομαζόμενη Χρυσή Ισλαμική Περίοδο (Islamic Golden Age), δηλ. κατά την περίοδο 750-1250 μ.Χ., από τους Μουσουλμάνους, οι οποίοι βελτίωσαν πολλές ινδικής προέλευσης τεχνικές μεταλλουργίας, παρασκευής αρωμάτων και χρήσης βοτάνων και καρυκευμάτων.
Οι Ινδοί κατείχαν γνώσεις πυρομεταλλουργίας και της κατεργασίας μεταλλικών αντικειμένων από ορείχαλκο, ίσως και από το 2.300 π.Χ και αργότερα, από το 1500 π.Χ., αντικειμένων από σίδηρο. Από την πρώτη χιλιετία π.Χ., οι Ινδοί είχαν γίνει ειδικοί στην κατεργασία και παρασκευή υψηλής ποιότητας χάλυβα, ο οποίος ήταν πολυτιμότερος και από τον ίδιο τον χρυσό σε ορισμένες περιοχές της Ευρώπης και της Μέσης Ανατολής. Μόλις τον 17ο αιώνα μ.Χ., οι Ευρωπαίοι μελέτησαν τον τύπο αυτό χάλυβα που τους επέτρεψε να τυποποιήσουν και να βελτιώσουν τις δικές τους διεργασίες παρασκευής χάλυβα, γεγονός που είχε ως άμεσο αποτέλεσμα την ονομαζόμενη Βιομηχανική Επανάσταση, η οποία ως βάση είχε τη χρήση χάλυβα για την κατασκευή εργαλείων, μηχανών, γεφυρών, κ.λπ.
Εκτός όμως από τη συμβολή των Ινδών στη χημεία των μετάλλων και της κατεργασίας τους, οι αλχημιστές τους (η ινδική αλχημεία είναι γνωστή ως Rasa Shastra, που στην κυριολεξία σημαίνει "η επιστήμη του υδραργύρου") ήταν διάσημοι για τα επιτεύγματά τους. 'Ηταν γνωστοί για την ποικιλία χρωστικών υλών που χρησιμοποιούσαν, την υαλουργία, την παρασκευή ενός είδους τσιμέντου, τη χημική κατεργασία δέρματος και την παρασκευή σαπουνιού.
Κατά τον 5ο - 7ο αιώνα μ.Χ., όταν η δυτική και βόρεια Ευρώπη ζούσε τις Σκοτεινές Περιόδους της ιστορίας της (Dark Ages), οι Ινδοί είχαν ήδη αναπτύξει ένα εκπληκτικό τεχνολογικό πολιτισμό και έκαναν χρήση πολλών χημικών τεχνικών. Περιγραφές των τεχνικών αυτών βρίσκονται στις Βέδες (Vedas, ~300 π.Χ., veda: γνώση, στα σανσκριτικά), που είναι αρχικά κείμενα Ινδουϊσμού και τα οποία είχαν μεγάλη επιρροή στον Βουδισμό και άλλες θρησκείες. Στις Βέδες βρίσκονται ύμνοι, μαγικές συνταγές και περιγράφονται τελετουργικές καταστάσεις από την Αρχαία Ινδία. Οι Βέδες συγκαταλέγονται μεταξύ των αρχαιότερων θρησκευτικών κειμένων και εκτός της πνευματικής τους αξίας είναι πλούσιες πηγές πληροφοριών για την καθημερινή ζωή των αρχαίων Ινδών.




O περίφημος σιδερένιος στύλος (iron pillar) του Delhi, ύψους 7 μ. και βάρους 7 τόνων. Κατασκευασμένος κατά τον 4ο αιώνα μ.Χ. και εκτεθειμένος στα καιρικά στοιχεία επί 1600 και πλέον χρόνια, παραμένει ανοξείδωτος. Τυπική απόδειξη των μεταλλουργικών γνώσεων των αρχαίων Ινδών.
Εικόνες αρχαίων κειμένων από τις Βέδες.
Τυπικά προϊόντα (φυσικές βαφές, φυτικά δηλητήρια), της Ινδικής Αλχημείας (Rasa Shastra).

Σκεύη Ινδών Αλχημιστών (σχέδια από ινδικά αλχημιστικά κείμενα)
Πηγές από το Διαδίκτυο: (1) "Indian Alchemy" (The Alchemy Web Site). (2) "Indian Alchemy" (indianalchemy.com)
7. Ιστορία της Χημείας και Κινέζικος Πολιτισμός

Αριστερά: Χρονολογίες στην Κινέζικη Αλχημεία. Δεξιά: Ο Wei Po Yang, "πατέρας" της Κινέζικης αλχημείας.
Οι Ευρωπαίοι για πολλές δεκαετίες αγνοούσαν τη συνεισφορά του Κινέζικου πολιτισμού σε θέματα επιστήμης, αλχημείας και το γεγονός ότι στην Κίνα είχαν παρασκευασθεί χημικά υλικά πολύ πριν ακόμη ανακαλυφθούν στην Δύση.
'Οπως οι αλχημιστές στη Δύση έτσι και στην Κίνα οι αλχημιστές από αρχαιοτάτων χρόνων επεξεργάζονταν μέταλλα και χρησιμοποιούσαν βότανα, αρώματα και φυτικά σκευάσματα για ιατρικούς σκοπούς. Η Κινέζικη αλχημεία ήταν ένα μίγμα πρακτικών εφαρμογών και Ταοϊστικών δοξασιών για τις ιδέες της ισορροπίας και της αρμονίας. Επίσης, πολλές κινεζικές αλχημιστικές πρακτικές σχετίζονταν με την ολιστική προσέγγιση της παραδοσιακής Κινέζικης ιατρικής για την υγεία του ανθρώπου, σύμφωνα με την οποία ακόμη και ορυκτά και ανόργανα υλικά μπορούν να συμβάλλουν σε θεραπευτικές τεχνικές.
Υπάρχουν ιστορικές ενδείξεις ότι οι Κινέζοι ενδιαφέρονταν για την αλχημεία από τον 4ο αιώνα π.Χ. 'Ηδη από το 175 π.Χ. είχε εκδοθεί επίσημο διάταγμα που προειδοποιούσε τους αλχημιστές να μην κατασκευάζουν κίβδηλα χρυσά νομίσματα, πράξη που θα επέσυρε τη θανατική τους καταδίκη.
'Οπως και στις άλλες περιοχές του πλανήτη, ο χρυσός και η μετατροπή άλλων ευτελών μετάλλων σε χρυσό ήταν ένας από τους κύριους στόχους πολλών Κινέζων αλχημιστών. Υπάρχουν αναφορές για έναν αλχημιστή, ονομαζόμενο Zou Yan (305 - 240 π.Χ.), που υπόσχονταν σε πλούσιους Κινέζους και άρχοντες πρόσθετα πλούτη, δύναμη και τιμές, όπως και την ικανότητα επίκλησης υπερφυσικών δυνάμεων για να πετύχουν οι ηγεμονικές τους επιδιώξεις.

Ο μετασχηματισμός φθηνών μετάλλων σε χρυσό υπήρξε ένας από τους κύριους στόχους των αλχημιστών όλου του κόσμου. Ποτέ δεν μπόρεσε η Χημεία μόνη της να το πετύχει, ωστόσο η επιδίωξη αυτή προσέφερε πολλές νέες γνώσεις.
'Ενας άλλος αλχημιστής παρουσιάσθηκε το 133 π.Χ. στο βασιλικό παλάτι υποσχόμενος το ελιξίριο της αθανασίας. Η ιδέα της παράτασης της ζωής και της αθανασίας είχε γίνει το κεντρικό σημείο δράσης πολλών Κινέζων αλχημιστών, κατά τρόπον αντίστοιχο της ιδέας της Φιλοσοφικής Λίθου (Philosopher's Stone) των αλχημιστών στη Δύση. Ιστορικά ντοκουμέντα δείχνουν ότι το 60 π.Χ. ο αυτοκράτορας Suan ανέθεσε σε έναν αλχημιστή, με το όνομα Liu Tsiang, να χρησιμοποιήσει τις δυνάμεις του για να αυξήσει τα χρόνια ζωής του με την παρασκευή αλχημιστικού χρυσού. Αν και απέτυχε να πραγματοποιήσει τις υποσχέσεις του, μόλις απέφυγε την εκτέλεση.
Το αρχαιότερο κινεζικό αλχημιστικό κείμενο πάνω γράφτηκε από τον Wei Po Yang (140 μ.Χ.). Σε αυτό γίνεται αναφορά στις αντίθετες, πλην όμως συμπληρωματικές δυνάμεις Yin και Yang. Η Κινέζικη αλχημεία δανείστηκε πολλές ιδέες από τον παραδοσιακή ιατρική που στηρίζονταν στις βασικές αρχές του Ταοϊσμού. Η φιλοσοφία αυτή στηρίζονταν στην αντίληψη των αντίθετων δυνάμεων, το Yin και Yang, που τα θεωρούσαν ενεργά στοιχεία (Yin = αρσενικό - ενεργό, Yang = θηλυκό - παθητικό).

Πανάρχαιο φιλοσοφικό σύμβολο αρμονίας και Yin Yang
Το Yin Yang είναι ένα πανάρχαιο σύμβολο. Εμφανίστηκε για πρώτη φορά σε κινέζικα ιστορικά έγγραφα ηλικίας περίπου 3000 χρόνων. H αυθεντική ονομασία του συμβόλου αυτού, που όλοι οι άνθρωποι είναι οικείοι μαζί του με την ονομασία Yin Yang, είναι Tai Chi Tu.
Στο Yin Yang o κύκλος συμβολίζει την ολότητα και το άπειρο του Chi (ζωτική ενέργεια). Δεν υπάρχει ούτε αρχή ούτε τέλος, διαπερνά μέσα από την ολότητα. Ο εξωτερικός αυτός κύκλος είναι το Σύμπαν που εμπεριέχει το Yang (φως) και το Yin (σκοτάδι). Η διαχωριστική γραμμή ανάμεσα σε αυτούς τους δύο κυκλικούς τομείς είναι καμπυλοειδής. Αυτό δηλώνει μια αέναη κίνηση και ροή του Yin μέσα στο Yang και αντίστροφα. H αναλογία των χρωμάτων είναι ίδια, επομένως τα δύο στοιχεία εξισορροπούν μεταξύ τους.
Οι Κινέζοι αλχημιστές έγραψαν αρκετά έργα Αλχημείας (Ko-Huang, 254-334 μ.Χ.), με περιγραφές χημικών διεργασιών που αφορούσαν την παρασκευή διάφορων υλικών, ελιξίριων ζωής, τον "μετασχηματισμό" μετάλλων και την περιγραφή βοτάνων με μαγικές θεραπευτικές ιδιότητες. Γνώριζαν το κιννάβαρι (HgS), τις θειούχες ενώσεις του αρσενικού (ερυθρά σανδαράχη, As2S2, και κίτρινη σανδαράχη, As2S3), την κιμωλία, χρωστικές από τα όστρακα των μυδιών (πορφύρα), το θείο, την πυρίτιδα, την άσφαλτο και πλήθος αλάτων. Επίσης περιγράφουν διάφορες τεχνικές μετασχηματισμού ευτελών μετάλλων σε χρυσό. Σε όλες αυτές τις διαδικασίες χρησιμοποιούσαν τεχνικές απόσταξης, σύντηξης και εξάχνωσης.
Ο αριθμός πέντε φαίνεται πως υπήρξε ο ιερός αριθμός της κινεζικής αλχημείας. Οι Κινέζοι αλχημιστές υποστήριζαν την ύπαρξη πέντε στοιχείων: ξύλο, πυρ, γη, μέταλλο και νερό και τα συνδυάζανε με πέντε χρώματα. Επίσης είχαν πέντε κατευθύνσεις (πορείες) που τα συνέδεαν με πέντε μέταλλα: χρυσός, άργυρος, μόλυβδο, χαλκό και σίδηρο. Ως αποτέλεσμα, κάθε αλχημιστική τεχνική διακρινόταν σε πέντε στάδια.



Χρήση νερόμυλου για τη διαβίβαση αέρα σε υψικάμινο χάλυβα
Παρασκευή χάλυβα, στάδιο απομάκρυνσης σκωρίας
Μεταλλικά κινεζικά σπαθιά (τα περισσότερα από σίδηρο)
Πηγές από το Διαδίκτυο: (1) "Ancient Chinese Alchemy" (Experiment-Resorces.com). (2) "Chemistry in Ancient China: Alchemy" (Hu Zhang)



Geber (Jaber Ibn Hayan, 721(;)-815, Βαγδάτη)
Αβικένας (Ibn Sina Avicenna,
980 -1037, Περσία)
Αβερρόης (Ibn Rushd Averroes, 1126 Cordova Ισπανίας - 1198, Marrakes)
8. Ιστορία της Χημείας στις Αραβικές Χώρες και Αλχημεία
Οι 'Αραβες χρησιμοποίησαν με επιτυχία πρώτοι τις διάφορες ανακαλύψεις, που παρέλαβαν από τους Ινδούς, τους Κινέζους και τους Αιγύπτιους (πυρίτιδα, πυξίδα, χαρτί, άρδευση χωραφιών, αρώματα, χρωστικές ύλες, καλλιέργεια δένδρων) και τα μετέφεραν στην Ευρώπη, όταν κατέλαβαν την Ισπανία. Οι 'Αραβες δεν μετέφεραν απλώς γνώσεις από την Ανατολή, αλλά συνέβαλαν ουσιαστικά στη Χημεία, όπως και σε άλλες θετικές επιστήμες, μια εποχή (μεσαίωνας 700-1400 μ.Χ.), που στην Ευρώπη κυριαρχούσαν η δεισιδαιμονία και οι θρησκευτικές προκαταλήψεις.
Αραβική ανακάλυψη είναι ένα πλήθος χημικών αντιδραστηρίων, που στη συνέχεια χρησιμοποίησαν οι Ευρωπαίοι αλχημιστές, όπως το νιτρικό και το θειικό οξύ και η ποτάσα (potash, K2CO3). Επίσης, τελειοποίησαν πολλές τεχνικές, όπως την υφαντουργία, τη μεταλλουργία, την παρασκευή χρωστικών υλών, την αγγειοπλαστική, την υαλουργία και την αρωματοποιία. Ονομαστά αραβικά προϊόντα ήταν τα λινά υφάσματα, οι μουσελίνες της Μοσούλης και τα περίφημα ξίφη της Δαμασκού, για τα οποία η μεταλλουργική τεχνική κατασκευής τους παραμένει ακόμη ένα επιστημονικό αίνιγμα.
Επίσης, οι 'Αραβες ανακάλυψαν σπουδαίες θεωρίες και τεχνικές για την ιατρική, τη γεωμετρία, την αστρονομία. Επινόησαν την άλγεβρα (al-jabr: επανόρθωση, αποκατάσταση), μελέτησαν το εκκρεμές και εισήγαγαν τα ψηφία-σύμβολα του δεκαδικού συστήματος αρίθμησης (αραβικά ψηφία). Τέλος, συνέβαλαν στην ανάπτυξη της οπτικής και της τριγωνομετρίας και βέβαια της αλχημείας.
Μέχρι την περίοδο των Αράβων, η αλχημεία ήταν ένα μίγμα φιλοσοφικών θεωριών, αλληγοριών, συμβόλων και κωδικοποιημένων γλωσσών. Κατά την περίοδο των Αράβων (από τον 8ο αιώνα μ.Χ. και μετά), η αλχημεία άρχισε να γίνεται μια συστηματική τεχνική με συγκεκριμένες πρακτικές πλευρές.

Τα περίφημα χαλύβδινα "Δαμασκηνά σπαθιά" (Damascus' swords), με τα χαρακτηριστικά μοτίβα τους, υπήρξαν διάσημα για την αντοχή τους και την εξαιρετικά αιχμηρή λεπίδα τους. Η παράδοση λέει ότι μπορούσαν με ένα κτύπημα να κόψουν τα ευρωπαϊκής κατασκευής σπαθιά, όπως και βράχους. Η κατασκευή τους (1100-1700 μ.Χ.) παραμένει ένα μυστήριο παρά το πλήθος των σχετικών ερευνών.
Ο 'Αραβας Τζαμπίρ Ιμπν Χαγιάν (Jaber Ibn Hayan, 721(;)-815, Βαγδάτη), μετέπειτα γνωστός στην Ευρώπη ως Geber, γνωστός και ως ο πρώτος των αλχημιστών, εισήγαγε τη μεθοδική και πειραματική προσέγγιση μιας αλχημιστικής επιστημονικής έρευνας που πραγματοποιούνταν σε ένα εργαστήριο. Ο Geber θεωρείται ως ο πατέρας της Αλχημείας. Ο Geber θεωρούσε ότι όλα τα μέταλλα αποτελούνταν από υδράργυρο και θείο και ότι ο υδράργυρος καθόριζε τη μεταλλικότητά τους και το θείο την αναφλεξιμότητά τους.
Οι ανακαλύψεις του Geber υπήρξαν πολύ σημαντικές και καταγράφηκαν στα πολυάριθμα βιβλία και σημειώσεις που άφησε. Μεταξύ άλλων, ανακάλυψε την ποτάσα, περιέγραψε μέθοδο απομόνωσης του καυστικού νατρίου, όπως και των ισχυρών οξέων, δηλ. του θειικού, του νιτρικού και του υδροχλωρικού οξέος. Στον Geber αποδίδεται η απομόνωση του αρσενικού και του αντιμονίου. Βελτίωσε τις τεχνικές κρυστάλλωσης, απόσταξης, σύντηξης, εξάχνωσης και εξάτμισης. Επίσης, εφηύρε ένα είδος άκαυστου χαρτιού, βρήκε ένα τρόπο προστασίας του σιδήρου από την οξείδωση, όπως ένα τρόπο διαχωρισμού του χρυσού από τον άργυρο με τη βοήθεια οξέων.
Πιστεύεται ότι ο Geber έγραψε πάνω από 200 βιβλία, τα οποία για αιώνες υπήρξαν για τους Ευρωπαίους αλχημιστές πηγές ανεκτίμητων πληροφοριών για διάφορες χημικές ουσίες.
O διάσημος 'Αγγλος φιλόσοφος και αλχημιστής Roger Bacon (1214-1294) τον αναγνώρισε ως τον πρωτοπόρο δάσκαλο της επιστήμης της Χημείας, ενώ, πολύ αργότερα, ο Γάλλος χημικός Marcellin Berthelot (1827-1907) είπε ότι ο Αριστοτέλης καθιέρωσε τη φιλοσοφία της λογικής και ο Geber τη Χημεία.
Ονομαστοί 'Αραβες φιλόσοφοι και ιατροί ήταν ο Αβικένας (Ibn Sina Avicenna, 980 -1037, Περσία) και ο Αβερρόης (Ibn Rushd Averroes, 1126 Cordova Ισπανίας - 1198 Marrakes, Μαρόκο). O Αβικένας είχε συντάξει ένα μεγάλο κατάλογο των μέχρι τότε γνωστών ουσιών, όπου περιέγραφε και τη φαρμακολογική δράση τους. Ο Αβερρόης έγραψε μια ιατρική εγκυκλοπαίδεια και σχεδόν για όλα τα έργα του Αριστοτέλη. Πρέπει να σημειωθεί ότι οι 'Αραβες θεωρούσαν τον Αριστοτέλη μεγάλο φιλόσοφο, τα έργα του οποίου διασώθηκαν και έγιναν γνωστά στην Ευρώπη από αραβικές μεταφράσεις και σχολιασμούς.
Αυτοί οι 'Αραβες σοφοί θεωρούνται ότι ήταν οι πρώτοι που ασχολήθηκαν συστηματικά με τη Χημεία και τις χημικές τεχνικές και συνέβαλαν αποφασιστικά στην πρόοδο της επιστήμης της Χημείας. Διέσωσαν τις αρχαίες γνώσεις αλχημείας και τις εμπλούτισαν. Ωστόσο, δεν υπήρξαν αποκλειστικά αλχημιστές. Αυτοί οι άνθρωποι ήταν στην κυριολεξία "πανεπιστήμονες", ήταν φιλόσοφοι και συγχρόνως γιατροί, θεολόγοι και συγχρόνως φυσικοί και μαθηματικοί, ποιητές και συγχρόνως μηχανικοί. 'Ηταν ένα σπάνιο είδος ανθρώπων, που συνέβαλαν αποφασιστικά στην πρόοδο της ανθρωπότητας.
Πηγές από το Διαδίκτυο: (1) "Ibn Rushd: Bridging Islamic Traditions and Greek Thought" (Martin Nick). (2) "Geber (Abu Musa Jabir ibn Hayyan)". (3) "Islamic Alchemy - The History of Chemistry" (experiments-rsources.com)



Το πιο γνωστό "χημικό επίτευγμα" των Βυζαντινών χρόνων, σίγουρα είναι το περίφημο "υγρό πυρ" (greek fire). Η σύνθεση του ήταν επτασφράγιστο μυστικό και μόνο εικασίες ως προς αυτήν μπορούν σήμερα να γίνουν. Δεν φαίνεται πάντως να ήταν ένα απλό καύσιμο μίγμα νάφθας και θείου. Υπάρχουν μαρτυρίες που αναφέρουν την αυτανάφλεξή του όταν ερχόταν σε επαφή με το νερό. 'Ετσι, διατυπώθηκε η υπόθεση ότι ένα δραστικό συστατικό του θα πρέπει να ήταν το φωσφίδιο του ασβεστίου (Ca3P2). Το φωσφίδιο αυτό σε επαφή με το νερό υδρολύεται παρέχοντας το αέριο φωσφίνη (PH3). Η φωσφίνη αυταναφλέγεται στον αέρα προκαλώντας ανάφλεξη και στα υπόλοιπα καύσιμα υλικά του μίγματος. Τώρα, το πώς θα μπορούσε να παρασκευασθεί το φωσφίδιο (που απαιτεί ισχυρότατα αναγωγικές συνθήκες ή ακόμη και μεταλλικό ασβέστιο για τη σύνθεσή του) παραμένει μυστήριο.

'Αμβυκας: Η τυπική διαχρονική συσκευή απόσταξης σε διάφορες "εκδοχές" (αρχαία ελληνική λέξη: άμβυξ, αραβική παραλλαγή: al ambic ή alambic και ως αντιδάνειο: λαμπίκος ή λαμπίκο).

Αλχημιστής σε αναζήτηση της Φιλοσοφικής Λίθου. Ζωγραφικός πίνακας (1771) του Joseph Wright, όπου απεικονίζεται ο αλχημιστής Hennig Brand (1630-1710)να ανακαλύπτει τον φωσφόρο. Αυτό συνέβη "κατά λάθος", όταν ο Brand αναζητούσε τη Φιλοσοφική Λίθο στο στερεό υπόλειμμα μεγάλης ποσότητας ούρων.
9. Ιστορία της Χημείας κατά την Περίοδο των Αλχημιστών
Η λέξη Αλχημεία, όπως αναφέρθηκε στην εισαγωγή, προέρχεται από το οριστικό αραβικό άρθρο Αλ και τη Χημεία. Λιγότερο πιθανές, αλλά ενδιαφέρουσες είναι άλλες θεωρίες για την προέλευσή της. 'Ετσι, πολλοί πιστεύουν ότι έχει κινεζική προέλευση ή ακόμη και ελληνική (Αριστοτέλης: 'Εστι δε πάσι αρχή μία και ουσία: Αρχή μία
Η ανάπτυξη της Αλχημείας και των αλχημιστών ήταν κάτι το αναμενόμενο κατά τον Μεσαίωνα, αφού οι ειδικές γνώσεις σε θέματα μεταλλουργίας γενικά και χρήσεις των φαρμακευτικών βοτάνων για τη θεραπεία ασθενειών, υπήρξαν πάντοτε σημαντικοί παράγοντες πλουτισμού. Η επιστήμη της Χημείας από αντικείμενο επιστημονικής γνώσης και αναζήτησης μετατράπηκε σε εμπορευματικό προϊόν με μεγάλη ζήτηση και χρηματική αξία.

Το αλχημιστικό σύμβολο της φιλοσοφικής λίθου (σύνθεση άλλων επιμέρους συμβόλων).
Οι αλχημιστές πίστευαν ότι υπάρχουν τέσσερα βασικά στοιχεία-ουσίες: η φωτιά, ο αέρας, η γη και το νερό και τρία αιθέρια στοιχεία: το θειάφι, το αλάτι και ο υδράργυρος. Η Αλχημεία ήταν ιδιαίτερα διαδεδομένη στην μεσαιωνική Ευρώπη. Πολλά από τα αλχημιστικά βιβλία ήταν γεμάτα με ανούσια μαγικά ξόρκια, επικλήσεις και άλλα αποκρυφιστικά στοιχεία.
Οι σημαντικότεροι στόχοι των αλχημιστών ήταν η ουτοπική μετατροπή (μετουσίωση) των κοινών μετάλλων σε χρυσό ή ασήμι, όπως και η δημιουργία του ελιξιρίου της ζωής (από την αρχαία ελληνική λέξη: ξήριον -ουσία που "ξηραίνει" τα τραύματα- και στη συνέχεια την αραβική: el iksir), το οποίο θα θεράπευε όλες τις ασθένειες και θα παρέτεινε τη ζωή του ανθρώπου. Η Φιλοσοφική Λίθος (lapis philosophorum) ήταν μια μυθική ουσία και βασικό συστατικό για την επίτευξη των στόχων αυτών. Για τους αλχημιστές αντιπροσώπευε το πέμπτο στοιχείο ή την πέμπτη ουσία ή την πεμπτουσία (quinta essentia ή quintessence), την ύπαρξη της οποίας δεχόταν ο Αριστοτέλης. Επίσης, οι αλχημιστές αναζητούσαν ένα παγκόσμιο διαλύτη, δηλαδή μια ουσία που θα μπορούσε να διαλύσει κάθε άλλη (azoth, alkahest). 'Ολες αυτές οι ουτοπικές έννοιες και ουσίες συχνότατα συγχέονται μεταξύ τους και σημαίνουν το ίδιο πράγμα και συνδυάζουν όλες τις παραπάνω ιδιότητες.
Οι αλχημιστές δεν επεδίωκαν μόνο τη βελτίωση κάποιων ιδιοτήτων των υλικών ή την παράταση του χρόνου ζωής, αλλά έδιναν και μια πνευματική διάσταση στις αναζητήσεις τους. Για παράδειγμα, η μετατροπή του "ευτελούς" μολύβδου σε "ευγενή" χρυσό, παραλληλιζόταν με την ψυχική ανύψωση και τον εξευγενισμό του πνεύματος.
Τα εργαστήρια των αλχημιστών ήταν γεμάτα με όργανα απόσταξης, φούρνους, φιάλες με χημικές ουσίες, διαλύτες και οξέα και πολλά συγγράμματα χημείας κυρίως Αραβικής προέλευσης. Πολλές υπήρξαν οι "παράπλευρες" χημικές ανακαλύψεις των αλχημιστών κατά τη διάρκεια των παράδοξων αναζητήσεών τους. Τυπικό παράδειγμα αποτελεί η ανακάλυψη του φωσφόρου (1669) από τον Γερμανό αλχημιστή Hennig Brand (1630-1710), όταν θέρμανε σε υψηλή θερμοκρασία το στερεό υπόλειμμα, που συνέλεξε μετά την εξάτμιση μιας μεγάλης ποσότητας ούρων. Προφανώς, στην υψηλή θερμοκρασία του φούρνου πραγματοποιήθηκε αναγωγή των φωσφορικών αλάτων από τον άνθρακα των οργανικών ουσιών του υπολείμματος. 'Οταν διαπίστωσε αυτή η κηρώδης ουσία καιγόταν με έντονο λαμπρό φως και κυρίως ότι από μόνη της λαμποκοπούσε στο σκοτάδι, την ονόμασε phosphorus mirabilis (θαυμαστή ουσία που φέρει φώς).
Οι αλχημιστές συνήθιζαν να κρατούν ως επτασφράγιστα μυστικά τις λεπτομέρειες των τεχνικών τους και να κρατούν σημειώσεις με "κρυπτογραφικά" σύμβολα. Αυτό είχε ως αποτέλεσμα να ταυτιστούν με μυστικιστικές ομάδες και συντεχνίες με "ύποπτους σκοπούς". Αλλά και οι ίδιοι οι αλχημιστές, τις περισσότερες φορές σκόπιμα και για λόγους εντυπωσιασμού και βιοπορισμού, δεν επεδίωξαν να διαχωρίσουν την "τέχνη" τους από το υπερφυσικό, το μαγικό και τη δεισιδαιμονία.
Οι αλχημιστές υπέστησαν πολλούς διωγμούς ανά τους αιώνες (συχνότατα δικαιολογημένους) και η εξάσκηση της αλχημιστικής τέχνης πολλές φορές απαγορεύτηκε από θεσμικά πρόσωπα όπως ο Πάπας Ιωάννης XXII (1317) ή ο Ερρίκος ο IV της Αγγλίας (1403).



Αριστερά-μέσον: Δύο από τις άφθονες ζωγραφικές απεικονίσεις αλχημιστών και των εργαστηρίων. Δεξιά: Ο δρόμος των αλχημιστών ή ο δρόμος του χρυσού (Zlata Ulicka, Golden Lane). Ένας στενός δρόμος με μικρά σπιτάκια-εργαστήρια χρυσοχόων, που βρίσκονται μέσα στο κάστρο της Πράγας. Ο θρύλος λέει ότι εκεί ζούσαν και αλχημιστές (στην πραγματικότητα αυτοί βρίσκονταν σε άλλα μέρη του κάστρου). Οι ηγεμόνες της Βοημίας (σημερινής Τσεχίας) κρατούσαν χρυσοχόους και αλχημιστές σε μια κατάσταση ημιαιχμαλωσίας και συνεχούς επιτήρησης.
Οι αλχημιστές αποτυπώνονταν σε έργα ζωγραφικής ή περιγράφονταν σε κείμενα ως άνθρωποι αναξιόπιστοι. Δεν ήταν λίγες οι φορές που Ευρωπαίοι ηγεμόνες πλήρωναν αδρά αλχημιστές για να τους εξασφαλίσουν "φθηνό" χρυσό ή ελιξίρια μακροζωίας. Δεν ήταν ακόμη λίγες οι φορές που αλχημιστές-απατεώνες ζητούσαν ποσότητες γνήσιου χρυσού από τους ηγεμόνες αυτούς για να τον χρησιμοποιήσουν ως "προζύμι" στα πειράματά τους και τελικά εξαφανίζονταν με τον χρυσό αυτό.
Μετά τις σημαντικές επιστημονικές ανακαλύψεις της Χημείας από τον 18ο αιώνα και μετά, η μεταστοιχείωση με καθαρά χημικά μέσα έχει αποκλεισθεί οριστικά, όπως και η ύπαρξη της φιλοσοφικής λίθου. Ωστόσο, ακόμη και σήμερα γίνεται μερική χρήση αλχημιστικών θεωριών, σε θεραπευτικές πρακτικές όπως είναι η ομοιοπαθητική, η αρωματοθεραπεία και η κρυσταλλοθεραπεία.




Roger Bacon (1214-1294), 'Αγγλος
Albertus Magnus (1193/1206-1280), Βαυαρός
Nicolas Flamel (1330-1418), Γάλλος
Paracelsus (1493-1541), Ελβετός
Μεταξύ των πιο διάσημων αλχημιστές όλων των εποχών (πέραν από τους προαναφερθέντες Geber, Αβικένα και Αβερρόη) θεωρούνται οι: Wei Boyang (Κίνα), που έκανε την πρώτη γραπτή αναφορά για την πυρίτιδα (142 μ.Χ.), ο Ζώσιμος ο Πανοπολίτης ('Ελληνας ή Αιγύπτιος, 4ος-5ος αιώνας μ.Χ.), ο Muhammad ibn Zakariya al-Razi (Περσία, 865-925 μ.Χ.), διάσημος φαρμακοποιός και γιατρός της εποχής του, ο Nagarjuna (Ινδία, 10ος αιώνας μ.Χ.), διάσημος μεταλλουργός (συνέγραψε διατριβή για τον υδράργυρο).
Διάσημοι δυτικοευρωπαίοι αλχημιστές ήταν ο Βαυαρός Albertus Magnus, (1193/1206-1280), ο 'Αγγλος Roger Bacon (1214-1294) γνωστός και ως "Doctor Mirabilis" (: ο θαυμάσιος δάσκαλος), ο Γάλλος Nicolas Flamel (1330-1418) και ο Ελβετός Θεόφραστος Παράκελσος (Theophrastus Bombastus von Hohenheim, 1493-1541).
Ο Παράκελσος θεωρείται ένας από τους μεγαλύτερους αλχημιστές, αστρολόγους, και αποκρυφιστές όλων των εποχών. Ωστόσο, ήταν και από τους πρώτους αλχημιστές που πίστεψε ότι η αναζήτηση της φιλοσοφικής λίθου για την παρασκευή χρυσού ήταν ματαιοπονία και ότι οι αλχημιστές θα έπρεπε να στρέψουν την έρευνά τους στην αναζήτηση φαρμάκων. Ήταν ο πρώτος ο οποίος δίδαξε ότι η ζωή η ίδια δεν είναι παρά μια σειρά χημικών διεργασιών και ότι κάθε αρρώστια στην ουσία είναι μια χημική δυσλειτουργία.
Θεωρείται ως ο "πατέρας" της τοξικολογίας και είχε διατυπώσει την περίφημη φράση "η δόση κάνει το δηλητήριο" (dosis facit venemum). Το 1536, εξέδωσε το Die grosse Wundartzney (το μεγάλο βιβλίο της Χειρουργικής). Ως σημαντικότερο έργο του θεωρείται το Philosofia sagax (υπάρχει και με τον τίτλο Astronomia magna, που είναι γραμμένο στα γερμανικά).
Μετά το θάνατό του Παράκελσου, το επιστημονικό έργο του άρχισε να αναγνωρίζεται και να εκτιμάται από πολλούς ιατρούς της Γερμανίας και της Γαλλίας, οι οποίοι του προσέδωσαν την προσωνυμία του "Λούθηρου της Ιατρικής". Αντίθετα οι εχθροί του, που δημιούργησε αρνούμενος να δεχθεί τις αντιλήψεις των ιατρών της εποχής του, τον αποκαλούσαν "φιλόσοφον ά-λογον" (χωρίς λογική) και τα δε ιατρικά του συγγράμματα ως προϊόντα διανοητικής ανισορροπίας.
Πηγές από το Διαδίκτυο: (1) "Alchemy" (Wikipedia). (2) "The Alchemy web site on Levity.com".







Οι θεμελιωτές της σύγχρονης Χημείας: Robert Boyle (1627-1691) και
Antoine Lavoisier (1743-1794)
10. Η Χημεία κατά τον 17ο και 18ο Αιώνα
Η ιστορία της Χημείας με τους αλχημιστές είχε φτάσει στα όρια μιας ψευδο-επιστήμης με πολλές δεισιδαιμονίες, παρανοήσεις και τυφλά πειράματα για χημικές μετατροπές που δεν έδιναν αποτελέσματα ή έδιναν, αλλά δεν ήταν τα επιζητούμενα και συχνά αγνοούνταν. Οι πρωτοπόροι και "πατέρες" της πραγματικής επιστήμης της Χημείας, με πραγματικά πειράματα, παρατήρηση, λεπτομερή καταγραφή μετρήσεων, αλλά και με έλεγχο της ακρίβειας των μετρήσεων, θεωρούνται ο Robert Boyle (1627-1691) στην Αγγλία και ο Antoine Lavoisier (1743-1794) στη Γαλλία.
Η σύγχρονη λέξη Χημεία εδραιώνεται τον 17ο αιώνα με το έργο του Robert Boyle, που θεωρείται ως ο τελευταίος των αλχημιστών και συγχρόνως ο πρώτος των χημικών, στο βιβλίο που εξέδωσε το 1661 "Ο Σκεπτικιστής Χυμικός" (The Skeptical Chymist), που έγινε βασικό σύγγραμμα-οδηγός για τους χημικούς που ακολούθησαν. Το πλήρες βιβλίο είναι διαθέσιμο στο διαδίκτυο από εδώ (βιβλιοθήκη του Πανεπιστημίου της Πενσυλβάνιας).
Ο Robert Boyle ήταν κατά τον 17ο αιώνα ένας φυσικός φιλόσοφος (όπως αποκαλούνταν οι επιστήμονες την εποχή εκείνη) με γνώσεις φυσικής, χημείας και θεολογίας.
Αν και επικρατούσε σε όλους τους πειραματιστές της εποχής εκείνης μια μηχανοκρατική αντίληψη, ο Robert Boyle προχώρησε περισσότερο από οποιονδήποτε χημικό της γενιάς του, αμφισβητώντας τη δομή της επικρατούσας χημικής θεωρίας. Ο μεγάλος αυτός ερευνητής χρησιμοποίησε χημικές μεθόδους για να αποδείξει ότι διαφορετικά σώματα διασπώνται σε διαφορετικές ουσίες. Ο Robert Boyle δεν ξέφυγε πολύ από τις επικρατούσες αντιλήψεις (δηλ. την πεποίθηση ότι υπήρχαν "άτομα" φωτιάς) που σχετίζονταν με την καύση και την αναπνοή των ζώων. Μετά από πολλές περιηγήσεις σε διάφορες χώρες κατέληξε στην Οξφόρδη το 1667, όπου εφηύρε την αντλία αερίων. Με την αντλία αυτή έκανε πειράματα σε κενό και διατύπωσε τους νόμους των αερίων, την περίφημη σχέση PV = σταθερά, υπό σταθερή θερμοκρασία, μια κοινή γνώση σήμερα, σημαντικό όμως εύρημα για εκείνη την εποχή.



O Johannes (John) Mayow (1641-1679) και τα σκεύη που χρησιμοποιούσε για τα περίφημα πειράματά του πάνω στην αναπνοή των ζώων
Ο Robert Hooke (1635-1703) και το μικροσκόπιό του. 'Ισως δεν είναι ευρύτερα γνωστό ότι είναι ο πρώτος που παρατήρησε τα κύτταρα. Ο όρος cell (για τα κύτταρα) οφείλεται στον Hook. Με τον όρο cell (κελί) ήθελε να παρομοιάσει τα κύτταρα με τα κελιά των μοναχών.
Ο Robert Boyle συνεργάσθηκε με τους επίσης φυσικούς φιλόσοφους της Οξφόρδης, τον Robert Hooke (1635-1703), έναν πανεπιστήμονα (φυσικός, χημικός, βιολόγος, αστρονόμος, μηχανικός, αρχιτέκτονας), ευρύτερα γνωστό κυρίως από τον νόμο της ελαστικότητας ο οποίος φέρει το όνομά του, όπως και τον John Mayow (1641-1679). Αυτοί οι δύο ερευνητές πραγματοποιούσαν μελέτες, ο πρώτος στα προϊόντα καύσης ενός κεριού και ο δεύτερος στην αναπνοή των ζώων, κλείνοντας τα πειραματόζωά του μέσα σε ένα δοχείο. Και στις δύο περιπτώσεις παρατηρούσαν όμοια αποτελέσματα και κατέληγαν στο συμπέρασμα ότι για να διατηρηθεί τόσο η καύση, όσο και η αναπνοή σε ένα κλειστό χώρο, ήταν απαραίτητη η συνεχής παροχή αέρα, αλλιώς το κερί θα έσβηνε και το ζώο θα πέθαινε.
Την ουσία που συντηρούσε την καύση ονομάστηκε από τον Mayow νιτρο-αερώδες πνεύμα (spiritu nitro-aereo), επειδή ο ερευνητής (σωστά) συσχέτιζε τα φαινόμενα αυτά με κάποιες ουσίες που περιέχονται στο "νίτρο" (KNO3). Ο Mayow θεωρούσε ότι το νιτρο-αερώδες πνεύμα είχε σχέση με τους σεισμούς, τους κεραυνούς και την κατάψυξη. Χρειάστηκαν άλλα 100 χρόνια για να ανακαλυφθεί το οξυγόνο από τον Lavoisier και να γίνει αντιληπτό ότι αυτό το αέριο τροφοδοτούσε την καύση και τη ζωή.


Οι θεμελιωτές της φλογιστικής θεωρίας: Johann Joachim Becher (1635-1682) και Georg Ernst Stahl (1660-1734).
10.1. Φλογιστική θεωρία. Το 1667 δύο Γερμανοί αλχημιστές - χημικοί, οι Johann Joachim Becher (1635-1682) και Georg Ernst Stahl (1660-1734), δημιούργησαν τη μυστικιστική θεωρία για το φλογιστόν (phlogiston) για να ερμηνεύσουν το φαινόμενο της καύσης. Σύμφωνα με τη θεωρία τους υπάρχει μια ιδιαίτερη μορφή ύλης, μια ουσία, το φλογιστόν, η οποία βρίσκεται σε κάθε υλικό που μπορεί να καεί. Το φλογιστόν χάνεται στον αέρα εν μέρει ή συνολικά κατά την καύση της ουσίας.
Η αντίληψη ότι η φλόγα απομακρύνει κάτι από το καιόμενο σώμα υπήρχε ήδη από την αρχαιότητα. Η αντίληψη αυτή συναντάται στην αριστοτελική θεωρία των τεσσάρων στοιχείων "γη, ύδωρ, πυρ και αήρ", αλλά και στα έργα του Παράκελσου για τις δύο εκπνοές της Γης. Το καθαρό συμπέρασμα ήταν ότι ό,τι καίγεται περιέχει την ουσία "φλογιστόν", το οποίο αποβάλλει κατά την καύση. 'Ετσι ίσχυαν "αντιδράσεις" όπως:
ξύλο
κάρβουνο
'Οταν διαπιστώθηκε ότι για να υπάρξει καύση ήταν απαραίτητη και η παρουσία αέρα και ότι από αυτόν ένα μέρος ουσιαστικά δεν χρησιμοποιείται για τις καύσεις, εισήχθησαν οι έννοιες του φλογιστικοποιημένου (phlogistated), που στην ουσία ήταν το CO2, και του αποφλογιστικοποιημένου (dephlogistated) αέρα, που στην ουσία ήταν το Ο2, καθώς και του μεφιτικού αέρα (mephitic, από το λατινικό mephitis: τοξικός, δύσοσμος), που στην ουσία ήταν το Ν2. Οπότε ήταν:
ξύλο + κοινός αέρας
και κοινός αέρας = μεφιτικός αέρας + αποφλογιστικοποιημένος αέρας, οπότε:
φλογιστικοποιημένος αέρας = αποφλογιστικοποιημένος αέρας + φλογιστόν



Ο διάσημος 'Αγγλος φυσιοδίφης, θεολόγος, ιερέας και χημικός Joseph Pristley (1733-1804). Ο πρώτος που απομόνωσε το οξυγόνο, αν και δεν το αναγνώρισε ως ξεχωριστό στοιχείο, επηρεασμένος από τη φλογιστική θεωρία της οποίας υπήρξε ένθερμος οπαδός. Δεξιά: Τα σκεύη που χρησιμοποίησε στις μελέτες πάνω στα διάφορα "είδη" αέρα.
Η φλογιστική θεωρία επικράτησε ουσιαστικά σε όλη τη διάρκεια του 18ου αιώνα, αν και προς το τέλος του αιώνα άρχισαν να εμφανίζονται κάποιες ασυνέπειες στη δομή της. Για παράδειγμα, είχαν ήδη διαπιστώσει ότι ο "αποφλογιστικοποιημένος" υδράργυρος, δηλαδή το οξείδιο του υδραργύρου, μπορούσε με απλή θέρμανση να ξαναδώσει υδράργυρο χωρίς κάποια "πηγή φλογιστού", όπως π.χ. άνθρακα, που χρειαζόταν για να ληφθούν άλλα μέταλλα από τα οξείδιά τους.
Ακόμη, είχε πλέον διαπιστωθεί ότι η καύση των μετάλλων στον αέρα, οδηγούσε σε προϊόν μεγαλύτερου βάρους, σε αντίθεση με ό,τι συνέβαινε π.χ. με το ξύλο. Αυτό οδήγησε πολλούς να πιστεύουν ότι το φλογιστόν, που "έχαναν" κατά την καύση, μπορεί να είχε και αρνητικό βάρος. 'Ολα αυτά άρχισαν να δημιουργούν σοβαρά "ρήγματα" στη θεωρία του φλογιστού.
Θα πρέπει εδώ να τονιστεί ότι οι οπαδοί της θεωρίας του φλογιστού δεν ήταν παραδοξολόγοι και ευφάνταστοι αλχημιστές, ούτε τσαρλατάνοι. Οι περισσότεροι ήταν σοβαροί επιστήμονες που προσπαθούσαν να απαντήσουν σε βασικές χημικές ερωτήσεις πραγματοποιώντας προσεκτικά πειράματα και σχολαστικές μετρήσεις, αξιοποιώντας στον μέγιστο δυνατό βαθμό τις περιορισμένες γνώσεις της εποχής. Μεταξύ των πλέον διάσημων και ένθερμων υποστηρικτών της και μέχρι τέλους της ζωής του ήταν ο διάσημος Joseph Pristley (1733-1804), ο οποίος υπεράσπιζε τη θεωρία ακόμη και όταν οι "αντι-φλογιστές" (με επικεφαλής τον Lavoisier) φαινόταν ότι είχαν αρχίσει πλέον να επικρατούν.
Η φλογιστική θεωρία, όσο και αν για τα σημερινά δεδομένα μας φαίνεται εξαιρετικά παράδοξη, σε κάποιο βαθμό είχε πλησιάσει την αλήθεια. Το φλογιστόν στην ουσία αντιπροσώπευε την "τάση" ή τη "δίψα" μιας ουσίας να προσλάβει οξυγόνο. 'Ετσι, η αντίδραση μιας ουσίας με το οξυγόνο, αντί να γραφεί συμβατικά ως: Α + [Ο]
10.2. Μετρήσεις ακριβείας. Από τις αρχές του 18ου αιώνα οι ερευνητές άρχισαν να γίνονται πιο σχολαστικοί στα πειράματά τους και άρχισαν πλέον να κάνουν συστηματική χρήση του ζυγού. Την αρχή έκανε ο ο Σκωτσέζος χημικός Joseph Black (1728-1799), ο οποίος θεωρείται ως ο εφευρέτης του αναλυτικού ζυγού και άρχισε να περιγράφει τα πειράματά του παρουσιάζοντας ακριβείς ποσοτικές σχέσεις. Αλλά ο Antoine-Laurent Lavoisier (1743-1794), έκανε το ζύγισμα με ακρίβεια αναπόσπαστο τμήμα της επιστήμης της Χημείας και διέλυσε τους γρίφους της αλχημιστικής αντίληψης.
Ο Lavoisier σε ηλικία 26 ετών έγινε γνωστός όταν κατέρριψε τη μέχρι τότε επικρατούσα θεωρία ότι το νερό μετατρέπεται σε "γη" κατά την επαναλαμβανόμενη απόσταξη. Για 100 ημέρες έβραζε νερό και μετέφερε το απόσταγμα που συνέλεγε, ξανά στον βραστήρα, έτσι ώστε να μην υπάρχει κάποια απώλεια. Ζυγίζοντας την αποστακτική συσκευή με το νερό πριν και μετά την όλη διαδικασία, όπως και το στερεό υπόλειμμα που είχε μαζευτεί στην αποστακτική συσκευή, έδειξε ότι το στερεό αυτό προϊόν προερχόταν από τα γυάλινα σκεύη και όχι από το νερό.


Ο Σκωτσέζος χημικός Joseph Black (1728-1799) εισήγαγε τους ζυγούς ακριβείας (αναλυτικούς ζυγούς) στα χημικά εργαστήρια.
Το 1772, ο Lavoisier άρχισε να εξετάζει τον ρόλο του αέρα στην καύση. Με καύση διάφορων υλικών (P, S, Pb) σε κλειστά δοχεία και προσεκτικές ζυγίσεις (η ακρίβεια ζύγισης που είχε πετύχει ήταν 0,5 mg) διατύπωσε την σωστή άποψη ότι το υλικό που καίγεται δεν αποβάλλει φλογιστόν, αλλά ενώνεται με ένα μέρος του αέρα, δηλαδή οξειδώνεται.
Ο Lavoisier υπήρξε εισηγητής και ένθερμος υποστηρικτής της αντι-φλογιστικής θεωρίας. Σύντομα, το φλογιστόν δεν είχε πλέον θέση στη θεωρία και σταδιακά τέθηκε στο περιθώριο, παρά το ότι μερικοί αξιόλογοι ερευνητές της εποχής, όπως ο Pristley, συνέχισαν να το θεωρούν θεμέλιο της χημικής θεωρίας. Η φλογιστική θεωρία, παρά τις αντιφάσεις της, διατηρήθηκε για ορισμένο διάστημα γιατί εξυπηρετούσε ιδεολογικές αντιλήψεις μερικών γνωστών επιστημόνων της εποχής.

Ο Antoine Lavoisier και η σύζυγός του Marie-Anne (Πίνακας του Jacques-Louis David, 1788). Ο Lavoisier θεμελίωσε τη σύγχρονη Χημεία. Μεταξύ πολλών άλλων, απέδειξε με σχολαστικά πειράματα και διατύπωσε τον βασικό νόμο της Χημείας για τη διατήρηση της μάζας. 'Ομως καρατομήθηκε, αφού "Η Δημοκρατία δεν χρειαζόταν ούτε επιστήμονες, ούτε χημικούς".
Ο Lavoisier αργότερα κατέληξε στο συμπέρασμα ότι ο αέρας ήταν μίγμα αερίων, όπου το 20% ήταν ένα αέριο, που το ονόμασε οξυγόνο, χρήσιμο στην καύση ενώ το υπόλοιπο ήταν ένα αέριο που δεν μπορούσε να διατηρήσει την καύση. Το ονόμασε oxygenium, με βάση την εσφαλμένη αντίληψη της εποχής, ότι αποτελεί συστατικό όλων των οξέων, δηλαδή ότι είναι το στοιχείο που "παράγει οξέα". Το 1787, με το βιβλίο του Méthode de Nomeclature Chimique καθιέρωσε ένα μεθοδικό και συστηματικό τρόπο ονοματοδοσίας των χημικών στοιχείων. Το 1789 δημοσίευσε το πρώτο βασικό εγχειρίδιο Χημείας το Traité Elémentaire de Chimie.
Ο Lavoisier, αν και ενεργός υποστηρικτής της Γαλλικής επανάστασης, αφενός μεν λόγω της αριστοκρατικής του καταγωγής, αφετέρου λόγω της άτυχης επαγγελματικής ενασχόλησής του σε σώμα φοροεισπρακτόρων, συνελήφθη και καταδικάστηκε σε θάνατο κατά τα χρόνια της τρομοκρατίας του Ροβεσπιέρου.
'Ισως, η μοίρα του Lavoisier είχε σφραγισθεί από κάποια χρόνια πριν, όταν είχε απορρίψει ως απαράδεκτη μια "επιστημονική" εργασία του Jean-Paul Marat, ενός από τους φανατικότερους ηγέτες της Γαλλικής Επανάστασης κατά την περίοδο της τρομοκρατίας, στερώντας του τη θέση μέλους της Γαλλικής Ακαδημίας των Επιστημών.
'Οταν ζητήθηκε από το δικαστήριο να του χαριστεί η ζωή για να συνεχίσει τα πειράματά του, ο δικαστής απέρριψε την αίτηση με την περίφημη φράση: "Η Δημοκρατία δεν χρειάζεται ούτε επιστήμονες, ούτε χημικούς". Καρατομήθηκε αμέσως μετά την απόφαση, στις 8 Μαΐου του 1794, μαζί με άλλους 27 καταδικασμένους ανθρώπους. Το σώμα του ρίχτηκε σε έναν κοινό τάφο.
Ο μαθηματικός Lagrange σχολιάζοντας την είδηση της εκτέλεσης του Lavoisier είπε "χρειάσθηκε μια στιγμή για να κοπεί αυτό το σπάνιο κεφάλι, αλλά και εκατό χρόνια να περάσουν δεν θα γεννηθεί άλλο αντάξιό του".

Διεξαγωγή πειράματος στο εργαστήριο του Lavoisier πάνω στην ανθρώπινη αναπνοή (σκίτσο της Marie-Anne Lavoisier, που φαίνεται δεξιά να κρατά σημειώσεις).
10.3. Ανακάλυψη Αερίων. Σημαντικό στάδιο εξέλιξης της επιστήμης της Χημείας αποτέλεσαν οι πειραματικές προσπάθειες για την ανακάλυψη αερίων και της σύστασης του αέρα. Από το 1624 ο Φλαμανδός ιατρός Jan Baptist van Helmont (1579-1644) διαπίστωσε ότι υπάρχουν διαφορετικά αέρια με διαφορετικές ιδιότητες. Ο van Helmont ανακάλυψε το διοξείδιο του άνθρακα (CO2), ως προϊόν της καύσης ξύλου και άλλων οργανικών ενώσεων και αρχικά το ονόμασε ξυλαέριο (ονομάσθηκε δεσμευμένος αέρας, fixed air, και φλογιστικοποιημένος αέρας, phlogisticated air).
Ο van Helmont ήταν εκείνος που εισήγαγε τον όρο-λέξη gas στο επιστημονικό λεξιλόγιο για την περιγραφή των διαφόρων "ειδών" αερίων ή "πνευμάτων". Πρέπει να σημειωθεί ότι αυτή η κοινή πλέον λέξη σε πολλές γλώσσες (gas: αγγλικά, γερμανικά, ισπανικά, ιταλικά, gaz: γαλλικά, газа: ρωσικά), έχει Ελληνική ρίζα και προέρχεται από τη λέξη χάος.
Τα πειράματά του van Helmont βοήθησαν τον Joseph Black και αργότερα τον Lavoisier να προτείνουν ότι ο ατμοσφαιρικός αέρας δεν είναι ένα αέριο, αλλά είναι μίγμα αερίων. Η πρόταση αυτή ήταν πολύ τολμηρή για την εποχή της, αφού βρισκόταν σε αντίθεση με την αριστοτέλεια αντίληψη, ότι ο αέρας δεν είναι μίγμα, αλλά είναι ένα από τα τέσσερα στοιχεία (γη, πυρ, αέρας, νερό).

Πειραματική διάταξη που χρησιμοποίησε ο Pristley για την παρασκευή οξυγόνου με θέρμανση οξειδίου του υδραργύρου
Ο Ο Joseph Pristley παρασκεύασε, απομόνωσε και χαρακτήρισε πολλούς "αέρες", όπως: Τον νιτρώδη αέρα (nitrous air, δηλ. το NO), τον ατμό του πνεύματος του άλατος ή όξινο αέρα (vapor of spirit of salt, acid air, δηλ. το HCl), τον αλκαλικό αέρα (alkaline air, δηλ. την ΝΗ3), τον αποφλογιστικοποιημένο νιτρώδη αέρα (dephlogisticated nitrous air, δηλ. το N2O) και κυρίως τον αποφλογιστικοποιημένο αέρα (dephlogisticated air, δηλ. το Ο2). 'Ετσι, αν και απομόνωσε το οξυγόνο (με θερμική διάσπαση του HgO στους 350 ºC), δεν αναγνώρισε τη στοιχειακή του φύση ως οπαδός της φλογιστικής θεωρίας.
Το υδρογόνο (H2) ανακαλύφθηκε αρχικά από τον Robert Boyle, αλλά μελετήθηκε συστηματικά από τον 'Αγγλο Henry Cavendish (1731-1810) που το αποκάλεσε εύφλεκτο αέρα και κάποια εποχή ταυτίστηκε με το φλογιστόν. Ο Cavendish, επινόησε μέθοδο παραγωγής και αποθήκευσης υδρογόνου πάνω από υδράργυρο και επίσης έδειξε ότι το νερό είναι το προϊόν της εκρηκτικής αντίδρασης μεταξύ υδρογόνου και το οξυγόνου. Υπήρξε ο πρώτος που εξέτασε σχολαστικά στη σύνθεση του αέρα και κατέληξε στο συμπέρασμα ότι "ο αέρας αποτελείται κατά ένα μέρος από αποφλογιστικοποιημένο αέρα [εννοώντας το οξυγόνο] και κατά τέσσερα μέρη από φλογιστικοποιημένο αέρα [εννοώντας το άζωτο]" (1785). Ακόμη, παρατήρησε ότι με δέσμευση του οξυγόνου και του αζώτου, παρέμενε αδέσμευτο το 1/120 του αρχικού όγκου αέρα. Την παρατήρηση αυτή αξιοποίησαν οι Rayleigh και Ramsay μετά από 100 χρόνια για να ανακαλύψουν αρχικά το αργόν και στη συνέχεια τα υπόλοιπα ευγενή αέρια (βλ. παρακάτω).
Ο Σουηδός φαρμακοποιός Carl Wilhelm Scheele (1742-1786) προσδιόρισε ότι ο αέρας ήταν μίγμα δύο αερίων, από τα οποία μόνο το ένα μπορούσε να συντηρήσει την καύση. 'Ηταν ο πρώτος που παρέλαβε καθαρό οξυγόνο, αλλά δεν το αναγνώρισε ως στοιχείο. Αργότερα παρασκεύασε και μελέτησε το υδροφθόριο (HF), το υδρόθειο (H2S), το υδροκυάνιο (HCN ), ενώ το 1774 απομόνωσε το κιτρινοπράσινο αέριο χλώριο (Cl2), το οποίο ονόμασε "αποφλογιστικοποιημένο μουριατικό οξύ" (μουριατικό οξύ: υδροχλωρικό οξύ). Επίσης ανακάλυψε τα αέρια: αμμωνία (NH3), διοξειδίου του θείου (SO2) και το υδροχλώριο (HCl). Το 1772, παρασκεύασε το "αεριούχο νερό", δηλαδή υπέρκορο διάλυμα διοξειδίου του άνθρακα (CO2) σε νερό.
Η συνεισφορά του Scheele στη Χημεία ήταν μεγάλη. Πέραν από την ανακάλυψη του οξυγόνου και του χλωρίου, ανακάλυψε ακόμη τα στοιχεία βάριο (1774), μαγγάνιο (1774), μολυβδαίνιο (1778) και βολφράμιο (1781). Παρά το ότι ο Scheele δεν είχε στη διάθεσή του τα εξελιγμένα χημικά όργανα που διέθετε το εργαστήριο του Lavoisier, με τη δουλειά του συνεισέφερε στην κατάρριψη της φλογιστικής θεωρίας. Ο θάνατός του σε σχετικά μικρή ηλικία (44 ετών) αποδίδεται στη συνεχή ενασχόλησή του με τοξικές ενώσεις βαρέων μετάλλων (μολύβδου, υδραργύρου), η επικινδυνότητα των οποίων δεν είχε ακόμη εκτιμηθεί σωστά.
Το άζωτο ανακαλύφθηκε αργότερα από τον μαθητή του Black, Daniel Rutherford (1749-1819), ο οποίος παρατήρησε ότι μετά από μια καύση σε κλειστό δοχείο, παραμένει ένα άγνωστο αέριο που δεν μπορούσε να συντηρήσει την καύση, αλλά και τη ζωή οργανισμών (α+ζωή). Το αέριο αυτό το ονόμασε "βλαβερό αέρα" ή "φλογιστικοποιημένο αέρα".




Jan Baptist van Helmont
(1579-1644)
Henry Cavendish
(1731-1810)
Carl Wilhelm Scheele
(1742-1786)
Daniel Rutherford
(1749-1819)
Οι ανακαλύψεις αυτές ήταν εξαιρετικής σημασίας για την εποχή τους. Παρά τις δυσκολίες να καταλάβουν τη φύση των στοιχείων και τα μίγματα, οι πειραματιστές της εποχής εκείνης έκαναν μεγάλες προόδους στην κατανόηση των βασικών αρχών της Χημείας. 'Ηταν μια εποχή κατά την οποία επικρατούσε πλήθος εσφαλμένων θεωριών λόγω της ιδεαλιστικής αντίληψης των πραγμάτων και του θρησκευτικού δογματισμού. Χρειαζόταν ένας Lavoisier, οι κορυφαίες ανακαλύψεις του οποίου καθιέρωσαν τη Χημεία ως θετική επιστήμη και διέλυσαν πολλούς "επιστημονικούς μύθους".
Πηγές από το Διαδίκτυο: (1) "Phlogiston Theory" (Jim Loy, 1996). (2) "Considerations on the Doctrine of Phlogiston and the Decomposition of Water" (Joseph Priestly, 1796). (3) "Death of Lavoisier" (John H. Lienhard).





Joseph Louis Proust
(1754-1806)
Claude Louis Berthollet
(1748-1822)
John Dalton
(1766-1844)
Amedeo Avogardo
(1776-1856)
Jöns Jakob Berzelius
(1779-1848)


'Ατομα και μόρια όπως απεικονίζονται στο σύγγραμμα του Dalton "A New System of Chemical Philosophy" (1808) (αποσπάσματα).
11. 18ος - 19ος αιώνας: Ατομική Θεωρία και Περιοδικός Πίνακας
Στις αρχές του 18ου αιώνα άρχισε να διαμορφώνεται η πεποίθηση μεταξύ των χημικών της εποχής εκείνης ότι οι χημικές ενώσεις έχουν συγκεκριμένη σύνθεση και ότι αποτελούνται από συγκεκριμένα στοιχεία και σε σταθερές αναλογίες μεταξύ τους ("νόμος καθορισμένων αναλογιών"). Ο κύριος υποστηρικτής αυτής της ιδέας υπήρξε ο Γάλλος χημικός Joseph Louis Proust (1754-1806).
Το 1797, ο Γάλλος χημικός Claude Louis Berthollet (1748-1822), απέρριψε τον νόμο των καθορισμένων αναλογιών, θεωρώντας ότι η αναλογία των στοιχείων σε μια ένωση καθορίζεται από την αναλογία υπό την οποία λαμβάνονται τα αντιδρώντα. Η άρνηση του Berthollet (ο οποίος βρισκόταν σε μόνιμη επιστημονική διαμάχη με τον Proust), η γνώμη του οποίου μέτραγε πολύ στην επιστημονική κοινότητα, καθυστέρησε την αποδοχή της ορθής θεωρίας του Proust.
Το θέμα ξεκαθάρισε σε μεγάλο βαθμό το 1808 με τη διατύπωση της ατομική θεωρίας του 'Αγγλου χημικού John Dalton (1766-1844). Ο Dalton υποστήριξε ότι τα στοιχεία αποτελούνται από μικροσκοπικά, άτμητα και άφθαρτα σωματίδια, συνδυασμοί των οποίων δημιουργούν τις διάφορες ουσίες. Στο κάθε στοιχείο ο Dalton είχε αποδώσει ένα σύμβολο.
Η θεωρία του Dalton, στην ουσία της, βασίζεται στην ιδέα της ατομικής θεωρίας του Δημόκριτου, και είχε σημαντική επίδραση στην εξέλιξη της Χημείας, αφού άρχισαν πλέον να αποδίδονται συγκεκριμένα ατομικά βάρη στα διάφορα στοιχεία. 'Ολα αυτά περιγράφονται στο περίφημο βιβλίο του Dalton Νέο Σύστημα της Χημικής Φιλοσοφίας (A New System of Chemical Philosophy).
Τιμητικά, το όνομα του Dalton διατηρείται στις μονάδες μοριακής μάζας κυρίως μεγαλομοριακών ενώσεων, π.χ. η πρωτεΐνη αιμοσφαιρίνη Α αναφέρεται ότι έχει μοριακή μάζα 68 kilodalton (kDa).
Κατά τη διάρκεια του 19ου αιώνα οι χημικοί είχαν χωρισθεί σε δύο στρατόπεδα γύρω από την ατομική θεωρία. Ο διάσημος Ιταλός χημικός Amedeo Avogardo (1776-1856) και ο Αυστριακός φυσικός Ludwig Edward Boltzmann (1844-1906) υπήρξαν ένθερμοι υποστηρικτές της ατομικής θεωρίας και συνεισέφεραν σε αυτήν με ανακαλύψεις στον τομέα των αερίων. Εναντίον της θεωρίας ήταν οι χημικοί Wilhelm Ostwald και Ernst Mach. O Avogadro πρότεινε τον διάσημο νόμο που φέρει το όνομά του, ότι "ίσοι όγκοι αερίων, κάτω από την ίδια πίεση και θερμοκρασία, περιέχουν ίσο αριθμό μορίων". Ως σταθερά ή αριθμός Avogadro (NA) αναφέρεται και ο αριθμός των μορίων που περιέχονται σε ένα γραμμομόριο μιας χημικής ένωσης
Το 1808, ο Σουηδός χημικός Jöns Jakob Berzelius (1779-1848) στο βιβλίο του Lãrbok I Kemien, πρότεινε τα σημερινά χημικά σύμβολα των στοιχείων (όσων είχαν μέχρι τότε βρεθεί) σε αντικατάσταση των γεωμετρικών συμβόλων, που χρησιμοποιούσε o Dalton. Ακόμη, καθιέρωσε τον σημερινό τρόπο αναγραφής των χημικών αντιδράσεων (μια μικρή διαφορά ήταν ότι ο αριθμός των ατόμων ενός στοιχείου σε ένα μόριο γραφόταν ως άνω δείκτης και όχι ως κάτω δείκτης), καθώς και την έννοια των ατομικών βαρών των στοιχείων .
Ο Berzelius ήταν αυτός που καθιέρωσε στη Χημεία χημικούς όρους με ελληνικές ρίζες, που περιγράφουν τα φαινόμενα όπως, π.χ. η κατάλυση, ο πολυμερισμός, ο ισομερισμός και αλλοτροπισμός.
Για αρκετές δεκαετίες η ανακάλυψη νέων στοιχείων υπήρξε ένα σημαντικό γεγονός στη Χημεία και ο αριθμός των χημικών στοιχείων αυξάνονταν, με μέσο ρυθμό ενός στοιχείου για κάθε έτος κατά την περίοδο 1840-1870. Καθώς οι φυσικές και οι χημικές ιδιότητες των στοιχείων άρχισαν να γίνονται γνωστά, ορισμένοι χημικοί άρχισαν να παρατηρούν κάποιες ομοιότητές τους κατά ομάδες, όπως και κάποια "περιοδικότητα" στις ιδιότητές, όταν τα στοιχεία εξετάζονταν κατά σειρά αυξανόμενου ατομικού βάρους. 'Οπως είναι γνωστό, εκείνη την εποχή δεν υπήρχε η παραμικρή ιδέα για την ηλεκτρονιακή δομή των ατόμων.



Robert Bunsen (1811-1899)
Gustav Kirchhoff (1824-1887)
Μια από τις αρχικές μορφές φασματοσκόπιου, εφεύρεση των Bunsen και Kirchhoff (1859)
Το 1864, ο Γερμανός Lothar Meyer (1830-1895) ήταν ο πρώτος που ασχολήθηκε με την κατάταξη των στοιχείων σε μια πρωταρχική μορφή "περιοδικού πίνακα", αλλά υπήρχαν και σημαντικά κενά σε πολλά σημεία του. Πέντε χρόνια αργότερα, το 1869, με το θέμα της περιοδικότητας των ιδιοτήτων των χημικών στοιχείων ασχολήθηκε ο Ρώσος χημικός Dmitri Mendeleev (1834-1907).
Τόσο ο Meyer, όσο και ο Mendeleev είχαν σπουδάσει υπό τον διάσημο χημικό Robert Bunsen (1811-1899). Θα πρέπει εδώ να σημειωθεί ότι ο Bunsen μαζί με τον επίσης διάσημο φυσικό Gustav Kirchhoff (1824-1887), θεωρούνται οι θεμελιωτές της φασματοσκοπίας, μέσω της οποίας ανακάλυψαν δύο ακόμη στοιχεία: το 1860 το καίσιο (Cs) και το 1861 το ρουβίδιο (Rb), που κάλυψαν δυο κενές θέσεις της 1ης ομάδας του περιοδικού πίνακα (ομάδα αλκαλίων).
To 1869, ο Mendeleev μελέτησε συστηματικά (τότε ήταν πλέον γνωστά 63 στοιχεία) τον πίνακα του Meyer και άρχισε να συγκεντρώνει πληροφορίες για τα κενά. Εξετάζοντας την περιοδικότητα διάφορων φυσικών και χημικών ιδιοτήτων των στοιχείων, ήταν σε θέση να προβλέψει τις φυσικές και χημικές ιδιότητες των στοιχείων (και των ενώσεών τους), που βρίσκονταν στον πίνακά του κάτω από το πυρίτιο, το αργίλιο και το βόριο και δεν είχαν ακόμη ανακαλυφθεί. Μάλιστα τους είχε δώσει τα "προσωρινά" ονόματα: εκα-πυρίτιο, εκα-αργίλιο και εκα-βόριο.
Ο Mendeleev χρησιμοποιούσε στα προσωρινά ονόματα τα προθήματα eka-, dvi- και tri- (στα σανσκριτικά: ένα, δύο, τρία) για να δηλώσει τον αριθμό θέσεων κάτω από το στοιχείο που ακολουθεί (π.χ. εκα-πυρίτιο: το στοιχείο που βρίσκεται μία θέση κάτω από το πυρίτιο). 'Οταν αργότερα ανακαλύφθηκαν τα στοιχεία αυτά (γερμάνιο, γάλλιο και σκάνδιο), οι προβλέψεις του Mendeleev αποδείχθηκαν εξαιρετικά ακριβείς.
Για να εκτιμηθεί το μέγεθος του επιτεύγματος της σχεδίασης του πρώτου περιοδικού πίνακα, θα πρέπει να ληφθεί υπόψη το γεγονός ότι την εποχή εκείνο οι επιστήμονες είχαν πλήρη άγνοια ως προς την δομή των ατόμων και ως προς την ύπαρξη των ηλεκτρονίων. Οι Mendeleev και Meyer βραβεύθηκαν ισάξια για το επιστημονικό αυτό επίτευγμα από την Royal Society της Μ. Βρετανίας (το 1883) με το τιμητικό για εκείνη την εποχή Davy Medal. Ο Mendeleev τιμήθηκε επίσης όταν το ραδιενεργό στοιχείο με ατομικό αριθμό 101 ονομάστηκε Μεντελέβιο (Mendelevium, Md).



Lothar Meyer (1830-1895)
Dmitri Mendeleev (1834-1907)
Οι 5 πρώτες περίοδοι του Περιοδικού Πίνακα του Mendeleev (με αστερίσκο σημειώνονται οι κενές θέσεις στοιχείων των οποίων προέβλεψε τις ιδιότητες)

Friedrich Wöhler
(1800-1882)
12. Οργανική Χημεία και ο Βιταλισμός
Μετά την επικράτηση της ατομικής θεωρίας και των ποσοτικών σχέσεων που συνέδεαν τα χημικά στοιχεία στις διάφορες ενώσεις τους, η Χημεία έγινε επιστημονικός κλάδος με πειραματικά τεκμηριωμένο περιεχόμενο. Παρ' όλα αυτά ακόμη και μέχρι σχεδόν τα μέσα του 19ου αιώνα επικρατούσαν ακόμη κάποιες "βιταλιστικές" απόψεις, που είχαν τις βάσεις τους σε αριστοτελικές θεωρίες περί ζωής. Μέχρι το 1828 υπήρχε η γενική πεποίθηση ότι δεν είναι δυνατή η παρασκευή οργανικών ουσιών στο εργαστήριο. Για την παρασκευή του χρειαζόταν μια ζωική δύναμη (vis vitalis), μια δύναμη ακαθόριστης προέλευσης και φύσης που έδινε "ψυχή" στα οργανικά σώματα.
Παράλληλα, αρκετά διαδεδομένη ήταν και η θεωρία της αυτόματης γένεσης ή αβιογένεσης (spontaneous generation, abiogenesis), σύμφωνα με την οποία οι ζωντανοί οργανισμοί γεννούνται από ανόργανη ύλη (χώμα, λάσπη, φυτική ύλη) με "θεϊκή παρέμβαση". 'Ολα αυτά ήταν αποτέλεσμα εσφαλμένης ερμηνείας της εμφάνισης μικροοργανισμών και υδρόβιων μικρών ζώων (σκουλήκια, σκαθάρια, κ.λπ.) στις λάσπες αγρών, όπως και κατά τη σήψη φυτικής και ζωικής ύλης.
Οι οργανικές ενώσεις που είχαν απομονωθεί από διάφορα φυσικά προϊόντα ή μετά από φυσικές διεργασίες, όπως π.χ. η αιθανόλη, το οξικό οξύ, η ακετόνη, διάφορα σάκχαρα, ήταν άφθονες. Ο μοριακός τύπος πολλών από τις ενώσεις αυτές ήταν σε γενικές γραμμές γνωστός, ωστόσο το δόγμα της ζωικής δύναμης εκ των προτέρων απέτρεπε κάθε επιδίωξη σύνθεσής τους.
Το 1828, ο νεαρός Γερμανός χημικός Friedrich Wöhler διαπίστωσε ότι μπορούσε να παρασκευάσει στο εργαστήριο μία οργανική ένωση. Αυτό το πέτυχε τυχαία, όταν με θέρμανση κυανικού αμμωνίου (NH4OCN) παρασκεύασε την ουρία (H2NCONH2), η οποία είναι οργανική ένωση, σύμφωνα με την ακόλουθη αλληλουχία:
AgOCN + NH4Cl
Είναι χαρακτηριστικό το "θριαμβευτικό" γράμμα που έστειλε στον σεβαστό καθηγητή του Berzelius, που υπήρξε ένθερμος οπαδός του βιταλισμού: "Πρέπει να σας πω ότι μπορώ να παρασκευάσω ουρία χωρίς να χρειαστώ νεφρά, ούτε άνθρωπο, ούτε σκύλο. Το κυανικό αμμώνιο είναι η ουρία!".
Ακολούθησαν βέβαια αντιδράσεις από τον Berzelius και άλλους υποστηρικτές του βιταλισμού, του τύπου "η ουρία βρίσκεται στο μεταίχμιο μεταξύ οργανικών και ανόργανων ενώσεων", αλλά το ρήγμα στη βιταλιστική θεωρία είχε ήδη γίνει. Και μια ακόμη εσφαλμένη θεωρία - τροχοπέδη καταρρίφθηκε. Το έτος 1828 θεωρείται πλέον το έτος έναρξης της Οργανικής Σύνθεσης. Στις μέρες μας, ο "παραδοσιακός" διαχωρισμός σε της Χημείας σε Ανόργανη και Οργανική εξακολουθεί να υφίσταται, αλλά καθαρά για λόγους συστηματικότερης εκμάθησης.



Αριστερά: Ο Jean Louis Pasteur (1822-1895) πειραματιζόμενος με τις περίφημες φιάλες χάρις στις οποίες κατέρριψε τη θεωρία της "αυτόματης γέννησης". Μέσον: Ο Pasteur έβρασε τον ζωμό σε μια φιάλη και στη συνέχεια έδωσε στο λαιμό το σχήμα S ("λαιμός κύκνου") με τη βοήθεια φλόγας. Αυτό αποτρέπει την εισαγωγή μικροοργανισμών του αέρα στη φιάλη, αλλά επιτρέπει τη μερική αναταλλαγή αέρα. 'Οταν ο "λαιμός κύκνου" έσπαζε, άρχιζε η ανάπτυξη μικροοργανισμών. Το θόλωμα στο ζωμό είναι ένδειξη ανάπτυξης μικροοργανισμών στον αρχικά διαυγή ζωμό κρέατος (περισσότερα). Δεξιά: Οι δύο κατοπτρικές κρυστάλλων του μικτού άλατος με αμμώνιο και νάτριο του D,L-τρυγικού οξέος ("ρακεμικού οξέος"), που διαχώρισε ο Pasteur με το χέρι και με απλή οπτική παρατήρηση (περισσότερα).
Το επόμενο σημαντικό θέμα που αντιμετωπίστηκε ήταν το θέμα της αυτόματης γένεσης των ζωντανών ειδών. Το θέμα αυτό είχε επηρεάσει αρνητικά την πρόοδο της βιοχημείας και της βιολογίας αλλά και άλλων επιστημών. Μάλιστα είχε επηρεάσει επιστήμονες και ιδεαλιστές φιλόσοφους (όπως ο Καντ, ο Χέγκελ) που είχαν συμβάλλει με σπουδαίες ανακαλύψεις. Τελικά, το θέμα έγινε τόσο σημαντικό ώστε η Γαλλική 'Ακαδημία Επιστημών προκήρυξε βραβείο σε όποιον θα κατόρθωνε με τεκμηριωμένα πειράματα να δείξει τι ακριβώς ισχύει.
Το βραβείο κέρδισε ο Γάλλος χημικός-μικροβιολόγος Jean Louis Pasteur (1822-1895) με τα απλά και ευφυή πειράματα που διεξήγαγε κατά το 1862-63. Ο Pasteur έδειξε ότι ζωμός κρέατος, που έχει βραστεί καλά και έχει προφυλαχθεί από μικροοργανισμούς του αέρα (χάρις σε φιάλες ειδικής κατασκευής που απέκλειαν την είσοδο αέρα) ήταν αδύνατο να αναπτυχθούν μικρόβια και άλλοι μικροοργανισμοί και μπορούσε ο ζωμός να μείνει αναλλοίωτος (και μάλιστα, όπως αποδείχθηκε, για χρόνια). Με αυτό το απλό πείραμα, που έμεινε στην ιστορία της Επιστήμης ως το πείραμα με τη φιάλη με "λαιμό κύκνου" ("swan neck" flask experiment), έδειξε ότι αυτόματη γένεση ζωής δεν υπάρχει, τερματίζοντας ένα ακόμη θέμα που ενέπλεκε την επιστήμη με παραδοξολογίες μυστικιστικού χαρακτήρα.
Το 1848, είχε προηγηθεί η επίλυση ενός άλλου χημικού προβλήματος από τον Pasteur. Είχε διαπιστωθεί ότι τρυγικό οξύ που λαμβανόταν από φυσικά προϊόντα (το L(+)-τρυγικό οξύ) είχε επακριβώς τις ίδιες χημικές ιδιότητες με το συνθετικά παρασκευαζόμενο τρυγικό οξύ ή το "παρατρυγικό οξύ" ή "ρακεμικό οξύ" (το D,L-τρυγικό οξύ), το οποίο μπορούσε να ληφθεί επίσης -κάτω υπό ορισμένες συνθήκες- και ως φυσικό προϊόν κατά τη ζύμωση του γλεύκους. Ωστόσο, το πρώτο έστρεφε το επίπεδο πόλωσης φωτός σε αντίθεση με το δεύτερο, που εμφανιζόταν ως "οπτικώς ανενεργό". Να σημειωθεί ότι το επίθετο "ρακεμικό" επεκτάθηκε αργότερα σε κάθε ισομοριακό μίγμα οπτικών αντιπόδων μιας ένωσης, αρχικά όμως αφορούσε το οπτικώς ανενεργό τρυγικό οξύ, δηλ. το D,L-τρυγικό οξύ.
O Pasteur κατάφερε εξοπλισμένος με τη βοήθεια ενός μεγεθυντικού φακού, με ένα τσιμπιδάκι και με μεγάλη υπομονή να διαχωρίσει τις δύο κατοπτρικές μορφές των κρυστάλλων του μικτού άλατος του ρακεμικού οξέος με αμμώνιο και νάτριο, το οποίο εμφανιζόταν ως οπτικώς ανενεργό. Διαπίστωσε στη συνέχεια ότι τα διαλύματα των δύο διαφορετικών κρυστάλλων είχαν ακριβώς αντίθετες στροφικές ικανότητες, ενώ ισομοριακό μίγμα τους δεν παρουσίαζε στροφική ικανότητα. 'Ετσι, ο Pasteur έδειξε έτσι το ρακεμικό οξύ αποτελείται από δύο "οπτικούς αντίποδες", αποδεικνύοντας έτσι την ύπαρξη χειραλικών ενώσεων. Ο Pasteur στάθηκε τυχερός διότι το άλας που χρησιμοποίησε είναι μια από τις λίγες ρακεμικές ουσίες που διαχωρίζονται σε οπτικούς αντίποδες κατά την κρυστάλλωση. Να σημειωθεί ότι τότε απολύτως τίποτα δεν ήταν γνωστό για τη στερεοχημεία των ενώσεων του άνθρακα, την τετραεδρική διάταξη των δεσμών του και φυσικά για τα D-, L- ή D,L-ισομερή.

Το κανονικό τετράεδρο των απλών δεσμών του άνθρακα (μόριο μεθανίου)
13. Οργανική Χημεία, Χημικοί Δεσμοί του 'Ανθρακα και Οργανικές Ενώσεις
Η Οργανική Χημεία έχει ως αντικείμενο μελέτης τις ενώσεις του άνθρακα. Ο άνθρακας παρουσιάζει κάποιες ξεχωριστές ιδιότητες σε σχέση με τα άλλα στοιχεία. Είναι το μοναδικό στοιχείο του οποίου τα άτομα μπορούν να σχηματίσουν δεσμούς μεταξύ τους δημιουργώντας επιμήκεις ανθρακικές αλυσίδες και δακτυλίους. Ο άνθρακας έχει τη δυνατότητα να σχηματίζει μια τεράστια ποικιλία χημικών ενώσεων, από το απλό μεθάνιο μέχρι τις πρωτεΐνες και τα νουκλεϊνικά οξέα με μοριακά βάρη της τάξης μερικών εκατομμυρίων. Αυτός είναι και ο λόγος που οι οργανικές ενώσεις είναι τα κύρια συστατικά μόρια των ζωντανών οργανισμών. Αλλά και η βιομηχανική επανάσταση δημιούργησε μεγάλο αριθμό χημικών βιομηχανιών με βάση τις οργανικές ενώσεις για φάρμακα, χρώματα, πολυμερή, φυτοφάρμακα, και βιοχημικά αντιδραστήρια.
Από τα μέσα του 19ου αιώνα άρχισε η ραγδαία ανάπτυξη της Οργανική Χημείας. Οι επιστήμονες άρχισαν να ενδιαφέρονται για τις δυνάμεις και τους δεσμούς που συγκρατούν τα άτομα άνθρακα μεταξύ τους και σχηματίζουν αυτήν την τεράστια ποικιλία ενώσεων. Το 1858, ο Γερμανός χημικός August Kekulé (1829-1896) και ο Σκώτος χημικός Archibald Couper (1831-1892), ανεξάρτητα ο ένας από τον άλλο, διατυπώνουν τις απόψεις τους για τις "τέσσερις μονάδες συγγένειας" ή δεσμούς του κάθε ατόμου άνθρακα. Η τετρασθένεια του άνθρακα ήταν δεδομένη και οι ενώσεις του σταθερές. Το 1865, ο Kekulé εισηγήθηκε ότι οι ανθρακικές αλυσίδες μπορούν να σχηματίσουν δακτυλίους με αναδίπλωση των δεσμών, ιδέα που ήταν αρκετά προχωρημένη για την εποχή του
Η θεωρία Kekulé για το τετρασθενές του άνθρακα ολοκληρώθηκε αργότερα με την παρέμβαση του Ολλανδού χημικού Jacobus van't Hoff (1852-1911, Nobel Χημείας του 1901) και του Joseph Le Bel (1847-1930), που επιβεβαίωναν ότι ο άνθρακας συνδέεται με άλλα τέσσερα άτομα τοποθετημένα στις 4 γωνίες ενός κανονικού τετραέδρου, με το άτομο του άνθρακα στο κέντρο του. Η πυραμιδική διάταξη φαίνεται ξεκάθαρα στην απλούστερη δυνατή περίπτωση, το μόριο μεθανίου (CH4).
Αρκετά, αργότερα οι χημικοί με μεγάλο αριθμό δεδομένων κατέληξαν οι 4 δεσμοί είναι ισοδύναμοι και σχηματίζονται με "ανάμιξη" ενός τροχιακού s και τριών τροχιακών p (υβριδισμός sp3). Ο υβριδισμός βοηθάει στον σχηματισμό 4 ισοδύναμων μοριακών τροχιακών τετραεδρικής διευθέτησης.


August Kekulé (1829-1896)
Η δομή του βενζολίου που προτάθηκε από τον Kekulé.
Η σημαντικότερη συμβολή του August Kekulé στην Οργανική Χημεία υπήρξε η θεωρία του για τη δομή του βενζολίου. Από τον 19ο αιώνα ήταν γνωστό ότι το βενζόλιο είχε τον μοριακό τύπο C6H6 και παρά την εμφανέστατη "ακορεστότητά" του, παρουσιαζόταν ως μια εξαιρετικά σταθερή ένωση με σημαντικές διαφοροποιήσεις ως προς τη χημική του συμπεριφορά, σε σχέση με άλλες γνωστές ακόρεστες οργανικές ενώσεις. Οι ιδιαιτερότητες αυτές αναφέρονται ως αρωνατικότητα ή αρωματικός χαρακτήρας.
Το 1865, ο Kekulé διατύπωσε την άποψη ότι το βενζόλιο αποτελείται από ένα εξαμελή δακτύλιο ανθράκων με τρεις διπλούς δεσμούς. Η ερμηνεία του ήταν ότι τρεις διπλοί δεσμοί "ταλαντώνονται" ταχύτατα μεταξύ δύο θέσεων. Η δομή αυτή γνώρισε την εποχή εκείνη πολλές επικρίσεις. Παρ' όλο που ερμήνευε ικανοποιητικά τον αριθμό των δισ-υποκατεστημένων βενζολίων, δεν μπορούσε να ερμηνεύσει την ελάχιστη δραστικότητα του βενζολίου σε σχέση με εκείνη των άλλων αλκενίων και ακόρεστων ενώσεων. Η ασυνήθιστη σταθερότητα του βενζολίου αποτέλεσε δυσεπίλυτο αίνιγμα για τους χημικούς της εποχής εκείνης.
Τελικά, απάντηση στο ερώτημα στο ερώτημα αυτό έδωσε η θεωρία του συντονισμού (ή μεσομέρειας), σύμφωνα με την οποία το βενζόλιο μπορεί να περιγραφεί ως ένα υβρίδιο δύο ισοδύναμων δομών, στις οποίες κάθε σύνδεση C-C αντιστοιχεί κατά μέσο όρο σε 1,5 δεσμό, δηλαδή σε μια ενδιάμεση κατάσταση μεταξύ απλού και διπλού δεσμού. Οι δομές συντονισμού διαφέρουν μόνο ως προς τις θέσεις των ηλεκτρονίων τους. Η πραγματική δομή βρίσκεται ανάμεσα στις δύο ακραίες εκδοχές.
Τελικά, η θεωρία του Kekulé για τη δομή του βενζολίου επικράτησε και οδήγησε στην υιοθέτηση ανάλογων τύπων για όλες τις αρωματικές ενώσεις. Το 1890, η "Εταιρεία των Γερμανών Χημικών" οργάνωσε ειδική τελετή, με το όνομα Benzolfest (: γιορτή για το βενζόλιο), για να τιμήσει τον Kekulé με την ευκαιρία της 25ης επετείου από τη δημοσίευση του πρώτου άρθρου του που πρότεινε τη δομή του βενζολίου. Στην ομιλία του, ο Kekulé αναφέρθηκε στο περίφημο "όνειρό" του (για τον "ουροβόρο όφι", πανάρχαιο αλχημιστικό σύμβολο του σύμπαντος), από το οποίο εμπνεύστηκε τη δομή του βενζολίου. Το όνειρο αυτό είναι ίσως ένα από τα ωραιότερα "παραμύθια" της χημείας (βλ. Χημική ένωση του μήνα: Βενζόλιο).





Γραμματόσημα που εκδόθηκαν προς τιμήν του Kekulé. Ο ίδιος και το περίφημο "όνειρό του" υπήρξαν θέματα πολλών χιουμοριστικών σκίτσων.

Justus von Liebig
(1803-1873)

Jean Baptiste Dumas
(1800-1884)

Charles Adolphe Wurtz
(1817-1884)

Edward Frankland
(1825-1899)
14. Εξελίξεις στη Χημεία κατά τον 19ο αιώνα
Η Χημεία απαλλαγμένη πλέον από παραδοξολογίες του παρελθόντος, από τα μέσα του 19ου αιώνα και μετά είναι πλέον μια καθιερωμένη και κοινωνικά αποδεκτή επιστήμη, αλλά συγχρόνως και ένα "παρθένο" έδαφος, το οποίο η ανθρώπινη διανόηση είναι πλέον έτοιμη να γονιμοποιήσει. Εμφανίζεται πλέον πλήθος λαμπρών επιστημόνων, ενδεχομένως με κάποιες προκαταλήψεις από διδασκαλίες και παραδοχές του παρελθόντος, αλλά αποκλειστικά επιστημονικού και μόνο χαρακτήρα, όπως και με νέες έξοχες ιδέες που χρειάζεται κάποιος αγώνας για να έρθουν στο προσκήνιο και να γίνουν αποδεκτές. Οι ανταγωνισμοί και οι αγώνες για την "προτεραιότητα" ιδεών είναι αναπόφευκτοι και συγχρόνως αποδοτικοί.

Το διάσημο σκεύος Kaliapparat, που επινόησε ο Liebig για τη δέσμευση του CO2 κατά τον στοιχειακό προσδιορισμό άνθρακα σε οργανικές ενώσεις.
Η Οργανική Χημεία επεκτάθηκε με ταχύτατο ρυθμό κατά τον 19ο και 20ο αιώνα με σημαντικό αριθμό νέων ανακαλύψεων και πειραματικών τεχνικών. Στην άνθιση της Οργανικής Χημείας συνέβαλε μια σειρά από έξοχους οργανικούς χημικούς που βελτίωσαν τις μέχρι τότε εργαστηριακές συσκευές, όπως ο Γερμανός Justus von Liebig (1803-1873) που συνεισέφερε πολλά στον τομέα του προσδιορισμού της στοιχειακής σύνθεσης των οργανικών ενώσεων.
Ο Γάλλος Jean Baptiste Dumas (1800-1884) καθιερώνει ως μονάδα το ατομικό βάρος του υδρογόνου, προσδιορίζει τα ατομικά βάρη του άνθρακα και του οξυγόνου και άλλων στοιχείων (συνολικά 30) και αναπτύσσει μέθοδο προσδιορισμού του αζώτου σε οργανικές ενώσεις.
Ο Γάλλος (Αλσατός) Charles Adolphe Wurtz (1817-1884) συνεισφέρει πολλά στην ανόργανη και στην οργανική σύνθεση και μένει στην ιστορία της Οργανικής Χημείας γνωστός χάρις στην ομώνυμη αντίδραση παρασκευής υδρογονανθράκων με την αντίδραση αλκυλαλογονιδίων με το μεταλλικό νάτριο.
Ο 'Αγγλος Edward Frankland (1825-1899), στην προσπάθειά του να απομονώσει οργανικές ρίζες (αλκύλια) αναφέρει το 1848 την πρώτη σύνθεση οργανομεταλλικής ένωσης (δηλ. ένωσης με απ' ευθείας δεσμό άνθρακα-μετάλλου), του διαιθυλο-ψευδαργύρου και αναγνωρίζει τις δυνατότητες εφαρμογής των οργανομεταλλικών ενώσεων αυτών στην οργανική σύνθεση, δυνατότητας που αργότερα φέρει στα όρια της τελειότητας ο Victor Grignard. Δικαιολογημένα ο Frankland θεωρείται ως ο "πατέρας της Οργανομεταλλικής Χημείας".


William Henry Perkin (1838-1907)
Παλαιό φιαλίδιο με στερεή μωβεΐνη και
φόρεμα βαμμένο με το χρώμα αυτό.
Σταθμός στην εφαρμοσμένη οργανική σύνθεση υπήρξε και το έτος 1856. Ο μόλις 18-χρονος τότε 'Αγγλος φοιτητής της Χημείας William Henry Perkin (1838-1907) στην προσπάθειά του να συνθέσει την περιζήτητη τότε κινίνη, οξείδωσε με διάλυμα διχρωμικού καλίου σε θειικό οξύ μίγμα διάφορων αρωματικών αμινών (ανιλίνες, τολουιδίνες). Διαπίστωσε ότι προέκυψε ένα σκουρόχρωμο προϊόν, που του λέρωσε τα γυάλινα σκεύη που χρησιμοποιούσε. Ο Perkin, προσπαθώντας να τα καθαρίσει με αλκοόλη, παρέλαβε ένα διάλυμα που μπορούσε εύκολα και ανεξίτηλα να βάψει μωβ μεταξωτά και άλλα υφάσματα. Το προϊόν αυτό υπήρξε το πρώτο συνθετικό οργανικό χρώμα, η μωβεΐνη (ή ιώδες της ανιλίνης). Αυτή ήταν η αρχή της βιομηχανικής παρασκευής οργανικών χρωμάτων που έμελλε να οδηγήσει σε βιομηχανίες χρωμάτων-κολοσσούς. 50 χρόνια μετά την "κατά λάθος" ανακάλυψη της μωβεΐνης, ήδη είχαν παρασκευασθεί 2000 συνθετικές χρωστικές ύλες.
Πολλοί υπήρξαν οι πρωτεργάτες πάνω στο νέο πεδίο της Χημείας, τη Φυσικοχημεία που ερμηνεύει χημικά φαινόμενα με καθιερωμένες γνώσεις από τη Φυσική και κυρίως από τη Θερμοδυναμική. Ο Αμερικανός χημικός, φυσικός και μαθηματικός Josiah Willard Gibbs (1839-1903) θεωρείται ο θεμελιωτής της Χημικής Θερμοδυναμικής. Ο Γάλλος Henri Louis Le Chatêlier (1850-1936) διατυπώνει περί τα τέλη του 19ου αιώνα την περίφημη αρχή του που διέπει κάθε χημική ισορροπία: "Εάν ένα χημικό σύστημα βρίσκεται σε ισορροπία, θα αντιδράσει σε κάθε αλλαγή συγκέντρωσης, θερμοκρασίας ή πίεσης κατά τρόπο που να ελαχιστοποιεί την αλλαγή αυτή".
Ο Ολλανδός οργανικός χημικός και φυσικοχημικός Jacobus Henricus van't Hoff (1852-1911) συνεισέφερε πολλά σε θέματα χημικής κινητικής και ισορροπίας. Το 1874 δημοσίευσε το βιβλίο με τίτλο "La chimie dans l' éspace" (η Χημεία στον χώρο), το οποίο θεωρείται η απαρχή της στερεοχημείας και όπου θεμελιώνεται η τετραεδρική δομή των κορεσμένων ενώσεων του άνθρακα, αν και αρχικά υπήρξε αντικείμενο σφοδρών επικρίσεων. Υπήρξε ο πρώτος επιστήμονας που τιμήθηκε το 1901 με το Nobel Χημείας για τις εργασίες σε θέματα χημικής δυναμικής και της ωσμωτικής πίεσης σε διαλύματα.
Στις αρχές του 20ου αιώνα, ο Γερμανός (από τη Λιθουανία) Wilhelm Ostwald (1853-1932) διατυπώνει τις θεωρίες του πάνω στη χημική ισορροπία, τη χημική κινητική και την κατάλυση και για το έργο του αυτό τιμήθηκε με το Nobel Χημείας του 1909.






Josiah Willard Gibbs
(1839-1903)
Henri Louis Le Chatêlier
(1850-1936)
Jacobus Henricus
van't Hoff (1852-1911)
Wilhelm Ostwald
(1853-1932)
Svante August Arrhenius
(1859-1927)
Walter Nernst
(1864-1941)
Το 1884, ο Σουηδός Svante August Arrhenius (1859-1927), στη διδακτορική διατριβή που υπέβαλε στο Πανεπιστήμιο της Ουψάλας, διατυπώνει τη θεωρία του για την ηλεκτρολυτική διάσταση, τον ιοντισμό και την ύπαρξη ιόντων. Η ιδέα του αυτή ήταν τόσο ριζοσπαστική για την εποχή της, που μόλις και κατάφερε να γίνει δεκτή η διατριβή του και μάλιστα με χαμηλό βαθμό. Σήμερα, η ηλεκτρολυτική διάσταση π.χ. των αλάτων σε διαλύματά τους αποτελεί κοινή γνώση, τότε όμως η ιδέα αυτή πολεμήθηκε σφοδρότατα.
Ο Arrhenious βρήκε ένθερμο υποστηρικτή της θεωρίας του στο πρόσωπο του Ostwald και αργότερα τιμήθηκε για αυτήν με το Nobel Χημείας του 1903 και στον van't Hoff, ο οποίος το 1889 απέδειξε πειραματικά την ορθότητα της θεωρίας της διάστασης των ηλεκτρολυτών.
Αυτό που ίσως δεν είναι ευρύτερα γνωστό για τον Arrhenious είναι το ότι πρώτος, ήδη από 1896, είχε προβλέψει ότι η καύση ορυκτών καυσίμων και η αύξηση του ατμοσφαιρικού CO2 θα οδηγήσει στο φαινόμενο της υπερθέρμανσης της ατμόσφαιρας του πλανήτη. Μάλιστα είχε υπολογίσει ότι διπλασιασμός της περιεκτικότητας της ατμόσφαιρας σε CO2 θα αυξήσει τη μέση θερμοκρασία της ατμόσφαιρας κατά 5ºC.
Ο Γερμανός φυσικοχημικός Walter Nernst (1864-1941), τιμήθηκε με το Nobel Χημείας του 1920 για τη θεωρία του πάνω στον 3ο θερμοδυναμικό νόμο (η εντροπία του τέλειου κρυστάλλου τείνει προς το μηδέν, όσο η θερμοκρασία του τείνει προς το απόλυτο μηδέν). Συνεισέφερε πολλά στη Φυσικοχημεία και είναι γενικότερα γνωστός για την περίφημη εξίσωση του, που είναι η βασική εξίσωση σε θέματα οξειδοαναγωγής και γενικότερα στον χώρο της Ηλεκτροχημείας.



John William Strutt, Λόρδος Rayleigh
(1842-1919)
William Ramsay
(1852-1916)
Σωλήνες ηλεκτρικής εκκένωσης με
διάφορα ευγενή αέρια.
Το 1896, ο 'Αγγλος φυσικός John William Strutt, Λόρδος Rayleigh (1842-1919) και ο Σκότος χημικός William Ramsay (1852-1916), διαπίστωσαν μια μικρή διαφορά στην πυκνότητα μεταξύ του αζώτου που λαμβάνεται με χημικές μεθόδους, σε σχέση με την πυκνότητα του αζώτου που λαμβάνεται από τον αέρα (μετά την απομάκρυνση του οξυγόνου και του διοξειδίου του άνθρακα). Το πρώτο ήταν μόλις κατά 0,5% ειδικώς ελαφρότερο από το δεύτερο. Με προσεκτικές μετρήσεις διαπίστωσαν ότι αυτή η μικρή διαφορά δεν ήταν κάτι το τυχαίο, αλλά εμφανιζόταν συστηματικά. Κατάλαβαν ότι η διαφορά αυτή οφειλόταν σε κάποιο άλλο συστατικό της ατμόσφαιρας, γεγονός που τους οδήγησε στην ανακάλυψη του αέριου στοιχείου αργόν.
Τα επόμενα 4-5 χρόνια ο Ramsey ανακάλυψε και τα υπόλοιπα ευγενή αέρια, δηλ. το νέον, το κρυπτόν, το ξένον, όπως και το ελαφρύτερο απ' όλα, το ήλιο, που ήταν ήδη γνωστή η παρουσία του στον ήλιο από φασματοσκοπικά δεδομένα. Ο Ramsey διαπίστωσε ότι τα αέρια αυτά ήταν χημικώς αδρανή και τα ονόμασε ευγενή αέρια. Αρκετά αργότερα, το 1910, απομόνωσε και το σχετικά βραχύβιο ραδιενεργό ευγενές αέριο, το ραδόνιο. O Rayleigh τιμήθηκε με το Nobel Φυσικής του 1904 gια τις μελέτες του πάνω στην πυκνότητα των αερίων και την ανακάλυψη του αργού. Με το Nobel Χημείας του ίδιου έτους τιμήθηκε ο Ramsey για την ανακάλυψη των ευγενών αερίων και την κατάταξή τους στον περιοδικό πίνακα.
Περίπου 60 χρόνια αργότερα διαπιστώθηκε ότι τα ευγενή αέρια δεν είναι και τόσο "ευγενή", όταν ο 'Αγγλος χημικός Neil Bartlett (1932-2008) διαπίστωσε ότι σχετικά εύκολα μπορούσαν να παρασκευαστούν φθοριούχες ενώσεις του ξένου. Σήμερα, είναι πλέον γνωστές ανάλογες ενώσεις του ραδονίου (σταθερότερες, αλλά βραχύβιες λόγω της ραδιενεργού διάσπασης του ραδονίου) και του κρυπτού (εξαιρετικά ασταθείς).
Ο Γερμανός χημικός Hermann Emil Fischer (1852-1919), τιμήθηκε με το Nobel Χημείας του 1902 για τη μεγάλη συνεισφορά στη χημεία των αμινοξέων, των πεπτιδίων και των πρωτεϊνών. Υπήρξε ο πρώτος που αναγνώρισε τη φύση του πεπτιδικού δεσμού, όπως και ο πρώτος που συνέθεσε πεπτίδια, φθάνοντας μέχρι και 18-πεπτίδιο, ένωση που έμοιαζε πλέον στις ιδιότητές της με πρωτεΐνη.


Η χημεία των αμινοξέων, πεπτιδίων και των πρωτεϊνών ξεκίνησε με τις ερευνητικές εργασίες του Hermann Emil Fischer
Hermann Emil Fischer
(1852-1919)
15. Συμβολή της Φυσικής στη Χημεία: Η Φύση των Ατόμων και του Χημικού Δεσμού
Κατά τα τέλη του 19ου αιώνα τα πράγματα είχαν φτάσει σε σημείο που δεν επαρκούσαν πλέον οι παρατηρήσεις και οι απλοί χημικοί στοιχειομετρικοί υπολογισμοί για να δώσουν την απάντηση στο θεμελιώδες ερώτημα: Πώς και γιατί συνδέονται τα άτομα και σχηματίζουν τις ενώσεις. 'Επρεπε πλέον να διευκρινιστεί πρώτα απ' όλα η φύση του ίδιου του ατόμου και η επιστήμη της Φυσικής είχε πλέον τα κατάλληλα εργαλεία και τους ανθρώπους που θα έδιναν τις απαντήσεις αυτές. Οι ανακαλύψεις στο θέμα αυτό άρχισαν να έρχονται με ραγδαίο ρυθμό.




Antoine Henri Becquerel (1852-1908)
Αμαύρωση φωτογραφικού φιλμ από τη ραδιενέργεια άλατος ουρανίου. Το περίγραμμα ενός χάλκινου σταυρού έδειξε ότι ορισμένα υλικά ήταν "αδιαφανή" ως προς την ακτινοβολία αυτή (περισσότερα).
Joseph John Thomson (1856-1940)
Ο σωλήνας Crookes με τον οποίο ο Thomson πραγματοποίησε τα πειράματά του (περισσότερα).
Η αρχή έγινε το 1896 με την ανακάλυψη της φυσικής ραδιενέργειας από τον Γάλλο φυσικό Antoine Henri Becquerel (1852-1908), όταν τυχαία διαπίστωσε ότι ενώσεις του ουρανίου προκαλούσαν αμαύρωση σε προστατευμένα από το φως φωτογραφικά φιλμ. 'Ηταν ήδη γνωστό ότι αντίστοιχο φαινόμενο μόνο οι ακτίνες Χ μπορούσαν να προκαλέσουν. Τιμήθηκε με το Nobel Φυσικής του 1903.

Ernst Rutherford
(1871-1937)

Hans Geiger
(1882-1945)

Ernest Marsden
(1889-1970)

Η εκτροπή ενός πολύ μικρού ποσοστού των α-σωματιδίων που προσπίπτουν σε ένα λεπτότατο φύλλο χρυσού (πάχους 0,4 μm), αποδεικνύει την παρουσία σημείων "πυκνού" θετικού φορτίου στο φύλλο, δηλαδή των πυρήνων των ατόμων χρυσού (περισσότερα).
Το 1897, ακολούθησε η ανακάλυψη του ηλεκτρονίου από τον 'Αγγλο φυσικό Joseph John Thomson (1856-1940), ως αποτέλεσμα των πειραμάτων που πραγματοποιούσε πάνω στην επίδραση του ηλεκτρικού πεδίου πάνω στις "καθοδικές ακτίνες" ενός σωλήνα Crookes. Η ανακάλυψη των ηλεκτρονίων προηγήθηκε περίπου 12 χρόνια της ανακάλυψης του πυρήνα. Ο Thomson τιμήθηκε για την ανακάλυψη αυτή με το Nobel Φυσικής του 1906. Οι ανακαλύψεις αυτές άρχισαν να αναδεικνύουν τη στενή συγγένεια μεταξύ των επιστημών της Φυσικής και της Χημείας.
Η Γαλλίδα (Πολωνικής καταγωγής) φυσικός και χημικός Marie Skłodowska Curie (1867-1934) υπήρξε η πρώτη γυναίκα που τιμήθηκε με το βραβείο Nobel. Είναι επίσης η μόνη γυναίκα που τιμήθηκε με δύο Nobel. Τo 1903, η Curie μοιράστηκε το Nobel Φυσικής με τον Becquerel για την ανακάλυψη της ραδιενέργειας και το 1911, τιμήθηκε με το Nobel Χημείας για την ανακάλυψη των στοιχείων ράδιο και πολώνιο. Στο πρόσωπο της Κιουρί αποδείχθηκε η άρρηκτη συγγένεια Φυσικής και Χημείας. Η Curie τιμήθηκε επίσης όταν το ραδιενεργό στοιχείο με ατομικό αριθμό 96 ονομάστηκε Κιούριο (Curium, Cm).
Το 1907, τιμήθηκε με το Nobel Φυσικής ο Ernst Rutherford (1871-1937) για την ανακάλυψη της διάσπασης των ραδιενεργών στοιχείων και ο οποίος θεωρείται σήμερα ο πατέρας της Πυρηνικής Φυσικής. 'Ετσι, η ουσιαστική φύση του ατόμου αποκαλύφθηκε από τα πειράματα των Thomson και Rutherford. Ο Rutherford τιμήθηκε επίσης όταν το ραδιενεργό στοιχείο με ατομικό αριθμό 104 ονομάστηκε Ραδεφόρντιο (Rutherfordium, Rf).
Το 1909, ο Αμερικανός φυσικός Robert Millikan (1868-1953), με το περίφημο πείραμα της "αιωρούμενης σταγόνας λαδιού", υπολογίζει με εξαιρετική ακρίβεια το ηλεκτρικό φορτίο του ηλεκτρονίου. Η τιμή που έδωσε ο Millikan ήταν μόλις 0,6% μικρότερη από τη σημερινή αποδεκτή τιμή (qe = 1.602176 x 10-19 C).



Robert Millikan
(1868-1953)
Henry Moseley
(1887-1915)
Niels Bohr
(1885-1962)
Το 1911, ο Αγγλο-Νεοζηλανδός χημικός και φυσικός Ernest Rutherford (1871-1937), ο Γερμανός φυσικός Hans Geiger (1882-1945), γνωστός από τον ανιχνευτή ραδιενέργειας που φέρει το όνομά του, και ο Αγγλο-Νεοζηλανδός φυσικός Ernest Marsden (1889-1970) ανακοινώνουν τα αποτελέσματα των πειραμάτων τους (το περίφημο πείραμα με το "φύλλο χρυσού") και επιβεβαιώνουν το ατομικό μοντέλο των ατόμων, με τον θετικά φορτισμένο μικροσκοπικό πυρήνα που περιβάλλεται από το αρνητικά φορτισμένο ηλεκτρονιακό νέφος.
Η ανακάλυψη της ύπαρξης πυρήνα στα άτομα κατέρριψε το λεγόμενο μοντέλο του σταφιδόψωμου (plum pudding) που προτάθηκε αρχικά από τον J. J. Thomson, σύμφωνα με το οποίο το άτομο ήταν μια θετικά φορτισμένη σφαίρα μέσα στην οποία κινούνταν τα αρνητικώς φορτισμένα ηλεκτρόνια. Τα άτομα πλέον άρχισαν να αποκτούν μορφή.
Το 1913, ο νέος 'Αγγλος χημικός Henry Moseley (1887-1915), εξετάζοντας τα φάσματα των ακτίνων Χ, που λάμβανε χρησιμοποιώντας διάφορα μεταλλικά στοιχεία ως στόχους, διαπίστωσε τη συστηματική μαθηματική σχέση μεταξύ του μήκους κύματος των ακτίνων Χ και ενός νέου χαρακτηριστικού του κάθε στοιχείου, του ατομικού αριθμού. 'Ετσι, έγινε γνωστό ότι κάθε στοιχείο, εκτός από το ατομικό βάρος, χαρακτηρίζεται και από τον ατομικό αριθμό. Από τα κενά στους ατομικούς αριθμός, προέβλεψε την ύπαρξη των στοιχείων άφνιο και ρήνιο λίγα χρόνια πριν την ανακάλυψή τους.
Το 1915, ο Moseley σε ηλικία μόλις 27 ετών, διέκοψε τις έρευνές του για να καταταγεί στον Βρετανικό στρατό. Λίγους μήνες αργότερα χάνει τη ζωή του πολεμώντας στη μάχη της Καλλίπολης κατά τον 1ο Παγκόσμιο Πόλεμο. Ο θάνατος στέρησε από τον ίδιο ένα βέβαιο Nobel και την επιστήμη από έναν εξαιρετικό επιστήμονα. Το γεγονός αυτό υπήρξε αφορμή να περάσει νόμος στην Βρετανία (και στη συνέχεια σε πολλά άλλα κράτη) που εξαιρούσε νέους λαμπρούς επιστήμονες από τη μάχιμη στρατιωτική υπηρεσία.
Τέλος, ο Δανός φυσικός Niels Bohr (1885-1962) για τη δομή των ατόμων έκανε ένα ακόμη σημαντικό βήμα ερμηνεύοντας τις γραμμές που παρουσιάζονται στο φάσμα εκπομπής του υδρογόνου και εισάγοντας την έννοια της τροχιάς των ηλεκτρονίων. Ο Bohr τιμήθηκε επίσης όταν το ραδιενεργό στοιχείο με ατομικό αριθμό 107 ονομάστηκε Μπόριο (Bohrium, Bh).




Φωτογραφίες της Marie Skłodowska Curie (1867-1934): 1η, 2η στο εργαστήριό της. 3η: Η Marie Curie και ο σύζυγός της, ο φυσικός Pierre Curie (1859-1906). 4η: Η Marie Curie και η κόρη της Irène Joliot-Curie (1897-1956), που με τον σύζυγό της Frederic Joliot-Curie (1900-1958) τιμήθηκαν με το Nobel Χημείας του 1935 για τις έρευνές τους στην τεχνητή ραδιενέργεια.


Mikhail Semyonovich Tsvet (1872-1919)
Σχηματική αναπαράσταση του πρώτου χρωματογραφικού διαχωρισμού του Tsvet
16. Σταθμοί στην Εξέλιξη της Χημείας κατά τον 20ο αιώνα
Ο 20ος αιώνας χαρακτηρίζεται από ραγδαία πορεία ανακαλύψεων τόσο για εφαρμογές στη χημική βιομηχανία, όσο και για το θεωρητικό υπόβαθρο της Χημείας. Την ίδια περίοδο ξεκινάει μία εκπληκτική πορεία ανακαλύψεων της κβαντικής χημείας, των νέων και ευαίσθητων αναλυτικών τεχνικών, της σύνθεσης πολύπλοκων οργανικών ενώσεων και πολυμερών που διαδραματίζουν σημαντική πρόοδο για την Χημεία.
Οι σημαντικότερες ανακαλύψεις στον τομέα της Χημείας και ορισμένες εμβληματικές ανακαλύψεις της φυσικής και της βιοχημείας παραθέτονται παρακάτω κατά χρονολογική σειρά:
16.1. Περίοδος 1900-1915
Το 1900, ο Γάλλος χημικός François Auguste Victor Grignard (1871-1932) ανακοινώνει μέθοδο σύνθεσης με τη βοήθεια οργανομαγνησιακών ενώσεων, που αποδείχθηκαν πολύ πιο εύχρηστες και ασφαλείς σε σχέση με άλλες δραστικές οργανομεταλλικές ενώσεις. Ο Grignard τιμήθηκε με το Nobel Χημείας του 1912.
Το 1903, ο Ρώσος βοτανολόγος Mikhail Semyonovich Tsvet (1872-1919), εξετάζοντας τις φυτικές χρωστικές ουσίες, ανακαλύπτει τη χρωματογραφία, μια εξαιρετικά χρήσιμη τεχνική τόσο για τον διαχωρισμό και ανάλυση πολύπλοκων χημικών μιγμάτων, όσο και για τον καθαρισμό χημικών ενώσεων.


Το φωτοηλεκτρονικό φαινόμενο ερμηνεύεται με την αποδοχή της σωματιδιακής φύσης του φωτός.
Το 1905, οι Γερμανοί χημικοί Fritz Haber (1868-1934) and Carl Bosch (1874-1940) αναπτύσσουν βιομηχανική μέθοδο παρασκευής αμμωνίας από το ατμοσφαιρικό άζωτο και υδρογόνο. Η μέθοδος αυτή έπαιξε ακρογωνιαίο ρόλο στην ανάπτυξη της χημικής βιομηχανίας και των λιπασμάτων για τη γεωργία, αλλά και των εκρηκτικών. Ο Haber τιμήθηκε με το Nobel Χημείας το 1918 και ο Bosch το 1931.
Το 1905, ο διάσημος Γερμανός φυσικός Albert Einstein (1879-1955) ερμηνεύει το φωτοηλεκτρικό φαινόμενο, δηλαδή την απόσπαση ηλεκτρονίων από την επιφάνεια μετάλλων (ιδιαίτερα έντονη στην περίπτωση των αλκαλίων), όταν αυτά δέχονται οπτική ακτινοβολία. Ο Einstein το ερμήνευσε κάνοντας δεκτή τη σωματιδιακή φύση του φωτός. Η λογική είναι απλή: Είναι αδύνατον η ενέργεια της οπτικής ακτινοβολίας "απλωμένη" (ως κύμα) σε όλη την φωτοευαίσθητη επιφάνεια ενός μετάλλου να επαρκεί, ώστε να επιτευχθεί η απόσπαση ηλεκτρονίου από τα επιμέρους άτομα, αφού η ενέργεια που δέχεται το κάθε άτομο είναι ελάχιστη. Αντίθετα, εάν η ενέργεια της ακτινοβολίας προσπίπτει στην επιφάνεια σε μορφή "πακέτων-βομβών", η απόσπαση αυτή καθίσταται ενεργειακά εφικτή για κάθε άτομο μετάλλου που δέχεται ένα ενεργειακό πακέτο, δηλ. το φωτόνιο. Για το έργο του αυτό τιμήθηκε με το Nobel Φυσικής του 1921. Ο Einstein τιμήθηκε επίσης όταν το ραδιενεργό στοιχείο με ατομικό αριθμό 99 ονομάστηκε Αϊνσταΐνιο (Einsteinium, Es).
Το 1907, ο Βέλγος χημικός Leo Hendrik Baekeland (1863-1944) ανακαλύπτει τον βακελίτη, πολυμερές προϊόν αντίδρασης φορμαλδεΰδης και φαινόλης, το πρώτο εμπορικά διαθέσιμο πλαστικό. Τα πολυμερή παύουν να θεωρούνται μόνο ενοχλητικά παραπροϊόντα της οργανικής σύνθεσης, αλλά προϊόντα με πολύτιμές ιδιότητες και πλήθος εφαρμογών. 'Εναρξη της Χημείας των Πολυμερών.
Το 1909, ο Δανός χημικός Søren Peder Lauritz Sørensen (1868-1939) προτείνει την έννοια του pH για τον χαρακτηρισμό της οξύτητας διαλυμάτων, όπως και δύο μεθόδους μέτρησής του: με τη βοήθεια έγχρωμων δεικτών και με ηλεκτροχημικά μέσα.






Victor Grignard
(1871-1932)
Leo Hendrik Baekeland (1863-1944)
William Henry Bragg
(1862-1942)
William Lawrence Bragg (1890-1971)
Peter Debye
(1884-1966)
Frederick Soddy
(1877-1956)
Το 1912, ο Βρετανός φυσικός και χημικός William Henry Bragg (1862-1942) και ο γιος του φυσικός William Lawrence Bragg (1890-1971) παρουσιάζουν την κρυσταλλογραφία ακτίνων-Χ, ένα σπουδαίο εργαλείο για τον προσδιορισμό της δομής κρυσταλλικών χημικών ενώσεων και διατυπώνουν τον περίφημο νόμο του Bragg (διάθλαση ακτίνων Χ από τους κρυστάλλους) πάνω στον οποίο βασίζεται η πανίσχυρη αυτή τεχνική. Για την εργασία τους τιμήθηκαν με το Nobel Φυσικής του 1915.
Την ίδια χρονιά, ο Ολλανδός φυσικοχημικός Peter Debye (1884-1966) ανακοινώνει τη θεωρία του για το μοριακό δίπολο και τη διπολική ροπή, για να περιγράψει την κατανομή των ηλεκτρικών φορτίων σε ασύμμετρα μόρια, που ευνοεί ορισμένες διπολικές έλξεις και διαμοριακές δυνάμεις, όπως ο δεσμός υδρογόνου. Προς τιμήν του, η διπολική ροπή ενός μορίου εκφράζεται σε μονάδες debye (D). O Debye τιμήθηκε με το Nobel Χημείας του 1936 για τις μελέτες του στις μοριακές δομές.
Το 1913, ο 'Αγγλος ραδιοχημικός Frederick Soddy (1877-1956) εξετάζοντας τα προϊόντα διάσπασης του ουρανίου προτείνει την ιδέα ότι ένα ραδιενεργό στοιχείο μπορεί να έχει περισσότερες από μία ατομικές μάζες και πρότεινε τον όρο "ισότοπο". Ισότοπα βέβαια έχουν και τα μη ραδιενεργά στοιχεία. Ο Soddy τιμήθηκε με το Nobel Χημείας του 1921.
Την ίδια χρονιά, ο 'Αγγλος φυσικός Joseph John Thomson (1856-1940) (γνωστότερος ως "J-J Thomson") εφαρμόζει τις γενικές θεωρίες περί θετικά φορτισμένων σωματιδίων που προκύπτουν από τον βομβαρδισμό με ταχύτατα ηλεκτρόνια και μπορούν να διαχωριστούν με βάση τον λόγο μάζας προς φορτίο (m/z). Τα πειράματά του οδήγησαν στην ανακάλυψη της φασματομετρίας μαζών. Ο Thomson τιμήθηκε με το Nobel Φυσικής του 1906 για τις εργασίες πάνω στην αγωγιμότητα των αερίων.




O Δανός Søren Sørensen (1868-1939) πρότεινε το 1909 την κλίμακα pH για τον χαρακτηρισμό της οξύτητας υδατικών διαλυμάτων. Ο προσδιορισμός του pH (στην περίπτωση άχρωμων διαλυμάτων) μπορεί να πραγματοποιηθεί με περιορισμένη ακρίβεια με τη βοήθεια οξεοβασικών δεικτών ή (ακριβέστερα) με ηλεκτροχημικές μετρήσεις. Σήμερα πραγματοποιείται σχεδόν αποκλειστικά ποτενσιομετρικά με τη βοήθεια του ονομαζόμενου "ηλεκτροδίου υάλου" και πεχαμέτρου.
16.2. Περίοδος 1916-1935
Κατά την περίοδο 1916-1923 ο Αμερικανός χημικός Gilbert N. Lewis (1875-1946) δημοσιεύει το πρωτοποριακό βιβλίο του "Το 'Ατομο και το Μόριο" (The Atom and the Molecule), που θέτει τα θεμέλια για τη θεωρία του χημικού δεσμού, ενώ το 1923 με τον Merle Randall (1888-1950) δημοσιεύουν το βιβλίο τους "Θερμοδυναμική και η Ελεύθερη Ενέργεια των Χημικών Ενώσεων" (Thermodynamics and the Free Energy of Chemical Substances), που αποτελεί το πρώτο κλασικό βιβλίο Χημική Θερμοδυναμικής. Το 1923 ο Lewis αναπτύσσει τη θεωρία περί οξέων και βάσεων με βάση την ηλεκτρονιακή δομή των χημικών ενώσεων.
Οι Irving Langmuir (1881-1957), Nobel Χημείας του 1932, και ο διάσημος Αμερικανός χημικός Linus Pauling (1901-1994), Nobel Χημείας του 1954 και Nobel Ειρήνης του 1962, προώθησαν τις ηλεκτρονιακές θεωρίες για τους χημικούς δεσμούς, το σθένος των στοιχείων και τα μοριακά τροχιακά.






Gilbert N. Lewis
(1875-1946)
Louis de Broglie
(1892-1987)
Erwin Schrödinger
(1887-1961)
Fritz London
(1900-1954)
Wallace Carothers
(1896-1937)
Erich Hückel
(1896-1980)
Η περίοδος 1924-1926 είναι ιδιαίτερα σημαντική για την Κβαντική Φυσική και Χημεία. Ο νεαρός Γάλλος φυσικός Louis de Broglie (1892-1987), Nobel Φυσικής του 1929, προτείνει την επαναστατική άποψη για την εποχή εκείνη, περί της κυματικής φύσης του ηλεκτρονίου, και αναπτύσσει την αντίληψη της δυαδική φύσης της ακτινοβολίας. Αργότερα, ο Αυστριακός Erwin Schrödinger (1887-1961) προτείνει την περίφημη εξίσωσή του, που αποτελεί τη μαθηματική θεμελίωση για την κυματική φύση της ατομικής δομής της ύλης. Ο Schrödinger τιμήθηκε με το Nobel Φυσικής του 1933.
Το 1927, οι Γερμανοί θεωρητικοί φυσικοί Fritz London (1900-1954) and Walter Heitler (1904-1981) εφαρμόζουν τις αρχές της νεοδιατυπωθείσας θεωρίας της κβαντομηχανικής για να ερμηνεύσουν τον ομοιοπολικό δεσμό στο μόριο του υδρογόνου, όπως και τις ενδομοριακές και διαμοριακές δυνάμεις (δυνάμεις London). Με τον τρόπο αυτό εγκαινιάσθηκε η γέννηση της Κβαντικής Χημείας.


Η πρώτη ένδειξη ύπαρξης του δευτερίου. Αριστερά από μια γραμμή Balmer του Η (πάνω από το βέλος) διακρίνεται η ασθενής γραμμή του D σε δείγμα φυσικού υδρογόνου ελαφρά εμπλουτισμένου σε D, που προέκυψε με εξάτμιση του υγροποιημένου αερίου (βλ. Χημική 'Ενωση του μήνα: Βαρύ ύδωρ).
Harold Clayton Urey
(1883-1981)
Το 1930, ο Linus Pauling (1901-1994) σε μια επιπλέον μεγάλη του συνεισφορά στη Χημεία προτείνει τους βασικούς κανόνες για τη χρήση της κρυσταλλογραφίας ακτίνων Χ στη μελέτη των χημικών δομών.
Το 1930, ο Αμερικανός χημικός της πολυεθνικής εταιρείας DuPont, ο Wallace Carothers (1896-1937) ανακαλύπτει το νάϋλον (nylon), το πολυμερές που έφερε επαναστατικές αλλαγές στα χημικά συνθετικά υλικά και το εμπορικά επιτυχέστερο προϊόν της χημικής βιομηχανίας.
Το 1931, ο Γερμανός φυσικοχημικός Erich Hückel(1896-1980) προτείνει τον κανόνα Hückel (4n +2), με τον οποίο προβλέπεται πότε ένα μονοκυκλικό, επίπεδο και με συζυγιακούς δεσμούς μόριο (με ένα τροχιακό p σε κάθε άτομο) έχει αρωματικό χαρακτήρα (όπου το n είναι ακέραιος αριθμός).
Το 1931, ο Αμερικανός χημικός Harold Clayton Urey (1883-1981) ανακαλύπτει το δευτέριο (deuterium, D), εξετάζοντας φασματοσκοπικά το συμπύκνωμα από τη σταδιακή εξάτμιση του υγρού υδρογόνου. Για την ανακάλυψη αυτή τιμήθηκε με το Nobel Χημείας του 1934 (βλ. Χημική 'Ενωση του μήνα: Βαρύ ύδωρ).
Το 1932, ο 'Αγγλος φυσικός James Chadwick (1891-1974) ανακαλύπτει το νετρόνιο. Για την ανακάλυψη αυτή τιμήθηκε με το Nobel Φυσικής του 1935. Ολοκληρώνεται πλέον η γνώση της βασική δομής των ατόμων.
Κατά την περίοδο 1932-1934 οι χημικοί Linus Pauling και Robert Mulliken (1896-1986, Nobel Χημείας του 1966) παρουσιάζουν μια ποσοτική θεώρηση της ηλεκτροαρνητικότητας των στοιχείων και διατυπώνουν μια κλίμακα ηλεκτροαρνητικότητας που φέρει το όνομά τους.


Glenn T. Seaborg (1912-1999)
Η πρώτη ορατή ποσότητα ένωσης του αμερικίου
(λίγα μg Am(OH)3).
16.3. Περίοδος 1936-1960
Το 1937 υπήρξε μια ιδιαίτερα αποδοτική χρονιά για την πετροχημική βιομηχανία. Ο Γάλλος χημικός μηχανικός Eugene Houdry (1892-1962) αναπτύσσει με επιτυχία μέθοδο κλασματικής καταλυτικής απόσταξης (διύλιση πετρελαίου, καταλυτική πυρόλυση). Οι τεχνική αυτή οδηγεί στη ραγδαία ανάπτυξη της πετροχημικής βιομηχανίας πετρελαίου και στην παρασκευή υψηλής ποιότητας καυσίμων για τροχοφόρα.
Το 1939, ο διάσημος Αμερικανός χημικός Linus Pauling (1901-1994) δημοσιεύει το πρωτοποριακό βιβλίο "Η Φύση του Χημικού Δεσμού" (The Nature of the Chemical Bond). Είναι ένα από τα σημαντικότερα συγγράμματα Χημείας, τόσο για τη φύση του ομοιοπολικού χημικού δεσμού, όσο και για τη θεωρία της υβριδοποίησης τροχιακών και τη θεωρία του συντονισμού, μέσω της ηλεκτραρνητικότητας των στοιχείων.
Το 1941, ο Αμερικανός χημικός Glenn T. Seaborg (1912-1999) με τη μέθοδο της δέσμευσης νετρονίων σε πυρηνικές αντιδράσεις κατάφερε να δημιουργήσει και να απομονώσει 9 στοιχεία που ανήκουν στα υπερουράνια στοιχεία, όπως και δεκάδες ισοτόπων. Το 1940 το πλουτώνιο (Pu) και στο διάστημα 1944-1958 το αμερίκιο (Am), το κιούριο (Cm), το μπερκέλιο (Bk), το καλιφόρνιο (Cf), το αϊνσταΐνιο (Es), το φέρμιο (Fm), το μεντελέβιο (Md) και το νομπέλιο (No).
Ο Seaborg υπήρξε ισχυρή επιστημονική φυσιογνωμία με τις πολυάριθμες ανακαλύψεις του στον τομέα των πυρηνικών καυσίμων και επιστημονικός σύμβουλος πολλών αμερικανών προέδρων. Για την ανακάλυψη των υπερουράνιων στοιχείων και τη μελέτη της χημείας τους ο Seaborg τιμήθηκε με Nobel Χημείας του 1935, το οποίο μοιράσθηκε με τον Αμερικανό φυσικό Edwin Mattison McMillan (1907-1991). Ο Seaborg τιμήθηκε επίσης όταν το ραδιενεργό στοιχείο με ατομικό αριθμό 106 ονομάστηκε Σιμπόργκιο (Seaborgium, Sg). Στο διαδίκτυο υπάρχει μια ωραία συλλογή άρθρων του Seaborg σχετικών με την ανακάλυψη και απομόνωση των υπερουράνιων στοιχείων.
Κατά τη διετία 1945-1946, o Ελβετός φυσικός Felix Bloch (1905-1983) και ο Αμερικανός φυσικός Edward Mills Purcell (1912-1997) ανακαλύπτουν τον Πυρηνικό Μαγνητικό Συντονισμό (Nuclear Magnetic Resonance, NMR), μια σημαντικότατη φασματοσκοπική τεχνική για τον προσδιορισμό της δομής οργανικών ενώσεων. Οι Bloch και Purcell τιμήθηκαν για την ανακάλυψή τους με το Nobel Φυσικής του 1952. Το 1954, ο Bloch υπήρξε ο πρώτος Γενικός Διευθυντής του Κέντρου Πυρηνικών Μελετών και Ερευνών (CERN) στη Γενεύη.




Felix Bloch
(1905-1983)
Edward Mills Purcell
(1912-1997)
'Ενα από τα πρώτα συστήματα NMR
(συνεχούς κύματος, 40 MHz) του 1961
Σύγχρονο σύστημα NMR (800 MHz) που χρησιμοποιείται σε δομικές μελέτες πρωτεϊνών
Το 1951, ο Linus Pauling (1901-1994) εξέτασε τη δυνατότητα χρήσης της φασματοσκοπίας των ακτίνων Χ για τον προσδιορισμό της δομής των πρωτεϊνών στον χώρο. Η δυνατότητα προσδιορισμού της δομής των πρωτεϊνών υπήρξε ανακάλυψη πρωταρχικής σημασίας για την κατανόηση της δράσης των ενζύμων και του ρόλου τους στα βιολογικά συστήματα. Για αυτήν την πρωτοποριακή έρευνα τιμήθηκε με το Nobel Χημείας του 1954.


Linus Pauling
(1901-1994)
Για την επιστημονική πολυπραγμοσύνη του Pauling και την εν γένει προσφορά του στην Επιστήμη και την Ανθρωπότητα, μπορεί να αναζητηθεί άφθονο υλικό στο διαδίκτυο, όπως ο ιστότοπος αυτός.
Θα πρέπει να σημειωθεί ότι η επιστημονική κοινότητα "όφειλε" στον Pauling το Nobel για δεκαετίες. Ενώ εμφανιζόταν συνεχώς ως υποψήφιος για το βραβείο, έβλεπε νεότερούς του επιστήμονες, να βραβεύονται ακόμη και για μικρότερης σημασίας επιστημονικά επιτεύγματα. Ουσιαστικά, το Nobel που έλαβε τελικά το 1954 δεν αφορούσε αυτή τη συγκεκριμένη ερευνητική ανακάλυψη, αλλά επιβράβευε μια ολόκληρη ζωή συνεχούς προσφοράς στην Επιστήμη της Χημείας σε πολλούς τομείς.
Ο Pauling υπήρξε ο μόνος επιστήμονας που τιμήθηκε με δεύτερο Nobel, που δεν είχε σχέση με τις Φυσικές Επιστήμες. Το 1963 τιμήθηκε με το Nobel Ειρήνης για την επιτυχή εκστρατεία του για την κατάργηση των πυρηνικών δοκιμών στην ατμόσφαιρα. Ο φιλειρηνικός ακτιβισμός του Pauling του είχε στοιχίσει τη στέρηση του διαβατηρίου του από το Υπουργείο Εξωτερικών των ΗΠΑ (1952), το οποίο του απεδόθη λίγο αργότερα, όταν χρειάστηκε να μεταβεί στη Σουηδία για την παραλαβή του πρώτου του βραβείου Nobel.
Το 1944, ο Αμερικανός χημικός Robert Burns Woodward (1917-1979) με τον συνεργάτη του William von Eggers Doering (1917-2011) ανακοίνωσαν τη σύνθεση της κινίνης, γεγονός που για εκείνη την εποχή ήταν μεγάλο επίτευγμα οργανικής σύνθεσης. Τη δεκαετία του 1940, στο εργαστήριο του Woodward συνέθεσαν σημαντικές οργανικές ενώσεις, όπως η χοληστερόλη, η κορτιζόνη, η στρυχνίνη, το λυσεργικό οξύ, η ρεσερπίνη και άλλα φυσικά προϊόντα με αρκετά πολύπλοκη μοριακή δομή. Στην αρχή της δεκαετίας του 1960 ο Woodward και συνεργάτες συνέθεσαν με πολυάριθμα στάδια το εξαιρετικά πολύπλοκο μόριο της Βιταμίνης Β12. Ο Woodward τιμήθηκε για το πολύπλευρο συνθετικό του έργο με το Nobel Χημείας του 1965.
Το 1952 ο Robert Burns Woodward (1917-1979), ο 'Αγγλος χημικός Geoffrey Wilkinson (1921-1996) και ο Γερμανός χημικός Ernst Otto Fischer (1918-2007) διευκρίνισαν τη δομή του φερροκενίου και καθιέρωσαν την Οργανομεταλλική Χημεία ως ιδιαίτερο κλάδο της Χημείας. Οι Geoffrey Wilkinson και Ernst Otto Fischer τιμήθηκαν το 1973 με το Nobel Χημείας για τις ανακαλύψεις τους, που συνέβαλαν στην αλματώδη ανάπτυξη της Οργανομεταλλικής Χημείας.

Robert Burns Woodward (1917-1979)

Geoffrey Wilkinson
(1921-1996)

Ernst Otto Fischer
(1918-2007)


Η σύνθεση και στη συνέχεια η διευκρίνιση της δομής του φερροκενίου (η πρώτη γνωστή ένωση "σάντουιτς") κατά τη δεκαετία του 1950, έδωσε σημαντική ώθηση στο πεδίο της Οργανομεταλλικής Χημείας (βλ. Χημική ένωση του μήνα: φερροκένιο).
Το 1953 υπήρξε μια ιδιαίτερα σημαντική χρονιά για την επιστήμη. Οι Αμερικάνος βιολόγος James Watson (1928), ο 'Αγγλος βιοφυσικός Francis Crick (1916-2004), ο Νεοζηλανδός βιολόγος Maurice Wilkins (1916-2004) και η Αγγλίδα βιοφυσικός Rosalind Franklin (1920-1958) με την τριπλή δημοσίευση των ερευνητικών τους εργασιών στο περιοδικό Nature πρότειναν τη δομή της διπλής έλικας για το μόριο του DNA (δυο αλληλοσυγκρατούμενοι πολυνουκλεοτιδικοί κλώνοι). Η ανακάλυψη αυτή θεωρήθηκε εξαιρετικά σημαντική για την κατανόηση της κληρονομικότητας. 'Ετσι, έγινε κατανοητό πλέον ότι οι γενετικές πληροφορίες ενός οργανισμού αποθηκεύονται στην αλυσίδα του μορίου DNA, υπό τη μορφή της αλληλουχίας των δεοξυριβονουκλεοτιδίων. Αυτό ονομάσθηκε "κεντρικό δόγμα της μοριακής γενετικής". Οι Watson, Crick και Wilkins τιμήθηκαν με το Nobel Ιατρικής και Φυσιολογίας του 1963.





James Watson
(1928)
Francis Crick
(1916-2004)
Maurice Wilkins
(1916-2004)
Rosalind Franklin
(1920-1958)
Το 1953, ο Αμερικανός χημικός και βιολόγος Stanley Miller (1930-2007) και Harold Clayton Urey (που είχε ανακαλύψει το δευτέριο) στο Πανεπιστήμιο του Σικάγου έκαναν ένα πρωτοποριακό πείραμα για τη σύνθεση οργανικών ενώσεων σε προβιοτικές συνθήκες. Ο βομβαρδισμός με ηλεκτρικές εκκενώσεις μίγματος αερίων CH4, NH3, H2 και υδρατμών, δηλ. σε συνθήκες που προσομοίαζαν εκείνες της αρχέγονης ατμόσφαιρας της Γης, έδωσε έναν "ζωμό" που περιείχε μια ποικιλία αμινοξέων και άλλων οργανικών ουσιών, πρόδρομων ενώσεων μορίων βιολογικής σημασίας (πρωτεϊνών, DNA). Το πείραμα των Miller-Urey περιγράφεται στις εισαγωγικές σελίδες σχεδόν κάθε βιβλίου Βιοχημείας και αποτέλεσε ένα σημαντικό βήμα στην αναζήτηση μιας τεκμηριωμένης θεωρία ως προς την προέλευση της ζωής στον πλανήτη Γη πριν από 3,5-4 δισεκατομμύρια χρόνια.




O Stanley Miller (1930-2007) και η περίφημη πειραματική διάταξη προσομοίωσης της αρχέγονης ατμόσφαιρας της Γης.
Ο Frederick Sanger (1918) και το μόριο της ινσουλίνης στο οποίο προσδιόρισε την αλληλουχία των αμινοξέων.
Κατά την περίοδο 1951-1953 ο 'Αγγλος βιοχημικός Frederick Sanger (1918) βρήκε τρόπο προσδιορισμού της αλληλουχίας των αμινοξέων της ινσουλίνης (βλ. Χημική ένωση του μήνα: Ινσουλίνη), που αποτελείται από δύο πεπτιδικές αλυσίδες συνδεόμενες με δύο δισουλφιδικές γέφυρες. Ο Sanger τιμήθηκε για την ανακάλυψή του αυτή με το Nobel Χημείας του 1958. Το 1980 ο Sanger μαζί με τον Αμερικανό βιοχημικό, φυσικό και μοριακό βιολόγο Walter Gilbert (1932) μοιράσθηκαν το Nobel Χημείας για τη συμβολή τους στον προσδιορισμό της ακολουθίας των νουκλεϊνικών βάσεων στα νουκλεϊνικά οξέα (DNA), ενώ το άλλο μισό του βραβείου απονεμήθηκε στον Paul Berg (1926) για τις βασικές βιοχημικές έρευνες στον τομέα των νουκλεϊνικών οξέων και ιδιαίτερα του ανασυνδυασμένου DNA.



Karl Waldemar Ziegler
(1898-1973)
Giulio Natta
(1903-1979)
Με τους καταλύτες Ziegler-Natta (εδώ μεταλλοκένιο Ti ή Zr), ελέγχεται ο βαθμός πολυμερισμού των α-ολεφινών και η στερεο- χημεία του λαμβανόμενου πολυμερούς.
Η δεκαετία του 1950-1960 συνέβη μια ανακάλυψη ιδιαίτερα μεγάλης επιστημονικής και οικονομικής σημασίας για τη βιομηχανία των πολυμερών. Ο Γερμανός χημικός Karl Waldemar Ziegler (1898-1973), σε συνεργασία με τον Ιταλό χημικό μηχανικό Giulio Natta (1903-1979), βρήκαν τους περίφημους καταλύτες, γνωστούς πλέον ως καταλύτες Zigler-Natta. Με τους καταλύτες αυτούς (οργανομεταλλικές ενώσεις του αργιλίου, του τιτανίου και ζιρκονίου) μπορούσαν να ελέγξουν τον πολυμερισμό α-ολεφινών (και κυρίως του αιθυλενίου και του προπυλενίου) για σχηματισμό πολυμερών καθορισμένης περιοχής μοριακού βάρους και στερεοχημείας (τακτικότητας). Για την ανακάλυψή τους αυτοί οι Ziegler και Natta τιμήθηκαν με το Nobel Χημείας του 1963.
16.4. Περίοδος 1961-1995
Το 1962 ο Αμερικανός βιοχημικός Robert Bruce Merrifield (1921-2006), καθηγητής στο Ινστιτούτο Ροκφέλλερ, Νέα Υόρκη, ανακοίνωσε για πρώτη φορά την ανακάλυψη της αυτοματοποιημένης πεπτιδικής σύνθεσης (σύνθεση στερεάς φάσης κατά Merrifield) σε υπόστρωμα πολυστυρενίου, που απλούστευσε κατά πολύ την παρασκευή πεπτιδίων. Ο Merrifield τιμήθηκε με το Nobel Χημείας του 1984.
Κατά την περίοδο 1953-1960, στα Πανεπιστήμια του Καίμπριτζ και της Οξφόρδης, ο Αυστριακής καταγωγής Βρετανός μοριακός βιολόγος Max Perutz (1914-2002) και ο 'Αγγλος χημικός John Kendrew (1917-1997) πραγματοποιούν μελέτες σφαιρικών πρωτεϊνών με ακτίνες-Χ. Είναι η "χρυσή περίοδος" της μελέτης των πρωτεϊνικών κρυστάλλων μεγάλης σημασίας βιολογικών μορίων σε ερευνητικά εργαστήρια. Οι δύο επιστήμονες επιβραβεύονται με το Nobel Χημείας του 1962 για τη εξακρίβωση της τρισδιάστατης δομής της αιμοσφαιρίνης και της μυοσφαιρίνης.
Το 1962, ο 'Αγγλος χημικός Neil Bartlett (1932-2008) στο πανεπιστήμιο Berkeley της Καλιφόρνιας συνέθεσε για πρώτη φορά φθοριωμένες ενώσεις ευγενών αερίων, που μέχρι τότε θεωρούσαν ότι ήταν τελείως αδρανή. Αρχικά συνέθεσε την ένωση εξαφθορολευκοχρυσικό ξένον, Xe+[PtF6]- και στη συνέχεια φθοριωμένες ενώσεις ξένου (XeF2, XeF4 και XeF6). Ακολούθησαν η σύνθεση του οξειδίου του ξένου(VI), του υπερξενικού οξέος (H4XeO6) και αλάτων του.

Robert Bruce Merrifield
(1921-2006)

Μια από τις πειραματικές διατάξεις που χρησιμοποίησε ο Merrifield για την αυτοματοποιημένη σύνθεση πεπτιδίων.

Neil Bartlett
(1932-2008)

Τη δεκαετία του 1960 προκάλεσε έκπληξη η σύνθεση των πρώτων σταθερών ενώσεων του ευγενούς αερίου ξένον. Σήμερα, πολλές από τις ενώσεις αυτές είναι εμπορικά διαθέσιμες (στη φωτογραφία φιάλες με XeF2)
Το ίδιο έτος, o Ούγγρος χημικός George Andrew Olah (1927) ανακαλύπτει τρόπο παρασκευής και σταθεροποίησης των καρβοκατιόντων μέσω αντιδράσεων υδρογονανθράκων με σουπεροξέα, όπως το περίφημο "μαγικό οξύ" (μίγμα SbF5 - HSO3F), τα οποία χαρακτηρίζονται από μια ισχυρότατη πρωτονιοδοτική ικανότητα. Ο Olah βραβεύθηκε για τη σημαντική του συμβολή στη χημεία των καρβοκατιόντων και των αντιδράσεων τους με το Nobel Χημείας του 1994 (βλ. Χημική ένωση του μήνα: Μαγικό οξύ).
Το 1964, η Βρετανίδα χημικός Dorothy Mary Crowfood-Hodgkin (1910-1994) τιμήθηκε με το Nobel Χημείας για τις πολυετείς έρευνές της πάνω στην εξακρίβωση της τριτογενούς δομής πρωτεϊνών με κρυσταλλογραφία ακτίνων Χ. Η Hodgkin, με κρυσταλλογραφία ακτίνων Χ, συνέβαλε στη μελέτη της ινσουλίνης, πενικιλίνης και της βιταμίνης Β12.




Max Perutz
(1914-2002)
John Kendrew
(1917-1997)
George Andrew Olah
(1927)
Dorothy Mary Crowfood-Hodgkin (1910-1994)
Το 1964, ο Ελβετός φυσικοχημικός Richard Robert Ernst (1933) πρότεινε την εφαρμογή του Ταχέος Μετασχηματισμού Fourier (Fast Fourier Transform, FFT) στη φασματοσκοπία του Πυρηνικού Μαγνητικού Συντονισμού (NMR). Με την εφαρμογή σύντομων και ισχυρών παλμών κατά τη λήψη του φάσματος, αντί της συνεχούς σάρωσης, βελτιώνεται η ευαισθησία της λήψης του φάσματος και με μαθηματική επεξεργασία του λαμβανόμενου σήματος (σήμα ως προς χρόνο) λαμβάνεται το φάσμα NMR (σήμα ως προς συχνότητα). Η μέθοδος αργότερα βρήκε σημαντική εφαρμογή στο NMR δύο διαστάσεων (2D-NMR) και της απεικόνισης μαγνητικού συντονισμού, γνωστότερης ως Μαγνητική Τομογραφία (Magnetic Resonance Imaging, MRI) με εφαρμογές στην ιατρική διάγνωση ασθενειών. Ο Ernst τιμήθηκε με το Nobel Χημείας του 1991.
Το 1965, οι Αμερικανοί χημικοί Robert Burns Woodward (1917-1979) και Roald Hoffmann (1937) πρότειναν τους κανόνες Woodward-Hoffmann (rules), οι οποίοι χρησιμοποιούν τη συμμετρία των μοριακών τροχιακών για να ερμηνεύσουν τη στερεοχημεία των χημικών αντιδράσεων και ιδιαίτερα των περικυκλικών αντιδράσεων. Οι Roald Hoffman και ο Ιάπωνας χημικός Kenichi Fukui (1918-1998), ο οποίος εισήγαγε μια απλοποιημένη προσέγγιση στα μοριακά τροχιακά για τις περικυκλικές αντιδράσεις με την εξέταση των μετωπικών τροχιακών, HOMO και LUMO, τιμήθηκαν για τις ανακαλύψεις στον τομέα των μοριακών τροχιακών με το Nobel Χημείας του 1981.
Κατά τις δεκαετίες 1950, 1960 και 1970 ένα από τα πιο διάσημα εργαστήρια οργανικών συνθέσεων και ανακάλυψης νέων συνθετικών μεθόδων υπήρξε το εργαστήριο του Elias James Corey (1928) στο Πανεπιστήμιο Harvard. Η ομάδα του εργαστηρίου Corey, στην οποία εργάστηκαν πολυάριθμοι χημικοί, υπήρξε εξαιρετικά δραστήρια. Στο εργαστήριο αυτό αναπτύχθηκαν περισσότερες από 300 συνθετικές μέθοδοι και πραγματοποιήθηκαν περισσότερες από 300 ολικές συνθέσεις πολύπλοκων οργανικών ενώσεων. Ο Corey ανέπτυξε τη μεθοδολογία της ρετροσυνθετικής ανάλυσης στη χημική σύνθεση. Το 1989, οι Corey EJ και Chen X-M δημοσίευσαν το σημαντικό βιβλίο "The Logic of Chemical Synthesis", που αποτελεί σταθμό στην οργανική σύνθεση. Ο Corey τιμήθηκε με το Nobel Χημείας του 1990, για την ανάπτυξη της ρετροσυνθετικής ανάλυσης.
Το 1971, ο Γάλλος χημικός Yves Chauvin (1930) ερμηνεύει τον μηχανισμό της ολεφινικής μετάθεσης, δηλαδή ενός είδους ανακατανομής των θραυσμάτων αλκυλενίου κατά τη σχάση του διπλού δεσμού άνθρακα-άνθρακα σε ολεφίνες. Η ανακάλυψη έπαιξε σημαντικό ρόλο στην έρευνα της οργανικής σύνθεσης και στη Βιομηχανική Χημεία (πετρέλαια, φάρμακα, πολυμερή). Ο Chauvin μαζί με τους Richard R. Schrock (1945) και Robert H. Grubbs (1942) τιμήθηκαν για τη συμβολή τους στο πεδίο της ολεφινικής μετάθεσης με το Nobel Χημείας του 2005.






Richard Robert Ernst
(1933)
Roald Hoffmann
(1937)
Kenichi Fukui
(1918-1998)
Elias James Corey
(1928)
Yves Chauvin
(1930)
Karl Barry Sharpless
(1941)
To 1975, ο Αμερικανός χημικός Karl Barry Sharpless (1941) και οι συνεργάτες τους ανακάλυψαν τις αντιδράσεις της στερεοεκλεκτικής οξείδωσης, συμπεριλαμβανομένης της εποξείδωσης Sharpless, της ασυμμετρικής διϋδροξυλίωσης και οξυαμίνωσης Sharpless. To 2001 τιμήθηκε με Nobel Χημείας για τη συμβολή του στην ανακάλυψη των στερεοεκλεκτικών αντιδράσεων.
Το 1985, η επιστημονική κοινότητα εξεπλάγη όταν ο Βρετανός χημικός Harold Kroto (1939), ο Αμερικανός χημικός Robert Curl (1933) και ο Αμερικάνος χημικός, φυσικός και αστρονόμος Richard Smalley (1943-2005) ανακάλυψαν τα φουλερένια, μια άγνωστη μέχρι τότε μορφή άνθρακα, όπου τα άτομα είναι συνδεμένα μεταξύ τους κατά τρόπο που να σχηματίζονται μόρια με τη μορφή μπάλας, με επιφάνειες αποτελούμενες από πενταμελείς ή εξαμελείς ανθρακικούς δακτυλίους. Η πλέον γνωστή ένωση είναι αυτή με 60 άτομα άνθρακα (C60). Οι ενώσεις αυτές είναι οι μόνες μορφές άνθρακα που παρουσιάζουν κάποια διαλυτότητα σε διάφορους οργανικούς διαλύτες. Το όνομα "φουλερένια" προέρχεται από την ομοιότητα των μορίων αυτών με τους "γεωδετικούς" θόλους κτηρίων, που σχεδίασε ο αρχιτέκτονας Richard Buckminster Fuller (1895-1983). Οι Harold Kroto, Robert Curl και Richard Smalley τιμήθηκαν για αυτήν την ανακάλυψή τους με το Nobel Χημείας του 1996.





Harold Kroto
(1939)
Robert Curl
(1933)
Richard Smalley
(1943-2005)
Μόριο του φουλερένιου C60
Ο αρχιτέκτονας Richard Buckminster Fuller (1895-1983) μπροστά σε ένα γεωδετικό θόλο
Το 1994-1996, πραγματοποιήθηκε η πρώτη ολική σύνθεση του αντικαρκινικού φαρμάκου Taxol (υπάρχει ως φυσικό προϊόν στον φλοιό του κορμού ενός είδους ελάτου) από τις ερευνητικές ομάδες του Κύπριου χημικού Kyriakos C. Nicolaou (1946) και των Αμερικανών χημικών Robert A. Holton και Samuel Danishefskiy (1936) (βλ. Χημική ένωση του μήνα: Ταξόλη).




Οι πρωταγωνιστές της ολικής σύνθεσης της ταξόλης: Αριστερά: Robert A Holton, Πολιτειακό Πανεπιστήμιο Φλόριντα. Μέσον: Kyriacos C. Nicolaou (1946, Κύπρος), Πανεπιστήμιο Καλιφόρνιας, στο San Diego. Δεξιά: Samuel J. Danishefsky (1936), Πανεπιστήμιο Columbia Νέας Υόρκης.
Το μόριο της ταξόλης, η ολική σύνθεση της οποίας περιλαμβάνεται πλέον στα αριστουργήματα της Οργανικής Σύνθεσης.
16.5. Οι σχετικά νεότερες εξελίξεις μέσω των Nobel Χημείας 1990-2010
Τα Βραβεία Nobel Χημείας των τελευταίων 15 χρόνων και η αιτιολογήσεις τους, όπως περιγράφονται από τη Επιτροπή Nobel της Βασιλικής Σουηδικής Ακαδημίας Επιστημών, αποτελούν ένα τρόπο συνοπτικής καταγραφής των σημαντικότερων επιτευγμάτων και ανακαλύψεων στους διάφορους τομείς της χημείας που πραγματοποιήθηκαν κατά τα τελευταία 30-40 χρόνια. Στις ανακαλύψεις αυτές σημαντικό υπάρχουν ανακαλύψεις με βιολογικά μόρια και βιοχημικές διεργασίες, νέες μεθόδους, νέα υλικά και ρύπανση του περιβάλλοντος. Τα βραβεία αυτά και η συνοπτική-τυπική αιτιολόγησή τους έχουν ως εξής:
1990, Elias James Corey: "Για την ανάπτυξη της θεωρίας και της μεθοδολογίας στην οργανική σύνθεση".
1991, Richard R. Ernst: "Για τη συνεισφορά του στην ανάπτυξη της μεθοδολογίας της φασματοσκοπίας πυρηνικού μαγνητικού συντονισμού (NMR) υψηλής διακριτικής ικανότητας".
1992, Rudolf A. Marcus: "Για τη συνεισφορά του στη θεωρία των αντιδράσεων μεταφοράς ηλεκτρονίων σε χημικά συστήματα.
1993, Kary B. Moullis, Michael Smith: "Για τη συνεισφορά τους στην ανάπτυξη της χημείας που βασίζεται στο DNA", κατά το ήμισυ στον πρώτο "Για την εφεύρεση των μεθόδων που βασίζονται στην αλυσιδωτή αντίδραση πολυμεράσης (PCR)" και κατά το υπόλοιπο ήμισυ στον δεύτερο "Για τη θεμελιακή συνεισφορά του στην καθιέρωση της βασιζόμενης σε ολιγονουκλεοτίδια κατευθυνόμενη κατά θέση μεταλλαξιγένεση και στην εφαρμογή της για τη μελέτη των πρωτεϊνών".
1994, George Α. Olah: "Για τη συνεισφορά του στη χημεία των καρβοκατιόντων".
1995, Paul J. Crutzen, Mario J. Molina, F. Sherwood Rowland: "Για την εργασία τους στην ατμοσφαιρική χημεία και ειδικότερα σε ό,τι αφορά τον σχηματισμό και τη διάσπαση του όζοντος".





Paul J. Crutzen (1933)
Mario J. Molina (1943)
F. Sherwood Rowland (1927)
Οι έρευνες των Crutzen, Molina και Rowland πάνω στις καταστροφικές επιπτώσεις των χλωροφθορανθράκων στο τροποσφαιρικό όζον, είχαν ως αποτέλεσμα τη σταδιακή απαγόρευση της παραγωγής και κάθε είδους χρήσης αυτών των ουσιών (βλ. Χημική ένωση του μήνα: 'Οζον)
1996, Harold W. Croto, Robert Curt, Richard E. Smalley: "Για την ανακάλυψη των φουλερενίων".
1997, Paul D. Boyer, John E. Walker, Jens C. Skou: Το ήμισυ του βραβείου στους δύο πρώτους "Για τη διευκρίνιση του ενζυμικού μηχανισμού σύνθεσης της τριφωσφορικής αδενοσίνης (ATP)" και το υπόλοιπο ήμισυ στον τρίτο "Για την πρώτη ανακάλυψη ενός ιοντο-μεταφορικού ενζύμου της Na+,K+ - ATPάσης".
1998, Walter Kohn, John A. Pople: Στον πρώτο "Για την ανάπτυξη της συναρτισοειδούς θεωρίας" και στον δεύτερο "για την ανάπτυξη υπολογιστικών μεθόδων στην Κβαντική Χημεία".
1999, Ahmed H. Zewall: "Για τις μελέτες του στις μεταπτωτικές καταστάσεις χημικών αντιδράσεων χρησιμοποιώντας φασματοσκοπία φεμτοδευτερολέπτων".



Ahmed H. Zewall (1946)
Σύστημα υπερταχέος laser στερεάς κατάστασης (Ti : σαπφείρου) που χρησιμοποιείται
για τη μελέτη ταχύτατων αντιδράσεων
Τυπικό 3-D φάσμα (απορρόφηση ως συνάρτηση μήκους κύματος - χρόνου)
2000, Allan J. Heeger, Allan G. McDiarmidt, Hideki Shirakawa: "Για την ανακάλυψη κα την ανάπτυξη αγώγιμων πολυμερών".
2001, William S. Knowles, Ryoji Noyori, K.Barry Sharpless: Το ήμισυ του βραβείου στους δύο πρώτους "Για την εργασία του πάνω στις χειραλικά καταλυόμενες αντιδράσεις υδρογόνωσης" και το υπόλοιπο ήμισυ στον τρίτο "Για την εργασία του πάνω στις χειραλικά καταλυόμενες αντιδράσεις οξείδωσης".
2002, John B. Fenn, Koici Tanaka, Kurt Wüthrich: "Για την ανάπτυξη μεθόδων ταυτοποίησης και δομικής ανάλυσης βιολογικών μακρομορίων", κατά το ήμισυ στους δύο πρώτους "Για την ανάπτυξη των μεθόδων ιοντισμού μαλακής εκρόφησης για αναλύσεις βιολογικών μακρομορίων με φασματομετρία μάζας" και κατά το υπόλοιπο ήμισυ στον τρίτο "Για την ανάπτυξη μεθόδων μαγνητικού πυρηνικού συντονισμού για τον προσδιορισμό της τρισδιάστατης δομής βιολογικών μακρομορίων σε διάλυμα".
2003, Peter Agre, Robert MacKinnon: "Για τις ανακαλύψεις σχετικά με τις μεμβράνες των κυττάρων", στον πρώτον "για την ανακάλυψη διαύλων ύδατος" και στον δεύτερο "Για τις δομικές και μηχανιστικές μελέτες των διαύλων ιόντων".
2004, Aaron Ciechanover, Avram Hershko, Irwin Rose: "Για την ανακάλυψη της απόπτωσης των πρωτεϊνών με την παρέμβαση της ουβικιτίνης".
2005, Ives Chauvin, Robert J. Grubbs, Richard R. Schrock: "Για την ανάπτυξη μεταθετικών μεθόδων στην οργανική σύνθεση".
2006, Rodger D. Kormberg: "Για τις μελέτες του σε μοριακή βάση των μηχανισμών αντιγραφής γενετικών πληροφοριών σε ευκαρυωτικά κύτταρα".
2007, Gerhard Ertl: "Για τις μελέτες του επί των χημικών διεργασιών σε επιφάνειες στερεών".
2008, Osama Shimomura, Martin Chalfie, Rogen Y. Tsien: "Για την ανακάλυψη, ανάπτυξη και πολλαπλές εφαρμογές της πράσινης φθορίζουσας πρωτεΐνης (Green Fluorescent Protein, GFP)".
2009, Venkatraman Ramakrishnan, Thomas A. Steitz, Ada E. Yonath: "Για τις μελέτες τους πάνω στη δομή και τη λειτουργία των ριβοσωμάτων".
2010, Richard F. Heck, Erichi Negishi, Akira Suazuki: "Για τις αντιδράσεις διασταυρούμενης σύνθεσης που καταλύονται από παλλάδιο".
17. Επίλογος
Η ιστορία της Χημείας συνεχίζεται με αμείωτο ερευνητικό και επιστημονικό ενδιαφέρον. Παρά τη ραγδαία εξέλιξη των Θετικών Επιστημών και ιδιαίτερα της Χημείας, τα τελευταία 50 χρόνια, παραμένουν ανεξερεύνητες πολλές επιστημονικές περιοχές και έτσι, ακόμη και σήμερα παραμένουν πολλά ερωτήματα και πολλές ενδιαφέρουσες πλευρές των φυσικών φαινομένων που δεν έχουν εξηγηθεί επαρκώς.
'Οπως και στους άλλους κλάδους της επιστήμης, η Χημεία είχε μια εξελικτική πορεία με πολλές ανατροπές, λανθασμένες απόψεις και σφάλματα στην ερμηνεία χημικών φαινόμενων. Παρ' όλα αυτά η πολύχρονη πειραματική εργασία χιλιάδων χημικών και οι οξυδερκείς παρατηρήσεις τους διαλεύκαναν πολλές πλευρές της χημικής δομής και των χημικών ιδιοτήτων των διαφόρων ουσιών. Η Χημεία συνέβαλε αποφασιστικά στην αύξηση του προσδόκιμου ζωής του ανθρώπου, στη θεραπεία πολλών ασθενειών και στην ανακάλυψη μεθόδων και νέων υλικών, που βελτίωσαν την ποιότητα της ζωής του ανθρώπου.
Η τεκμηριωμένη πειραματική εργασία πολλών χημικών και η επανάληψη των πειραματικών δεδομένων παραμένει η μόνη ασφαλής μέθοδος για την πρόοδο της επιστήμης. Στην ιστορία της Χημείας υπήρξαν πολλοί επιστήμονες οι οποίοι με τα ευφυή πειράματά τους και την εύστοχη ερμηνεία των φυσικοχημικών αποτελεσμάτων συνέβαλαν στην πρόοδο της επιστήμης και στη διαφώτιση του ανθρώπου για τα φυσικά φαινόμενα πάνω στον πλανήτη Γη και στο Σύμπαν.
Πηγή http://www.chem.uoa.gr/
Εγγραφή σε:
Αναρτήσεις (Atom)